- 2021-08-06 发布 |
- 37.5 KB |
- 13页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
新教材高中化学第七章有机化合物第3节第2课时乙酸课件 人教版必修第二册
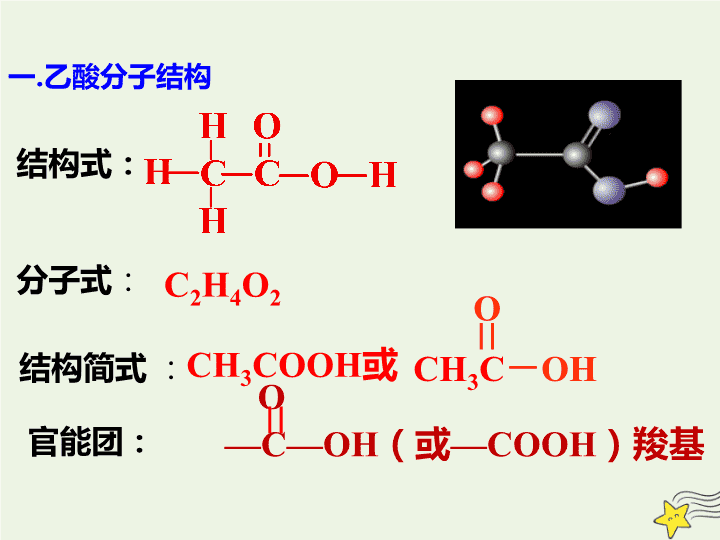
第三节 乙醇与乙酸 学习目标 1. 了解乙酸的组成、结构、物理性质和主要应用。 2. 掌握乙酸的主要化学性质。 3. 了解乙酸与人类生活和健康的知识,体会学习有机化学的意义,提高科学素养和生活质量。 第 2 课时 乙酸 一 . 乙酸分子结构 分子式 : C 2 H 4 O 2 结构式: 结构简式 : CH 3 COOH 或 O CH 3 C - OH 官能团: —C—OH (或 —COOH )羧基 O 颜色 : 无色 气味 : 有强烈刺激性气味 挥发性: 易挥发(沸点 : 117.9℃ ) 低 (16.6℃) ( 无水乙酸又称为 : 冰醋酸 ) 溶解性: 易溶于水、 乙醇等溶剂 二 . 乙酸的物理性质 状态 : 液体 熔点: 请利用下列药品设计实验方案来证明乙酸具有酸性? 新制 Cu(OH) 2 悬浊液、乙酸溶液、石蕊试液、碳酸钠粉末 实验步骤 现象 1 石蕊溶液中加入乙酸 2 新制 的 Cu(OH) 2 悬浊液再加入少量的乙酸溶液 3 碳酸钠粉末 中加入乙酸 溶液变红 Cu(OH) 2 溶解,生成蓝色溶液 碳酸钠粉末溶解 有气泡产生 实验探究一:乙酸具有酸性吗? 结论:乙酸具有 酸性 ( 1 )酸的通性 ① 使酸碱指示剂变色 ② 与碱反应 ④ 与活泼金属反应 ⑤ 与碱性氧化物反应 ③ 与部分盐反应 三 . 乙酸的化学性质 CH 3 COOH CH 3 COO - + H + 如何除水垢? 水垢主要成份: CaCO 3 离子方程式: 2CH 3 COOH+CaCO 3 =Ca 2+ +2CH 3 COO — +H 2 O +CO 2 ↑ 实验探究二:乙酸乙酯的制取 乙醇 浓硫酸 乙酸 饱和 碳酸钠 溶液 步骤: 在大试管里加入 3mL 乙醇 , 然后 边振荡 试管边慢慢 加入 2mL 浓硫酸 和 2mL 冰醋酸 ; 在另一支试管中加入 饱和 Na 2 CO 3 溶液 ; 按照图所示连接好装置 , 加热观察现象 。 ( 1 )导管口为什么要在溶液的液面上方? 乙醇 浓硫酸 乙酸 饱和 碳酸钠 溶液 ( 2 )药品的添加顺序如何? 防止倒吸 先加乙醇再加浓 H 2 SO 4 最后加乙酸 思考 乙酸乙酯 现象 :溶液分层,上层有无色透明的油状液体产生 , 并有香味。 O O CH 3 — C — OH+H — O — C 2 H 5 CH 3 — C — O — C 2 H 5 + H 2 O 浓 H 2 SO 4 酸脱羟基、醇脱氢 ( 羟基上的 ) 取代反应 实质: 反应类型: ( 2 )酯化反应 定义: 酸和醇 反应生成 酯和水 的反应叫做酯化反应。 O O CH 3 — C — OH+H — O — C 2 H 5 CH 3 — C — O — C 2 H 5 + H 2 O 浓 H 2 SO 4 CH 3 COOCH 3 + H 2 O CH 3 COOH + HOCH 3 浓 H 2 SO 4 乙酸甲酯 试一试:请同学们试着写出乙酸和甲醇反应的化学方程式。 练习 下列物质中,能与醋酸发生反应的是( ) ①乙醇 ②金属铝 ③甲烷 ④碳酸钙 ⑤氢氧化钠⑥ 氧化镁 A.①③④⑤⑥ B.②③④⑤ C. ①②④⑤⑥ D. 全部 C O CH 3 —C—O—H 课堂小结 一 . 乙酸分子结构 二 . 乙酸的物理性质 三 . 乙酸的化学性质 ( 1 )酸的通性 CH 3 COOH CH 3 COO - + H + ( 2 )酯化反应 CH 3 COOH + HOC 2 H 5 CH 3 COOC 2 H 5 +H 2 O 浓 H 2 SO 4 △ 酸性 酯化反应查看更多