- 2021-08-06 发布 |
- 37.5 KB |
- 6页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
化学卷·2018届江西省奉新县第一中学高二上学期期末考试(2017
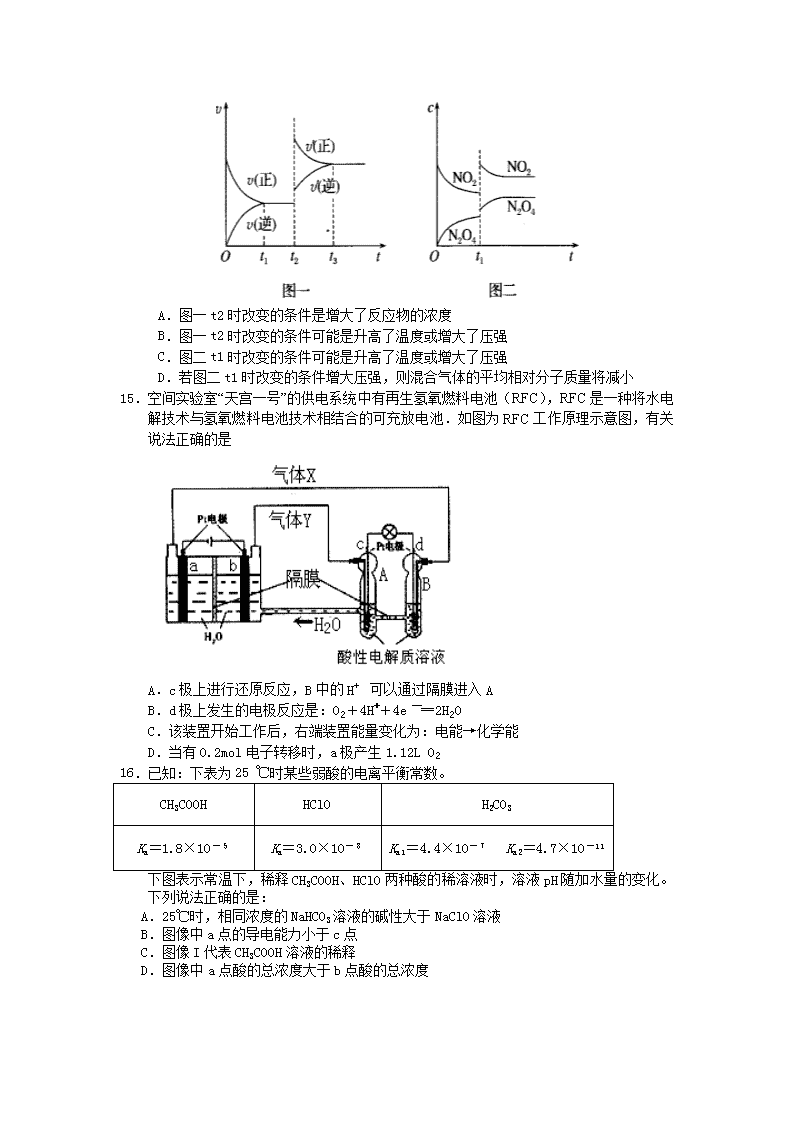
高二上学期期末考试 化学试卷 可能用到的相对原子质量: H-1 C-12 N-14 O-16 Mg-24 Al-27 Cu-64 第Ⅰ卷 一、选择题:(本题含16个小题,每小题3分,共48分。每小题只有一个正确答案) 1.我国宋代《梦溪笔谈》记载的有关自然科学知识中有255条科技史实。部分如下: ①信州铅山县有苦泉,流以为涧。挹其水熬之,则成胆矾。烹胆矾则成铜;熬胆矾铁釜, 久之亦化为铜。水能为铜,物之变化,固不可测。 ②取精铁锻之百余火,每锻称之,一锻一轻,至累锻而斤两不减,则纯钢也,虽百炼,不耗矣。 上述科技史实没有涉及到的化学反应类型有: A.化合反应 B.分解反应 C.置换反应 D.复分解反应 2.下列气体既可以用碱石灰干燥又可以用浓硫酸干燥的是: A.Cl2 B.CH4 C.NH3 D.SO2 3.下列说法正确的是(NA表示阿伏加德罗常数的值) A.30g乙烷含有的共价键数目为8NA B.2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA C.1mol甲基含10 NA个电子 D.标况下,22.4L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA 4. 在反应3H2 + N2 2NH3 中,经一段时间后,氨的浓度增加了0.6 mol•L-1,在此时间内 用H2表示的平均反应速率为0.45 mol•L-1s-1则反应所经过的时间为 A.0.44s B.1s C.2s D.0.33s 5.下列热化学方程式正确的是(注:ΔH的绝对值均正确) A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g) ΔH=-1367.0 kJ·mol-1 (燃烧热) B.Ba(OH)2(aq)+2HCl(aq)===BaCl2(aq)+2H2O(l) ΔH=-57.3 kJ·mol-1 (中和热) C.S(s)+O2(g)===SO2(g) ΔH=-269.8 kJ·mol-1 (反应热) D.2NO2===O2+2NO ΔH=+116.2 kJ·mol-1 (反应热) 6.实验时研究化学的基础,图中所示的实验操作正确的是:实验时研究化学的基础,图中 所示的实验操作正确的是: A.装置①:干燥CO2 B.装置②:实验室制取并收集O2 C.装置③:装置气密性的检查 D.装置④:吸收NH3 7.某有机物分子式为C4H8,据此推测其结构和性质不可能的是 A.它与乙烯可能是同系物 B.一氯代物可能只有一种 C.分子结构中甲基的数目可能是0、1、2 D.等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8 8.已知水的电离方程式:H2O H+ + OH-。下列叙述中,正确的是: A.升高温度,KW增大,pH不变 B.向水中加入少量硫酸,c(H+)增大,KW不变 C.向水中加入氨水,平衡向逆反应方向移动,c (OH-)降低 D.向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低 9. 某无色溶液中由水电离产生的C(H+)和C(OH-)的乘积为1×10-18( 25℃),下列离子组在此溶液中能大量共存的是: A.MnO4- Cl- K+ Na+ B.CO32- NO3- Cu2+ Na+ C.SO42- HCO3- K+ Na+ D.SO42- NO3- K+ Na+ 10.关于CaCO3沉淀的溶解平衡说法正确的是 A.CaCO3沉淀生成和沉淀溶解不断进行,但速率相等 B.CaCO3难溶于水,溶液中没有Ca2+和CO32- C. 升高温度,CaCO3沉淀的溶解度无影响 D. 向CaCO3沉淀中加入Na2CO3固体,CaCO3沉淀的溶解度不变 11.下列有机物的系统命名中正确的是: A. 3-甲基-4-乙基戊烷 B. 3,3,4-三甲基己烷 C. 3,4,4-三甲基己烷 D. 3,5-二甲基己烷 12. 某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法不正确的是: A. 若溶液中c(A-)=c(Na+),则溶液一定呈中性 B. 溶液中不可能存在:c(Na+)>c(A-)>c(H+)>[c(OH-) C. 若c(OH-)>c(H+),溶液中可能存在:c(Na+)>c(OH-)>c(A-)>c(H+) D. 若溶质为NaA、HA,则不可能存在:c(A-)>c(Na+)>c(H+)>c(OH-) 13. 化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是 A.惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl- -2e- = Cl2 ↑ B.氢氧燃料电池(酸性电解质)的正极反应式:O2 + 2H2O + 4e-=4OH- C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu -2e- = Cu2+ D.钢铁发生电化学腐蚀的正极反应式:Fe-2e- = Fe2+ 14.已知图一表示的是可逆反应C0(g)+H2(g) C(s)+H20(g) △H>O化学反应速率(V)与 时间(t)的关系,图二表示的是可逆反应2N02(g) N204(g) △H<O的浓度(c)随 时间(t)的变化情况。下列说法中正确的是 : A.图一t2时改变的条件是增大了反应物的浓度 B.图一t2时改变的条件可能是升高了温度或增大了压强 C.图二t1时改变的条件可能是升高了温度或增大了压强 D.若图二t1时改变的条件增大压强,则混合气体的平均相对分子质量将减小 15.空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是 A.c极上进行还原反应,B中的H+ 可以通过隔膜进入A B.d极上发生的电极反应是:O2+4H++4e一═2H2O C.该装置开始工作后,右端装置能量变化为:电能→化学能 D.当有0.2mol电子转移时,a极产生1.12L O2 16.已知:下表为25 ℃时某些弱酸的电离平衡常数。 CH3COOH HClO H2CO3 Ka=1.8×10-5 Ka=3.0×10-8 Ka1=4.4×10-7 Ka2=4.7×10-11 下图表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。下列说法正确的是: A.25℃时,相同浓度的NaHCO3溶液的碱性大于NaClO溶液 B.图像中a点的导电能力小于c点 C.图像I代表CH3COOH溶液的稀释 D.图像中a点酸的总浓度大于b点酸的总浓度 第Ⅱ卷 二、填空题:(本题含5小题,共52分) 17.(8分)海水是镁的主要来源之一。从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥;④电解得到产物。 (1)以上提取镁的全过程中,没有涉及的化学反应类型是 (填序号)。 A.分解反应 B.化合反应 C.置换反应 D.复分解反应 (2)下列关于提取镁的说法中不正确的是 (填序号)。 A.此法的优点之一是原料来自大海 B.进行①②③步骤的目的是富集MgCl2 C.可用电解熔融氧化镁的方法制取镁 D.电解冶炼镁要消耗大量电能 (3)电解熔融氯化镁制取镁的化学反应方程式 。 (4)③中沉淀物与盐酸反应的离子反应方程式 。 18.(10分) 现有25 ℃时0.1 mol/L的氨水。请回答以下问题: (1)若向氨水中加入少量硫酸铵固体,此时溶液中氢氧根离子浓度________(填“增大”“减小”或“不变”); (2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式________________; 所得溶液的pH________7(填“>”“<”或“=”),用离子方程式表示其原因_________________。 (3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol· L-1,则c(SO42-)=________; 19. (10分)分析、归纳、探究是学习化学的重要方法和手段之一。下面就电解质A回答有关问题(假定以下都是室温时的溶液)。 (1)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=a ①当a =10时,A溶液呈碱性的原因是(用离子方式程式表示) 。 ②当a =10,n =1时,A溶液中各种离子浓度由大到小的顺序为 , c(OH-)-c(HB)=________ mol/L。 ③当n=1、c=0.1,溶液中c(HB)∶c(B-)=1∶99时,A溶液的pH为______(保留整数值)。 (2)已知难溶电解质A的化学式为X2Y3,测得其饱和溶液中X3+离子的浓度为c mol/L ,则该 难溶物X2Y3的溶度积常数为Ksp=_______。 20.(6分) 以下是同学们在探讨金属及其化合物性质和应用时进行的探究实验: 士兵在野外加热食物时通常采用“无焰食物加热器”,其主要化学成分为镁粉、铁粉、氯化钠,使用时加入水与其中的镁反应放出热量。下面是在相同的室温下(约20℃)对该产品的两份实验: I.向加有等量水的隔热容器中分别加入下列各组物质,结果参见下图1。 ①1.0mol镁一整根、0.10mol铁粉、0.10mol氯化钠粉末; ②将1.0mol镁条剪成100份、 n1 mol铁粉、0.10mol氯化钠粉末; ③1.0mol镁粉、0.10mol铁粉、0.10mol氯化钠粉末; II.向加有100mL水的隔热容器中分别加入0.10mol镁粉、0.50mol铁粉及不同量的氯化钠 粉末,不断搅拌,第15min时记录温度升高的幅度参见下图2。 请回答下列问题: ⑴如果实验Ⅰ只验证了一种外因对镁与水反应速率的影响,则该因素是___________。 A.反应温度 B.NaCl的用量 C.铁的用量 D.镁的表面积 由此确定n1= ⑵实验Ⅱ中当NaCl的用量大于0.125mol时,实验就无须再做的原因是__________。 A.加入更多的NaCl不再增加反应速率 B.加入NaCl反而会降低反应速率 C.已达到沸点不再有温度变化 D.需要加入更多的铁粉来提高温度 ⑶如果在实验2中加入了0.060molNaCl,则第15min时混合物的温度最接近于______。 A.34℃ B.42℃ C.50℃ D.62℃ ⑷铁粉、NaCl能使反应速率增加的原因是______________________________________。 21.(8分)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白: (1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 。 (2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 。 A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液 B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 C.酸式滴定管在滴定前有气泡,滴定后气泡消失 D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 (3)若滴定开始和结束时,酸式滴定管中的液面如图所示,所用盐酸溶液的体积为 mL。 (4) 某学生根据三次实验分别记录有关数据如下表: 滴定 次数 待测氢氧化钠溶 液的体积/mL 0.1000mol·L+1盐酸的体积(mL) ziyuanku.com滴定前刻度 滴定后刻度 第一次 25.00 0.00 26.11 第二次 25.00 1.56 30.30 第三次 25.00 0.22 26.31 请选用数据列式计算该氢氧化钠溶液的物质的量浓度:C(NaOH)= (保留小数点后4位)。 22. (10分)科学家认为,氢气是一种高效而无污染的理想能源,近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展。 (1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是 。(选填字母) A.电解水 B.锌和稀硫酸反应 C.光解海水 D.分解天然气 (2)用水分解获得氢气的能量变化如图1所示,表示使用催化剂是曲线 .该反应为 (放热还是吸热)反应。 (3)1g的氢气完全燃烧生成液态水释放出142.9kJ的热量,写出其完全燃烧的热化学方程式: 。 (4) 氢氧燃料电池能量转化率高,具有广阔的发展前景.现用氢氧燃料电池进行图2所示实验: ①氢氧燃料电池中,正极的电极反应式为 。 ②图2装置中,某一铜电极的质量减轻6.4g,则a极上消耗的O2在标准状况下的体积为 L。查看更多