- 2021-07-08 发布 |
- 37.5 KB |
- 10页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
高一化学课件:1物质结构 元素周期律
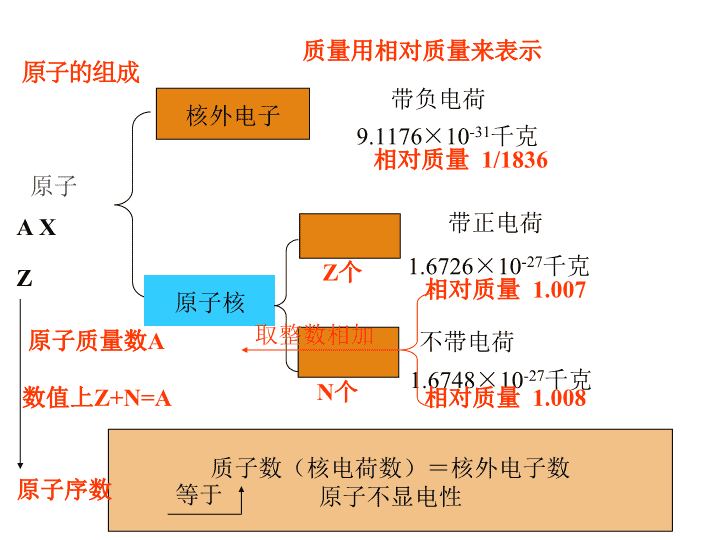
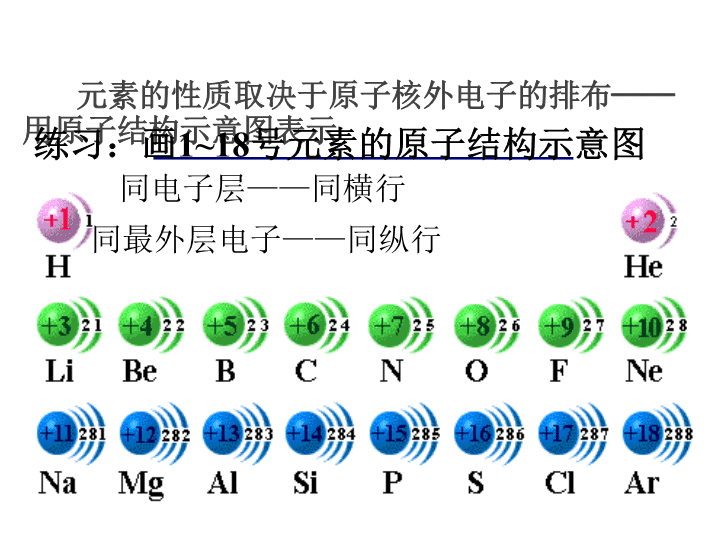
第一章 物质结构 元素周期律 原子的组成 原子 原子核 质子质子质子 中子中子中子 带负电荷 带正电荷 不带电荷 1.6748×10-27千克 1.6726×10-27千克 9.1176×10-31千克 质子数(核电荷数)=核外电子数 原子不显电性 核外电子 质量用相对质量来表示 相对质量 1/1836 相对质量 1.007 相对质量 1.008 Z个 N个 原子质量数A 数值上Z+N=A X Z A 取整数相加 原子序数 等于 元素的性质取决于原子核外电子的排布—— 用原子结构示意图表示练习:画1~18号元素的原子结构示意图 同电子层——同横行 同最外层电子——同纵行 1、按照原子序数递增的顺序从左到右排列将电子层数相 同的元素排成一个横行 2、把最外层电子数相同的元素(个别例外)按电子层数递 增的顺序从上到下排成纵行 一、元素周期表 周期 族 周期表的编排原则 1、参照元素周期表,观察每一周期(横行)有哪些特 点?各周期元素分布如何?以前三周期为例,周期序数和 原子核外电子层数有什么样的关系? 讨论: 元素周期表共有7行7个周期,每一周期元 素个数并不一定相等,周期序数=原子核外电 子层数 2、与每一周期元素作对比,族(纵行)主要由哪几部 分构成?每一族元素分布有什么特点? 以主族为例, 主族序数和原子核最外层电子数有什么样的关系? 元素周期表共有18个纵行,共16个族,分别为7 主7副1零1VIII族。主族元素最外层电子数= 主族序数 3、观察元素周期表,周期序数和族序数的表示有什 么不同?“1…”“Ⅰ…”“A”“B”分别代表什么 意思?具体某元素,我们如何表示它在元素周期表中 的位置呢? 元素周期表中,周期用纯数字表示,族用 “Ⅰ~Ⅶ”和“A”和“B”表示。“A”代表主 族,“B”代表副族。如:“N”所在的位置为第 二周期第ⅤA族。 周 期 表 7个周期 7个主族:由短周期和长周期 元素共同构成的族(IA~VIIA) 7个副族:仅由长周期构成的族 (ⅠB~ⅦB) VIII族(3个纵行):Fe、Co、 Ni等9种元素 横的方面 (7个横行) 纵的方面 (18个纵行) 零族:稀有气体元素 1 2 3 4 5 6 7 2种元素 8种元素 8种元素 18种元素 18种元素 32种元素 26种元素 短周期 长周期 不完全周期 元素周期表结构 1.写出下列元素在周期表中的位置 Na Cl Fe 2.写出原子序数为16、55、88三种 元素在周期表中的位置 Na 第三周期第ⅠA族 Cl 第三周期第ⅦA族 Fe 第四周期第Ⅷ族 16 第三周期第ⅥA族 55 第六周期第ⅠA族 88 第七周期第ⅡA族 随堂练习: 1、具有真正意义上的元素周期表是有哪位化学家发现的 ( ) A.门捷列夫(俄国) B.纽兰兹(英国) C.迈尔(德国) D.尚古多(法国) 2、不能作为元素周期表中元素排列顺序的依据的是( ) A.原子的核电荷数 B.原子的核外电子数 C.原子的质子数 D.原子的中子数 3、请仔细观察元素周期表,你可以发现其中有_____个横 行,也就是有____个周期,短周期指 周期,长周期 周期。元素周期表有______个纵行,分为 ___个族,其中 ____个主族,___个副族,___个第Ⅷ族,____个0族,0族 即是 元素。由短周期和长周期共同构成的 族 。 A D 主族和零族 七 一二三 四五六七 十八 十六 七 七 一 一 稀有气体 七 布置作业 1、熟记1~20号元素顺序和符号 4、某元素的原子AZM,它的氯化物MCl 1.17g溶于水制成溶 液后, 加入1mol/L的AgNO3溶液20ml恰好完全反应。若这 种同位素原子核内有12个中子,求: (1)Z值和A值; (2)把X的单质在空气中燃烧,有何现象?写出反应的化 学方程式。 解: (1)设与AgNO3溶液反应消耗氯化物MCl的物质的量为n mol。则: MCl + AgNO3 = AgCl + MNO3 1 1 n mol 1mol/L X 20ml X10-3 1/n = 1/(1 X 20 X 10-3) n = 0.02(mol) M的摩尔质量= 1.17/0.02 – 35.5 = 23(g/mol) A=23 Z = A – N = 23 – 12 = 11 由此可以断定M为Na (2)剧烈燃烧,发出黄色火焰,有淡黄色固体产生; 2Na + O2 = Na2O2查看更多