- 2021-07-08 发布 |
- 37.5 KB |
- 48页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020届二轮复习物质结构元素周期律课件(48张)(广西专用)
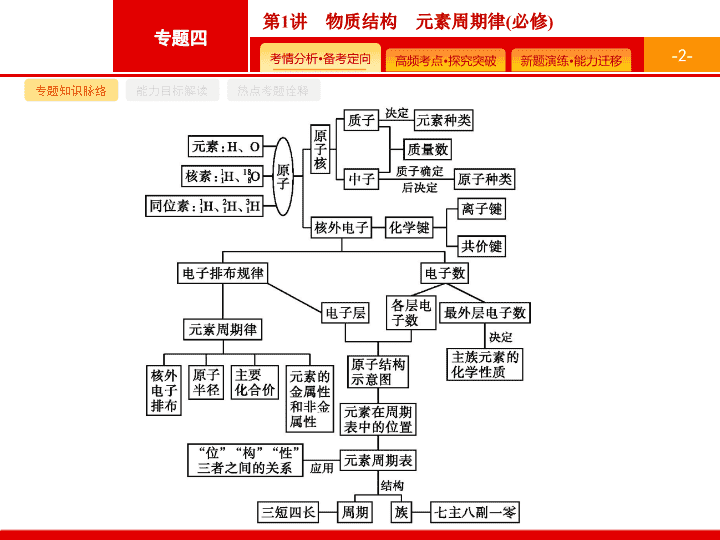
第 1 讲 物质结构 元素周期律 ( 必修 ) - 2 - 专题知识脉络 能力目标解读 热点考题诠释 - 3 - 专题知识脉络 能力目标解读 热点考题诠释 - 4 - 专题知识脉络 能力目标解读 热点考题诠释 1 .(2019 全国 Ⅰ ) 科学家合成出了一种新化合物 ( 如图所示 ), 其中 W 、 X 、 Y 、 Z 为同一短周期元素 ,Z 核外最外层电子数是 X 核外电子数的一半。下列叙述正确的是 ( ) A.WZ 的水溶液呈碱性 B. 元素非金属性的顺序为 X>Y>Z C.Y 的最高价氧化物的水化物是中强酸 D. 该新化合物中 Y 不满足 8 电子稳定结构 C 解题要领 由题给化合物的结构可知 ,W 为第 Ⅰ A 族金属元素 ;Z 最外层有 7 个电子 , 由 “Z 核外最外层电子数是 X 核外电子数的一半 ” 可知 ,X 核外电子数为 14, 即 X 为硅元素 ; 由四种元素为同一短周期元素可知 ,W 为钠元素 ;Z 为氯元素 ;Y 为磷元素。 NaCl 的水溶液呈中性 ,A 项错误 ; 元素非金属性的顺序为 Z(Cl)>Y (P)>X(Si),B 项错误 ;P 的最高价氧化物的水化物为磷酸 , 是中强酸 ,C 项正确 ;P 原子最外层有 5 个电子 , 与 Si 共用两对电子 , 加上得到 Na 的 1 个电子 , 因此最外层满足 8 电子稳定结构 ,D 项错误。 - 5 - 专题知识脉络 能力目标解读 热点考题诠释 2 .(2018 全国 Ⅰ ) 主族元素 W 、 X 、 Y 、 Z 的原子序数依次增加 , 且均不大于 20 。 W 、 X 、 Z 最外层电子数之和为 10;W 与 Y 同族 ;W 与 Z 形成的化合物可与浓硫酸反应 , 其生成物可腐蚀玻璃。下列说法正确的是 ( ) A. 常温常压下 X 的单质为气态 B.Z 的氢化物为离子化合物 C.Y 和 Z 形成的化合物的水溶液呈碱性 D.W 与 Y 具有相同的最高化合价 B 解题要领 根据 “W 与 Z 形成的化合物可与浓硫酸反应 , 其生成物可腐蚀玻璃 ” 可知 , 该生成物为 HF, 则结合 “W 与 Y 同族 ” 及 “W 、 X 、 Z 最外层电子数之和为 10” 可推知 ,W 为氟元素 ,X 为钠元素 ,Y 为氯元素 ,Z 为钙元素。常温常压下 , 金属钠为固态 ,A 项错误 ;CaH 2 为离子化合物 ,B 项正确 ;CaCl 2 为强酸强碱盐 , 其溶液呈中性 ,C 项错误 ;F 无正价 , 而 Cl 的最高价为 +7 价 ,D 项错误。 - 6 - 专题知识脉络 能力目标解读 热点考题诠释 3 .(2017 全国 Ⅰ ) 短周期主族元素 W 、 X 、 Y 、 Z 的原子序数依次增大 ,W 的简单氢化物可用作制冷剂 ,Y 的原子半径是所有短周期主族元素中最大的。由 X 、 Y 和 Z 三种元素形成的一种盐溶于水后 , 加入稀盐酸 , 有黄色沉淀析出 , 同时有刺激性气体产生。下列说法不正确的是 ( ) A.X 的简单氢化物的热稳定性比 W 的强 B.Y 的简单离子与 X 的具有相同的电子层结构 C.Y 与 Z 形成化合物的水溶液可使蓝色石蕊试纸变红 D.Z 与 X 属于同一主族 , 与 Y 属于同一周期 C 解题要领 W 的简单氢化物可用作制冷剂 , 可知 W 为 N;Y 的原子半径是短周期主族元素中半径最大的 , 可知 Y 为 Na;X 、 Y 和 Z 组成的盐溶于水后 , 加入稀盐酸有黄色沉淀和刺激性气味的气体产生 , 可知此盐为 Na 2 S 2 O 3 , 即 X 为 O,Z 为 S 。 O 的非金属性比 N 的强 , 则 H 2 O 的热稳定性比 NH 3 的强 , 故 A 项正确 ;Na + 与 O 2- 的电子层结构相同 ,B 项正确 ;Na 2 S 的水溶液因水解呈碱性 , 故 C 项错误 ;S 与 O 同主族 , 与 Na 同周期 ,D 项正确。 - 7 - 专题知识脉络 能力目标解读 热点考题诠释 4 .(2017 全国 Ⅱ )a 、 b 、 c 、 d 为原子序数依次增大的短周期主族元素 ,a 原子核外电子总数与 b 原子次外层的电子数相同 ;c 所在周期序数与族序数相同 ;d 与 a 同族。下列叙述正确的是 ( ) A. 原子半径 :d>c>b>a B.4 种元素中 b 的金属性最强 C.c 的氧化物的水化物是强碱 D.d 单质的氧化性比 a 单质的氧化性强 B 解题要领 由于都是主族元素 , 故 a 原子核外电子总数只能是 8,a 为氧元素 ;a 、 b 、 c 、 d 为短周期元素 , 原子序数依次增大 ,c 所在周期序数与族序数相同 ,c 为 Al, 则 b 为 Na 或 Mg 元素 ;d 与 a 同族 , 则 d 为硫元素。 A 项 , 同周期元素 , 从左到右原子半径逐渐减小 , 电子层数越多 , 原子半径越大 , 故原子半径 :Na( 或 Mg)>Al>S>O,A 项错误 ;4 种元素中 Na( 或 Mg) 的金属性最强 ,B 项正确 ; 铝的氧化物对应的水化物是两性氢氧化物 ,C 项错误 ;D 项 ,S 的氧化性弱于 O 2 ,D 项错误。 - 8 - 命题热点一 命题热点二 命题热点三 原子结构、原子核外电子排布规律 有关原子结构解题的思维路径 - 9 - 命题热点一 命题热点二 命题热点三 问题探究 1 . 原子结构和原子核外电子排布有哪些重要规律 ? (1) 构成原子或离子的微粒间的数量关系。 ① 如在 中 : 质量数 ( A ) = 质子数 ( Z ) + 中子数 ( N ) ② 核电荷数 = 质子数 = 原子的核外电子数 ③ 阳离子 (M n + ): 核电荷数 = 质子数 = 离子核外电子数 + 电荷数 ( n ) ④ 阴离子 (R n - ): 核电荷数 = 质子数 = 离子核外电子数 - 电荷数 ( n ) (2) 原子核外电子排布规律。 ① 各层容纳的电子数最多为 2 n 2 个 ( n 表示电子层数 ); ② 最外层电子数最多为 8 个 ; ③ 电子总是尽可能由内层排起 , 逐步往外层排 , 能量逐渐增大。 - 10 - 命题热点一 命题热点二 命题热点三 2 . 短周期元素原子结构有哪些特点 ? (1) 最外层电子数是次外层电子数 2 倍的原子是 C;3 倍的是 O;4 倍的是 Ne; 最外层电子数是次外层电子数 的是 Li 、 Si 。 (2) 最外层电子数与电子层数相等的原子有 H 、 Be 、 Al; 最外层电子数是电子层数 2 倍的原子是 He 、 C 、 S;3 倍的是 O 。 (3) 最外层电子数不是 8 的短周期元素的简单离子有 Li + 、 H + 、 H - 等。 (4) 气态密度最小 , 原子半径最小 , 原子核中只有质子没有中子 , 原子序数、电子层数、最外层电子数三者均相等的是 H 。 - 11 - 命题热点一 命题热点二 命题热点三 例 1 微粒中所含有的相关微粒数存在一定的代数关系。下列有关叙述正确的是 ( ) - 12 - 命题热点一 命题热点二 命题热点三 分析推理 (1) 如何理解同位素 ? 同位素是指质子数相同 , 中子数不同的同一元素的不同原子 , 互为同位素的原子中子数不同 , 质量数也不同。如 , 其质量数之和为 22, 而质子数之和为 10, 质量数之和不是质子数之和的两倍。 (2) 同种元素的原子和离子之间的结构特征关系如何 ? 同种元素的原子和离子 , 无论它们的中子数是否相同 , 它们的核电荷数一定相同 , 核外电子数一定不同。 (3) 如何确定核外电子总数相同的简单阴离子和阳离子之间的等量关系 ? b X n - 和 a Y m + 两种离子 , 当它们核外电子总数相同时 , 有 a-m=b+n , 即 a=b+m+n 。 答案 D - 13 - 命题热点一 命题热点二 命题热点三 题后反思 1 . 不是所有原子核都由质子和中子组成 , 如 无中子。 2 . 地壳中含量最高的非金属是 O 不是 N 。 3 . 任何微粒中 , 质量数 = 质子数 + 中子数 , 但质子数与电子数不一定相等。 4 . 质子数相同的微粒不一定属于同一种元素 , 如 Ne 和 H 2 O 。 5 . 因许多元素存在同位素 , 故原子的种类多于元素的种类 , 有多少种核素就有多少种原子。并非所有元素都有同位素 , 如 Na 、 F 、 Al 等就没有同位素。 6 . 互为同位素的原子中子数不同 , 质子数相同 , 化学性质几乎完全相同 , 物理性质差异较大。 - 14 - 命题热点一 命题热点二 命题热点三 对点训练 1 (2017 北京高考 )2016 年 IUPAC 命名 117 号元素为 Ts( 中文名 “ ”, tián ),Ts 的原子核外最外层电子数是 7 。下列说法不正确的是 ( ) A.Ts 是第七周期第 ⅦA 族元素 B.Ts 的同位素原子具有相同的电子数 C.Ts 在同族元素中非金属性最弱 D. 中子数为 176 的 Ts 核素符号是 D - 15 - 命题热点一 命题热点二 命题热点三 “ 位 ”“ 构 ”“ 性 ” 的关系及应用 有关 “ 位 ”“ 构 ”“ 性 ” 题目解题思维路径 - 16 - 命题热点一 命题热点二 命题热点三 - 17 - 命题热点一 命题热点二 命题热点三 - 18 - 命题热点一 命题热点二 命题热点三 问题探究 1 . 原子结构与位置、性质的关系包括哪些内容 ? - 19 - 命题热点一 命题热点二 命题热点三 - 20 - 命题热点一 命题热点二 命题热点三 2 . 如何比较元素的金属性和非金属性强弱 ? - 21 - 命题热点一 命题热点二 命题热点三 - 22 - 命题热点一 命题热点二 命题热点三 例 2 短周期元素 X 、 Y 、 Z 、 W 的原子序数依次增大 , 其中 Y 、 Z 原子的核外电子数之和与 X 、 W 原子的核外电子数之和相等 ,Z 单质可以用来冶炼其他熔点较高的金属 ,X 和 W 间可形成一种能产生酸雨的化合物 , 则下列说法不正确的是 ( ) A. 原子半径从大到小顺序为 W>Z>Y>X B.X 与 Y 可形成既含离子键又含非极性共价键的化合物 C.X 、 W 分别形成的简单氢化物中 , 后者还原性强 D.X 形成单核阴离子的核外电子数与 Y 、 Z 、 W 原子的核外内层电子数相同 - 23 - 命题热点一 命题热点二 命题热点三 分析推理 (1) 铝热反应有何作用 ? 哪些物质可形成酸雨 ? 铝热反应主要是用来冶炼高熔点的金属。形成酸雨的物质包括氮氧化物、硫氧化物。所以 Z 为 Al; 结合原子序数依次增大可知 W 为 S 、 X 为 O 。 (2)Y 的核外电子数 =24-13=11, 为 Na 。 (3) 怎样比较原子半径或离子半径 ? 原子半径应用元素周期表进行比较 , 首先把 X 、 Y 、 Z 、 W 放在元素周期表中大致位置 , 可知 Y 的原子半径最大 ,A 选项错误 ; 离子半径大小比较 , 应用 “ 同层比核 ”, 具有相同电子层结构的离子 , 核电荷数越大 , 离子半径越小 , 如 r (Al 3+ )< r (Na + )< r (F - )< r (O 2- ) 。 (4) 其他选项 , 可采取具体举例法分析 —— 由 Na 2 O 2 可知 B 项正确 ;H 2 S 的还原性强于 H 2 O 的 ,C 选项正确 ;O 2- 的核外电子数为 10,Na 、 Al 、 S 的内层电子数之和均为 10,D 选项正确。 答案 A - 24 - 命题热点一 命题热点二 命题热点三 题后反思 解答元素 “ 位 ”“ 构 ”“ 性 ” 关系的 “ 六大误区 ” - 25 - 命题热点一 命题热点二 命题热点三 对点训练 2 1 .a 、 b 、 c 、 d 为短周期元素 ,a 的原子中只有 1 个电子 ,b 2- 和 c + 离子的电子层结构相同 ,d 与 b 同族。下列叙述错误的是 ( ) A.a 与其他三种元素形成的二元化合物中其化合价均为 +1 价 B.b 与其他三种元素均可形成至少两种二元化合物 C.c 的原子半径是这些元素中最大的 D.d 与 a 形成的化合物的溶液呈弱酸性 A 解析 根据 a 的原子中只有 1 个电子 , 可知 a 为氢元素 , 依据 b 2- 和 c + 离子的电子层结构相同 , 且元素都为短周期元素 , 可知 b 为氧元素 ,c 为钠元素 , 最后根据 d 与 b 同族且为短周期元素可知 d 为硫元素。 NaH 中 H 为 -1 价 ,A 项错误 ; 由 H 2 O 、 H 2 O 2 、 Na 2 O 、 Na 2 O 2 、 SO 2 、 SO 3 等物质可知 B 项正确 ; 原子半径由大到小的顺序为 Na>S>O>H,C 项正确 ;H 2 S 的水溶液呈弱酸性 ,D 项正确。 - 26 - 命题热点一 命题热点二 命题热点三 2 .(2018 天津理综 ) 下列有关物质性质的比较 , 结论正确的是 ( ) A. 溶解度 :Na 2 CO 3查看更多