- 2021-07-08 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018届高考一轮复习人教版第3节考点1晶体和晶胞学案3
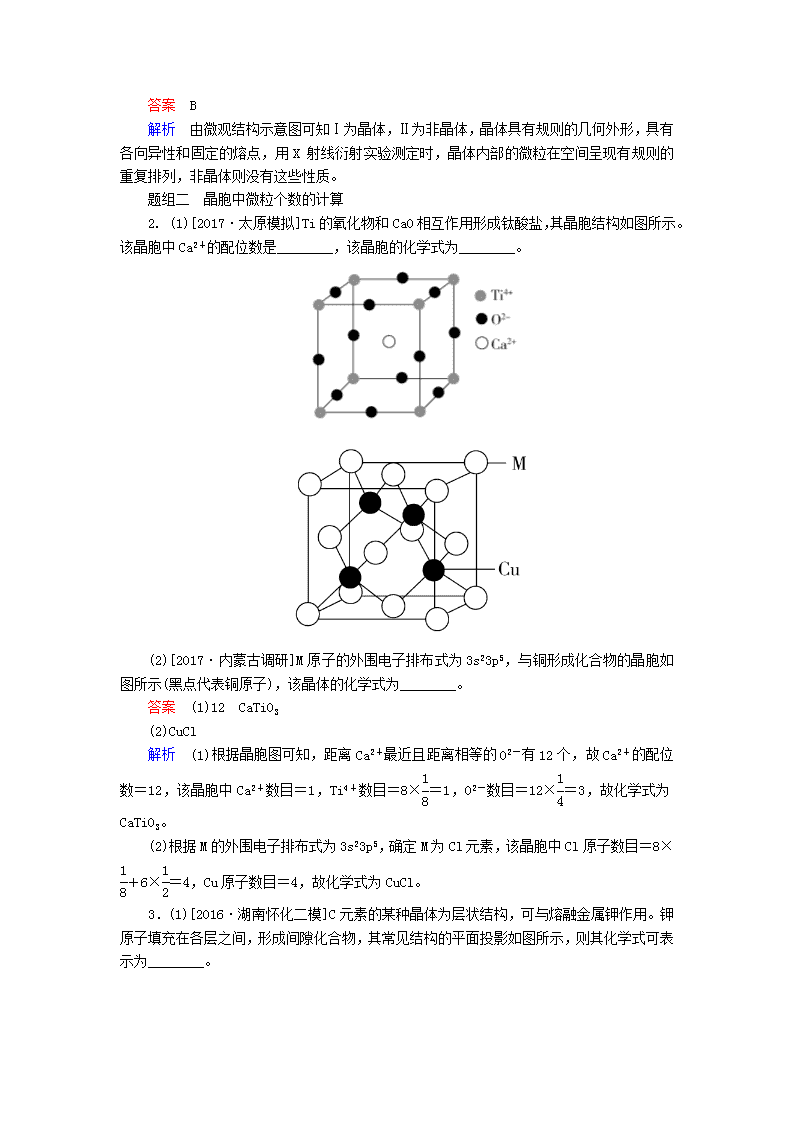
第3节 晶体结构与性质 明考纲 1.理解离子键的形成,能根据离子化合物的结构特征解释其物理性质。 2.了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系。 3.理解金属键的含义,能用金属键理论解释金属的一些物理性质,了解金属晶体常见的堆积方式。 4.了解分子晶体与原子晶体、离子晶体、金属晶体的构成微粒、微粒间作用力的区别。 5.能根据晶胞确定晶体的组成并进行相关的计算。 6.了解晶格能的概念及其离子晶体的性质。 析考情 本节是选修3的重要组成部分,在高考中占有极其重要的地位。高考在本节中的考点是:①晶体常识;②分子晶体与原子晶体;③金属晶体;④离子晶体。它是原子结构和化学键知识的延伸提高,其中对四大晶体做了阐述,结合数学立体几何的知识,充分认识和挖掘典型晶胞的结构,形象、直观地认识四种晶体,每年高考必考。 考点1 晶体和晶胞 1.晶体与非晶体 2.获得晶体的三条途径 (1)熔融态物质凝固。 (2)气态物质冷却不经液态直接凝固(凝华)。 (3)溶质从溶液中析出。 3.晶胞 (1)概念:描述晶体结构的基本单元。 (2)晶体与晶胞的关系:数量巨大的晶胞“无隙并置”构成晶体。 (3)晶胞中粒子数目的计算——均摊法:如某个粒子为n个晶胞所共有,则该粒子有属于这个晶胞。 易错警示 (1)具有规则几何外形的固体不一定是晶体,如玻璃。 (2)晶体与非晶体的本质区别:是否有自范性。 (3)晶胞是从晶体中“截取”出来具有代表性的“平行六面体”,但不一定是最小的“平行六面体”。 (4)区分晶体和非晶体最科学的方法是对固体进行X射线衍射实验。 判断正误,正确的画“√”,错误的画“×”。 (1)具有规则几何外形的固体一定是晶体。(×) (2)晶体内部的微粒按一定规律周期性的排列。(√) (3)区分晶体和非晶体最可靠的方法是测定其有无固定熔沸点。(×) (4)通过X射线衍射实验的方法可以区分晶体和非晶体。(√) (5)立方晶胞中,顶点上的原子被4个晶胞共用。(×) (6)缺角的NaCl晶体在饱和NaCl溶液中会慢慢变为完美的立方体块。(√) 题组一 晶体与非晶体的区别 1.如图是物质的微观结构示意图,请认真观察两图,判断下列说法正确的是( ) A.两种物质在一定条件下都会自动形成有规则几何外形的晶体 B.Ⅰ形成的固体物理性质有各向异性 C.Ⅱ形成的固体一定有固定的熔、沸点 D.二者的X射线衍射图谱是相同的 答案 B 解析 由微观结构示意图可知Ⅰ为晶体,Ⅱ为非晶体,晶体具有规则的几何外形,具有各向异性和固定的熔点,用X射线衍射实验测定时,晶体内部的微粒在空间呈现有规则的重复排列,非晶体则没有这些性质。 题组二 晶胞中微粒个数的计算 2. (1)[2017·太原模拟]Ti的氧化物和CaO相互作用形成钛酸盐,其晶胞结构如图所示。该晶胞中Ca2+的配位数是________,该晶胞的化学式为________。 (2)[2017·内蒙古调研]M原子的外围电子排布式为3s23p5,与铜形成化合物的晶胞如图所示(黑点代表铜原子),该晶体的化学式为________。 答案 (1)12 CaTiO3 (2)CuCl 解析 (1)根据晶胞图可知,距离Ca2+最近且距离相等的O2-有12个,故Ca2+的配位数=12,该晶胞中Ca2+数目=1,Ti4+数目=8×=1,O2-数目=12×=3,故化学式为CaTiO3。 (2)根据M的外围电子排布式为3s23p5,确定M为Cl元素,该晶胞中Cl原子数目=8×+6×=4,Cu原子数目=4,故化学式为CuCl。 3.(1)[2016·湖南怀化二模]C元素的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图所示,则其化学式可表示为________。 (2)[2016·四川绵阳模拟]Al的单质为面心立方最密堆积(如图),则一个晶胞中Al原子数目为________。 答案 (1)KC8 (2)4 解析 (1)由图可知,1个K原子周围直接相邻的C原子有6个,不直接相邻的有6个,并且被3个K原子共用,所以1个K原子对应8个C原子,化学式为KC8。 (2)Al原子位于晶胞的顶点和面心处,依据均摊法,一个晶胞中Al原子数=+=4个。 总结提升 晶胞计算的思维方法 1.原则 晶胞任意位置上的一个粒子如果是被n个晶胞所共有,那么,每个晶胞对这个粒子分得的份额就是。 2.方法 (1)长方体(包括立方体)晶胞中不同位置的粒子数的计算 (2)非长方体晶胞中粒子视具体情况而定,如石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳原子)被三个六边形共有,每个六边形占1/3。 注意:(1)在使用均摊法计算晶胞中微粒个数时,要注意晶胞的形状,不同形状的晶胞,应先分析任意位置上的一个粒子被几个晶胞所共有。如六棱柱晶胞中,顶点、侧棱、底面上的棱、面心依次被6、3、4、2个晶胞所共有。 (2)在计算晶胞中粒子个数的过程中,不是任何晶胞都可用均摊法。 题组三 晶体的密度及微粒间距离的计算 4.(1)[2017·西安检测]铜是第四周期最重要的过渡元素之一,已知CuH晶体结构单元如图所示。该化合物的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则该晶胞中Cu原子与H原子之间的最短距离为________cm(用含ρ和NA的式子表示)。 (2)[2017·广州检测]CuFeS2的晶胞如图所示,晶胞参数a=0.524 nm,b=0.524 nm,c=1.032 nm;CuFeS2的晶胞中每个Cu原子与________个S原子相连,列式计算晶体密度ρ=__________________________________________________________。 (3)[2017·陕西质检]NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488 pm,Na+半径为102 pm,H-的半径为______,NaH的理论密度是______ g·cm-3。 答案 (1)× (2)4 =4.31 g·cm-3 (3)142 pm 1.37 解析 (1)CuH晶胞中有Cu原子数目=8×+6×=4,含有H原子数目=4,则晶胞的边长= cm,则Cu原子与H原子之间的最短距离=× cm。 (2)根据晶胞图可知,每个Cu原子与4个S原子相连,该晶胞中含有Cu原子数目=8×+4×+1=4,含有Fe原子数目=4×+6×=4,含有S原子数目=8个,故化学式为CuFeS2,该晶体密度 ρ= ==4.31 g·cm-3。 (3)由NaCl晶胞可知,NaH晶胞中Na+位于棱上和体心,H-位于顶点和面心,故NaH晶胞的边长相当于H-的直径和Na+的直径之和,故H-的半径为=142 pm。NaH晶胞中含有4个Na+和4个H-,则该晶体的密度为 g÷(488×10-10 cm)3=1.37 g·cm-3。 总结提升 晶胞各物理量的计算 对于立方晶胞,可简化成下面的公式进行各物理量的计算:a3×ρ×NA=n×M,a表示晶胞的棱长,ρ表示密度,NA表示阿伏加德罗常数的值,n表示1 mol晶胞中所含晶体的物质的量,M表示晶体的摩尔质量。 (1)计算晶体密度的方法 (2)计算晶体中微粒间距离的方法查看更多