- 2021-07-08 发布 |
- 37.5 KB |
- 10页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
【化学】陕西省西安中学2020届高三第六次模拟考试
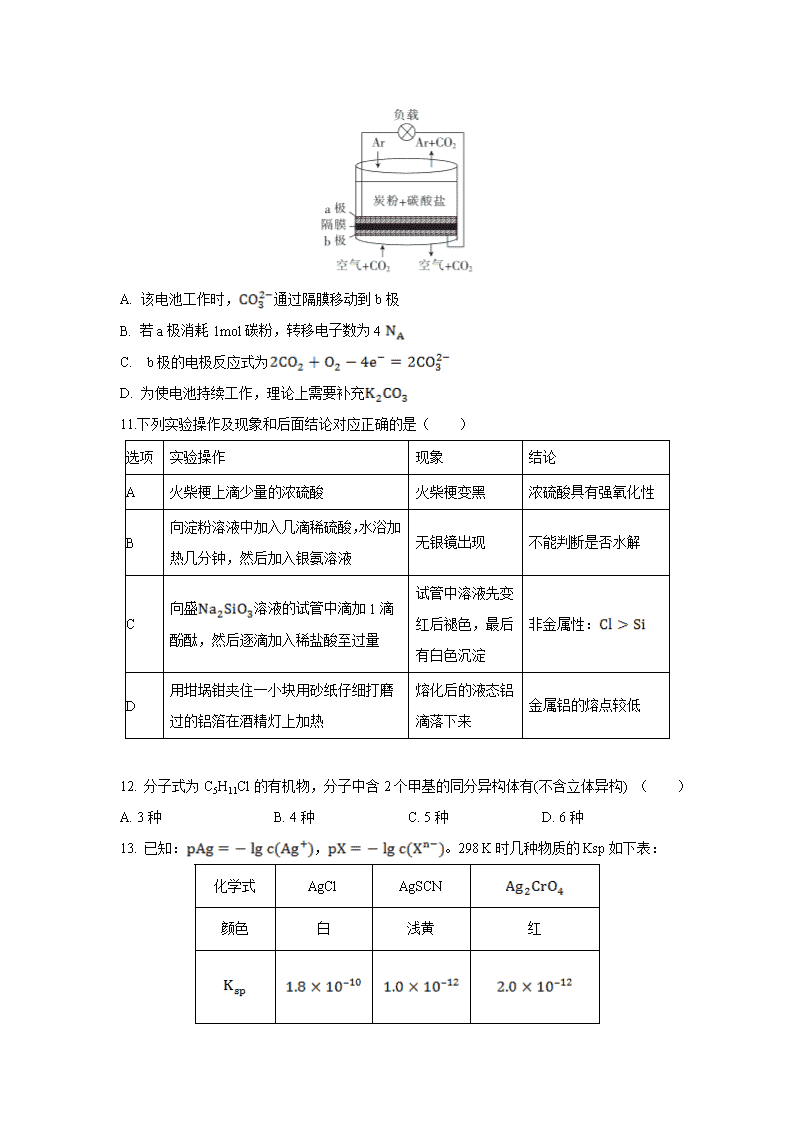
陕西省西安中学2020届高三第六次模拟考试 可能用到的相对相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Cu-64 Ba-137 Ni-59 Sr-88 一、选择题(本题共7小题,每小题6分。在每小题给出的四个选项中,只有一项是符合题目要求的) 7. 2020年5月新修订的《北京市生活垃圾管理条例》将正式实施,垃圾分类并回收利用,可以减少污染,保护环境,节约自然资源,而环境保护与化学知识息息相关,下列有关说法正确的是( ) A. 废旧电池中含有镍、镉等重金属,不可用填埋法处理,属于有害垃圾 B. 各种玻璃制品的主要成分是硅酸盐,不可回收利用,属于其他(干)垃圾 C. 废弃的聚乙烯塑料属于可回收垃圾,不易降解,能使溴水褪色 D. 含棉、麻、丝、毛及合成纤维的废旧衣物燃烧处理时都只生成和 8. 用表示阿伏加德罗常数的值,下列叙述正确的是( ) A. 28 g乙烯和丙烯中的极性键数目为4 B. 1.0 mol CH4与Cl2在光照下反应生成CH3Cl分子数为1.0 C. 1 mol氖气中含有的原子总数为2 D. 溶液中的数目为 9. 化合物X是一种医药中间体,其结构简式如图所示。下列有关化合物X的说法正确的是( ) A. 分子中两个苯环一定处于同一平面 B. 不能与饱和溶液反应 C. 在酸性条件下水解,水解产物只有一种 D. 化合物X不能发生氧化反应 10. 以熔融的碳酸盐为电解液,泡沫镍为电极,氧化纤维布为隔膜(仅允许阴离子通过)可构成直接碳燃料电池,其结构如图所示,下列说法正确的是( ) A. 该电池工作时,通过隔膜移动到b极 B. 若a极消耗1mol碳粉,转移电子数为4 C. b极的电极反应式为 D. 为使电池持续工作,理论上需要补充 11.下列实验操作及现象和后面结论对应正确的是( ) 选项 实验操作 现象 结论 A 火柴梗上滴少量的浓硫酸 火柴梗变黑 浓硫酸具有强氧化性 B 向淀粉溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入银氨溶液 无银镜出现 不能判断是否水解 C 向盛溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至过量 试管中溶液先变红后褪色,最后有白色沉淀 非金属性: D 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 熔化后的液态铝滴落下来 金属铝的熔点较低 12. 分子式为C5H11Cl的有机物,分子中含2个甲基的同分异构体有(不含立体异构) ( ) A. 3种 B. 4种 C. 5种 D. 6种 13. 已知:,。298 K时几种物质的Ksp如下表: 化学式 AgCl AgSCN 颜色 白 浅黄 红 AgCl、AgSCN、Ag2CrO4 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是( ) A. 图中x代表AgCl曲线,z代表AgSCN曲线 B. 298K时,在和的物质的量浓度均为的溶液中,滴入少量 的溶液,首先产生的是红色沉淀 C. 298 K时若增大p点的阴离子浓度,则y上的点沿曲线向上移动 D. 298 K时的平衡常数 二、非选择题:包括必考题和选考题两部分。第26题~28题为必考题,每个试题考生都必须做答。第35题~36题为选考题,考生根据要求作答。 (一)必考题 26.(14分) 锶为第五周期IIA族元素,其化合物六水氯化锶是实验室重要的分析试剂,工业上常以天青石主要成分为SrSO为原料制备,生产流程如下: 已知:经盐酸浸取后的溶液中除含有Sr和Cl外,还有少量的Ba杂质。 的溶度积常数为,SrSO的溶度积常数为。 O的摩尔质量为。 工业上天青石焙烧前应先研磨粉碎,其目的是__________________________。 工业上天青石隔绝空气高温焙烧时,若中只有S元素被还原,且转移了电子。则该反应的化学方程式为____________________________。 浸取后加入硫酸的目的是用离子方程式表示______________________________。为了提高原料的利用率,滤液中Sr的浓度应不高于_____________ 注:此时滤液中Ba浓度为。 产品纯度检测:称取产品溶解于适量水中,向其中加入含AgNO 的AgNO溶液溶液中除Cl外,不含其它与Ag反应的离子,待Cl完全沉淀后,滴入滴含Fe的溶液作指示剂,用 的NHSCN标准溶液滴定剩余的AgNO,使剩余的Ag以AgSCN白色沉淀的形式析出。已知:SCN先与Ag反应。 滴定反应达到终点的现象是_________________________________________。 若滴定过程用去上述浓度的NHSCN溶液,则产品中SrClO的质量百分含量为______________保留3位有效数字。 由晶体制取无水氯化锶的主要仪器除了酒精灯、泥三角、三脚架外,还有___________________。 27.(15分)甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。 Ⅰ、用生产甲醇 已知:的燃烧热为,的燃烧热为, 则 ________。 将和按物质的量之比充入体积为的恒容密闭容器中反应, 如图1两条曲线分别表示压强为和下转化率随温度的变化关系。 其中a点的平衡常数表达式为:________________。 ,b两点化学反应速率分别用、表示,则______填“大于”、“小于”或“等于”。 在恒容密闭容器中投入和发生反应: ,实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是______。 A.该反应的正反应为放热反应 B.压强大小关系为 C.M点对应的平衡常数K的值约为 D. 在及时,图中N点正逆 Ⅱ用CO生产甲醇 已知:,如图3是该反应在不同温度下CO的转化率随时间变化的曲线。 该反应的焓变______填“”、“”或“”。 和温度下的平衡常数大小关系是______填“”、“”或“”。 Ⅲ甲醇的应用 甲醇制氢气。甲醇水蒸气重整制氢反应: 。某温度下,将 的原料气充入恒容密闭容器中,初始压强为,反应达到平衡时总压强为,则平衡时甲醇的转化率为__________________。 以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图4所示。阳极的电极反应式为_____________________。 28. (14分)镍的全球消费量仅次于铜、铝、铅、锌,居有色金属第五位,常用于各种高光泽装饰漆和塑料生产,也用作催化剂,制取原理:,实验室用如图所示装置制取 。 已知:黑色;熔点,沸点 ,以上与空气混合易爆炸;熔点,沸点 。 回答下列问题: 装置A中发生反应的化学方程式为_______________________________________。 装置 C用于合成 夹持装置略,最适宜选用的装置为_____填标号。 实验过程中为了防止____________,必须先观察______________________________。 制得的 中常溶有 等杂质,提纯的方法是______填标号。 A.分液 B.蒸馏 C.过滤 D.重结晶 利用“封管实验”原理可获得高纯镍。如图所示的石英玻璃封管中充有 CO气体,则高纯镍粉在封管的______温度区域端生成填“323K”或“473K”。 实验中加入 ,C装置质量减轻 设杂质不参加反应,E装置中盛有 溶液100mL,则 溶液的物质的量浓度至少为______填实验现象再加热 C装置。 (二)选考题 35.[化学——物质结构与性质](15分) 黄铜是人类最早使用的合金之一,主要由锌和铜组成。回答下列问题: 铜原子核外电子共有______种不同运动状态,基态铜原子的核外占据最高能层电子的电子云轮廓图形状为_____________。 根据铜、锌原子结构可知第二电离能_____填“大于”或“小于”。 向蓝色硫酸铜溶液中加入稍过量的氨水,溶液变为深蓝色。 分子中心原子的杂化类型为______;分子中的键角:____填“大于”或“小于”。 通过上述实验现象可知,与的配位能力:_____填“大于”或“小于”。 氨硼烷可以作为机动车使用的备选氢来源或氢储存的材料。 下列与氨硼烷是等电子体的有______填编号 A.乙烷 写出的结构式结构中若含配位键用表示___________。 某磷青铜晶胞结构如图所示。 其化学式为___________。 若晶体密度为,最近的Cu原子核间距为______用表示阿伏加德罗常数,用M表示该晶体的摩尔质量。 36.[化学——有机化学基础](15分)化合物H是一种高效除草剂,其合成路线流程图如下: B的分子式为________; 中含氧官能团名称为 和 。 的反应类型为 。 写出同时满足下列条件的D的一种同分异构体的结构简式: 。 不能发生水解反应,能与溶液发生显色反应 分子中有4种不同化学环境的氢。 的分子式为,写出F的结构简式: 。 已知:与苯环相连时,易被氧化;与苯环相连时,再引入其他基团主要进入它的间位。 请写出以A和D为原料制备的合成路线流程图 。 无机试剂任用,合成路线流程图示例见本题题干 【参考答案】 7.A 8.A 9.C 10.B 11.B 12.B 13.D 26.(14分,每空2分) 增加反应物的接触面积,提高化学反应速率; ;; 当加入最后1滴溶液时,溶液由无色变为红色,且30s内不褪色; ; 坩埚。 27.(15分,除标注外每空2分) (1分)大于 28.(14分,每空2分) ; CO及与装置中空气混合在加热条件下会发生爆炸; E装置中生成黑色沉淀 B 473K 35.(15分,除标注外每空2分) ;(1分)球形;(1分)小于;(1分) ;小于;小于;;(1分); ;(1分)。 36.(15分,除标注外每空2分) C7H7NO2 ) 醚键;羧基 取代反应/硝化 或 或 (3分)查看更多