- 2021-07-07 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
【化学】湖南省娄底市2019-2020学年高一下学期期末考试试卷
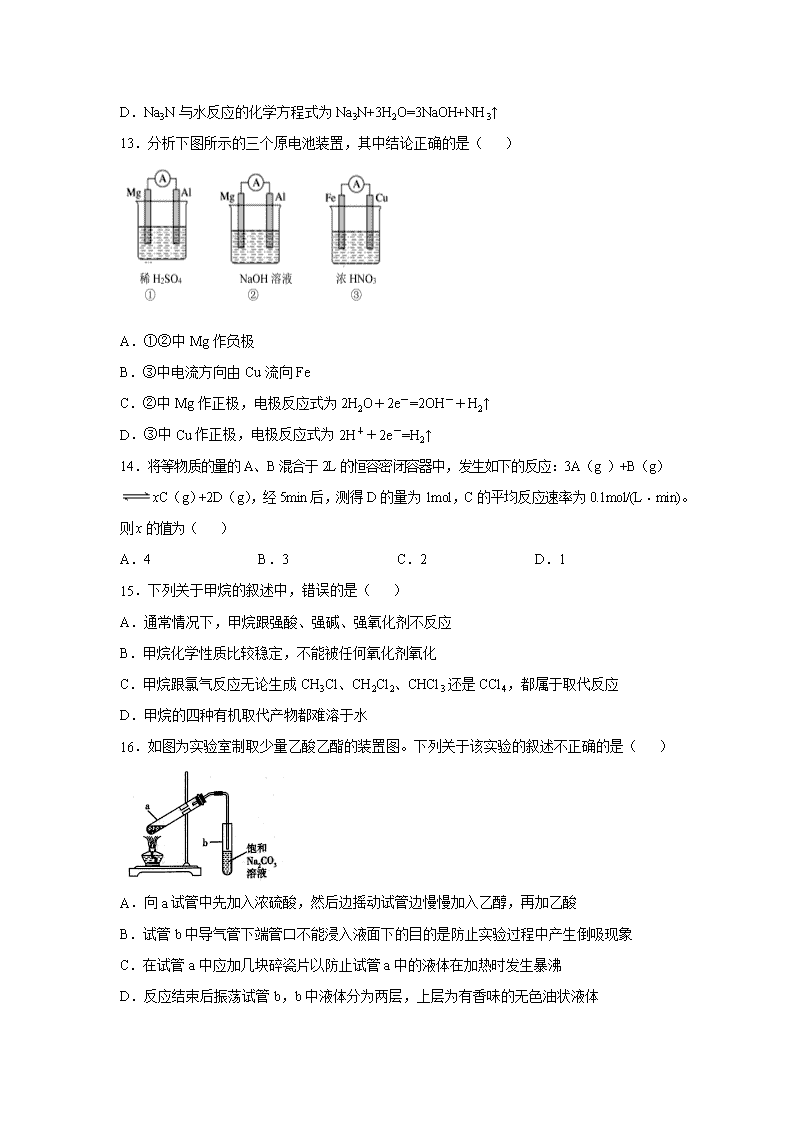
湖南省娄底市2019-2020学年高一下学期期末考试试卷 总分:100分 时量:90分钟 可能用到的相对原子质量: O 16 Zn 65 Cl 35.5 一、单选题(每题3分,共48分) 1.中学化学实验室经常用到下列实验装置,其中不可用于物质分离的是( ) A. B. C. D. 2.习主席在十九大报告中指出:“绿水青山就是金山银山。”而利用化学知识降低污染、治理污染,改善人类居住环境是化学工作者当前的首要任务。下列做法不利于环境保护的是( ) A.开发清洁能源 B.有效提高能源利用率 C.研制易降解的生物农药 D.对废电池做深埋处理 3.下列反应既属于氧化还原反应,又属于吸热反应的是( ) A.锌粒与稀硫酸的反应 B.灼热的木炭与CO2反应 C.甲烷在氧气中的燃烧反应 D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 4.苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指( ) A.甲烷 B.乙烯 C.乙炔 D.生长素 5.设NA为阿伏伽德罗常数的值,下列说法正确的是( ) A.标准状况下,22.4L以任意比例混合的氮气和氧气所含的原子数为NA B.用含有0.01mol氯化铁的水溶液制成氢氧化铁胶体,含有的胶体粒子数为为0.01NA C.标准状况下,22.4LCCl4中分子数为NA D.32gO2和O3混合气体中含有原子数为2NA 6. C1O2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得C1O2:2KClO3+H2C2O4+H2SO42ClO2↑+K2SO4+2CO2↑+2H2O,下列说法中正确的是( ) A.在反应中H2C2O4既不是氧化剂也不是还原剂 B.1 mol KClO3参加反应,在标准状况下能得到22.4 L气体 C.1 mol KClO3参加反应有2 mol电子转移 D.KClO3在反应中是氧化剂 7.在给定条件下,下列选项所示的物质间转化不能实现的是( ) A.Fe(s)FeCl3(s)Fe(OH)3(s) B.CaCl2(aq)CaCO3(s)CaO(s) C.NaHCO3(s)Na2CO3(s)NaOH(s) D.Al2O3(s)AlCl3(aq) Al(OH)3 (s) 8.下列对于元素周期表结构的叙述中,正确的是( ) A.7个横行代表7个周期,18个纵行代表16个族 B.副族元素中有非金属元素 C.除第一周期外,其他周期均有18种元素 D.碱金属元素是指ⅠA族的所有元素 9.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO、NO2的混合气体,这些气体与1.68LO2(标准状况下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗溶液NaOH的体积是( ) A.15mL B. 30mL C.45 mL D.60 mL 10. X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图示。下列说法正确的是( ) A.Y、Z、X三种元素的原子半径依次增大 B.X、Z都是第二周期ⅥA族元素,单质的氧化性X>Z C.Y的气态氢化物的热稳定性比Z的高 D.W元素最高价氧化物的水化物的酸性比Z的强 11.下列说法正确的是( ) A.氯化铵固体受热分解和干冰升华均只需克服分子间作用力 B. I2、Br2、Cl2、F2的熔、沸点逐渐降低 C.HCl气体溶于水和NaOH熔化破坏的化学键类型相同 D.NaF、H2SO4中所含化学键的类型相同 12.氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3,主要用于制造炸药及用作分析试剂等。下列分析不正确的是( ) A.化合物Na3N是由离子键形成的 B.Na3N与过量的HCl(aq)反应,生成两种盐 C.比较Na3N中两种粒子的半径:r(Na+)>r(N3-) D.Na3N与水反应的化学方程式为Na3N+3H2O=3NaOH+NH3↑ 13.分析下图所示的三个原电池装置,其中结论正确的是( ) A.①②中Mg作负极 B.③中电流方向由Cu流向Fe C.②中Mg作正极,电极反应式为2H2O+2e-=2OH-+H2↑ D.③中Cu作正极,电极反应式为2H++2e-=H2↑ 14.将等物质的量的A、B混合于2L的恒容密闭容器中,发生如下的反应:3A(g )+B(g)xC(g)+2D(g),经5min后,测得D的量为1mol,C的平均反应速率为0.1mol/(L﹒min)。则x的值为( ) A.4 B.3 C.2 D.1 15.下列关于甲烷的叙述中,错误的是( ) A.通常情况下,甲烷跟强酸、强碱、强氧化剂不反应 B.甲烷化学性质比较稳定,不能被任何氧化剂氧化 C.甲烷跟氯气反应无论生成CH3Cl、CH2Cl2、CHCl3还是CCl4,都属于取代反应 D.甲烷的四种有机取代产物都难溶于水 16.如图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述不正确的是( ) A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加乙酸 B.试管b中导气管下端管口不能浸入液面下的目的是防止实验过程中产生倒吸现象 C.在试管a中应加几块碎瓷片以防止试管a中的液体在加热时发生暴沸 D.反应结束后振荡试管b,b中液体分为两层,上层为有香味的无色油状液体 非选择题(每空2分,52分) 二、填空题 17.(本题6分)火药是古代道士配出的“药”,燃放烟花爆竹“产生大量烟雾。这种烟雾的成分是二氧化硫,与空气中的水分最终形成了稀硫酸气溶胶。 (1)根据所学知识,进行科学分析,下列说法正确的是________。 A.二氧化硫与空气中的水通过化合反应直接形成稀硫酸 B.稀硫酸具有强氧化性,可以用于杀菌消毒 C.烟花爆竹燃烧产生的SO2和可吸入颗粒物均属于大气污染物 (2)某学习小组想检验某地区的雨水中是否含有硫酸根,设计实验:取少量雨水于试管中,加入盐酸酸化无明显现象,再加入__________溶液(填“BaCl2”或“AgNO3”)产生白色沉淀。证明该地区雨水中含有硫酸根。 (3)“绿水青山就是金山银山”,工业生产中通常在煤中加入适量石灰石进行脱硫处理,解决煤燃烧产生二氧化硫的问题,完成化学方程式:2CaCO3+O2+2SO2=2__________+2CO2。 18.(本题10分)下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。 完成下列填空(填元素符号或化学式): (1)元素B在元素周期表中的位置是 ,A、B、C三种元素原子半径从大到小的顺序是_________________。 (2)D简单离子的结构示意图为_____________,D、E中金属性较强的元素是________。 (3)E的最高价氧化物的水化物与B的最高价氧化物的水化物反应的离子方程式是 。 19.(本题8分)苯是一种有毒的液体,也是良好的有机溶剂,请回答下列关于苯的问题: (1)上述反应中属于取代反应的是:__________,属于加成反应的是:__________。 (2)请写出反应③的化学方程式__________。 (3)下列化合物中,能发生类似于反应④的是__________ A.乙烷 B.乙烯 C.乙醇 20.(本题6分)在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)N2O4(g)(无色),如图所示。 (1)曲线___________(填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。 (2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中υ(NO2)=0.3mol/(L•s),乙中υ(N2O4)=6mol/(L•min),则______中反应更快。 (3)在0到3min中内N2O4的反应速率为__________。 21.(本题10分) 微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为: Zn+2OH- - 2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH- 总反应式为Ag2O+Zn=ZnO+2Ag (1)Ag2O是______极,Zn发生______反应。 (2)电子由________极流向________极(填“Zn”或“Ag2O”),当电路通过0.1mol电子时,负极消耗物质的质量是___________g。 三、实验题 22.(本题12分)某实验小组用下列装置进行乙醇催化氧化的实验。 (1)实验过程中铜网出现黑色和红色交替的现象,请写出乙醇被催化氧化的化学反应方程式_________________________________________。 (2)甲水浴的作用是_________________________________________;乙水浴的作用是_________________________________________。 (3)反应进行一段时间后,试管a中能收集到不同的物质,它们是________________。 (4)若乙装置内试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_________;要除去该物质,可在混合液中加入____________(本空填写字母)。 a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳 【参考答案】 1.A 2.D 3.B 4.B 5.D 6.D 7.B 8.A 9.D 10.D 11.B 12.C 13.C 14.C 15.B 16.A 17.C BaCl2 CaSO4 18.第二周期VA族 N>O>H Na Mg(OH)2 + 2H+ ==Mg2+ + 2H2O 19.①③ ④ +HNO3(浓)+H2O B 20.X 甲 0.05mol/(L•min) 21. 正 氧化 Zn Ag2O 3.25 22. 2CH3CH2OH+O22CH3CHO + 2H2O ; 加热,使乙醇气化 冷却,使乙醛等液化 乙醛、乙醇、水 乙酸 c 查看更多