2017-2018学年湖北省荆州中学高二上学期第一次阶段性测试化学试题
荆州中学高二年级2017~2018学年上学期阶段性考试(一)
科目:化学
考试时间:90分钟
可能用到的相对原子质量 H1 C12 N14 O16 Na23 Al27
一、单项选择题(16小题共48分)
1.下列做法能体现理性、低碳、环保生活理念的是( )
A.极力反对校园垃圾,又经常使用一次性餐具
B.夏天盖着厚被子吹空调
C.尽量购买本地的、当季的食物,减少食物的加工过程
D.开着大排量的家用汽车开直播声讨雾霾天气
2.下列变化中属于吸热反应的是( )
A.葡萄糖在人体内缓慢氧化 B.灼热的炭和二氧化碳气体化合
C.铝粉与氧化铁粉末反应 D.过氧化钠与水的反应
3.下列各组物质的燃烧热相等的是( )
A.石墨和金刚石 B.1g H2和2g H2 C.C2H2和苯 D.气态乙醇和液态乙醇
4.一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(g)⇌zC(g),达到平衡后测得A气体的浓度为0.5mol/L,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A浓度为0.4mol/L,则下列叙述正确的是( )
A.平衡向正反应方向移动 B.x+y<z C.C的体积分数降低 D.B的转化率提高
5.已知分解1 mol H2O2放出热量98 kJ。在含少量I–的溶液中,H2O2分解的机理为:
H2O2+I–→H2O+IO– 慢 H2O2+IO–→H2O+O2+I– 快
下列有关该反应的说法正确的是( )
A.反应速率与I–浓度有关 B.反应活化能为98 kJ/mol
C.IO–是该反应的催化剂 D.υ(H2O2)=υ(H2O)=υ(O2)
6.下列有关化学用语使用正确的是( )
A.H、D、T互为同素异形体
B.NH4Cl的电子式:
C.原子核内有8个质子、10个中子的氧原子: O
D.硫离子(S2‾)结构示意图:
7.NA表示阿伏加德罗常数,下列说法正确的是( )
A.11.2LH2含有的电子数目是NA
B.0.1mol/L的Na2SO4溶液中,含SO42-数目是0.1NA
C.46gNO2和N2O4的混合气体中,含氮原子数目是NA
D.1molFeCl3跟沸水完全反应转化为氢氧化铁胶体,其中胶体粒子的数目是NA
8.下列各组离子在指定溶液中一定能大量共存的是( )
A.强酸性溶液中:Na+、K+、Cl-、S2O32-
B.强碱性溶液中:Ba2+、K+、HCO3-、NO3-
C.0.lmol/L(NH4)2CO3溶液中:K+、Na+、NO3-、Cl-
D.0.lmol/LFeCl3溶液中:Na+、NH4+、SCN-、SO42-
9.足量的锌和一定量盐酸的反应,为了减缓反应速率又不影响产生氢气的总量,可采用的措施是( )
A.加NaOH固体 B.加硫酸铜固体 C.加醋酸钠固体 D.加硝酸钠溶液
10.一定条件固定容积的容器中,可逆反应X(g)+3Y(g)⇌2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol/L、0.4mol/L、0.08mol/L,则下列判断不正确的是( )
A.c1:c2的值不能确定
B.平衡时,Y和Z的生成速率之比为3:2
C.c1的取值范围为0<c1<0.14 mol/L
D.0.28mol/L
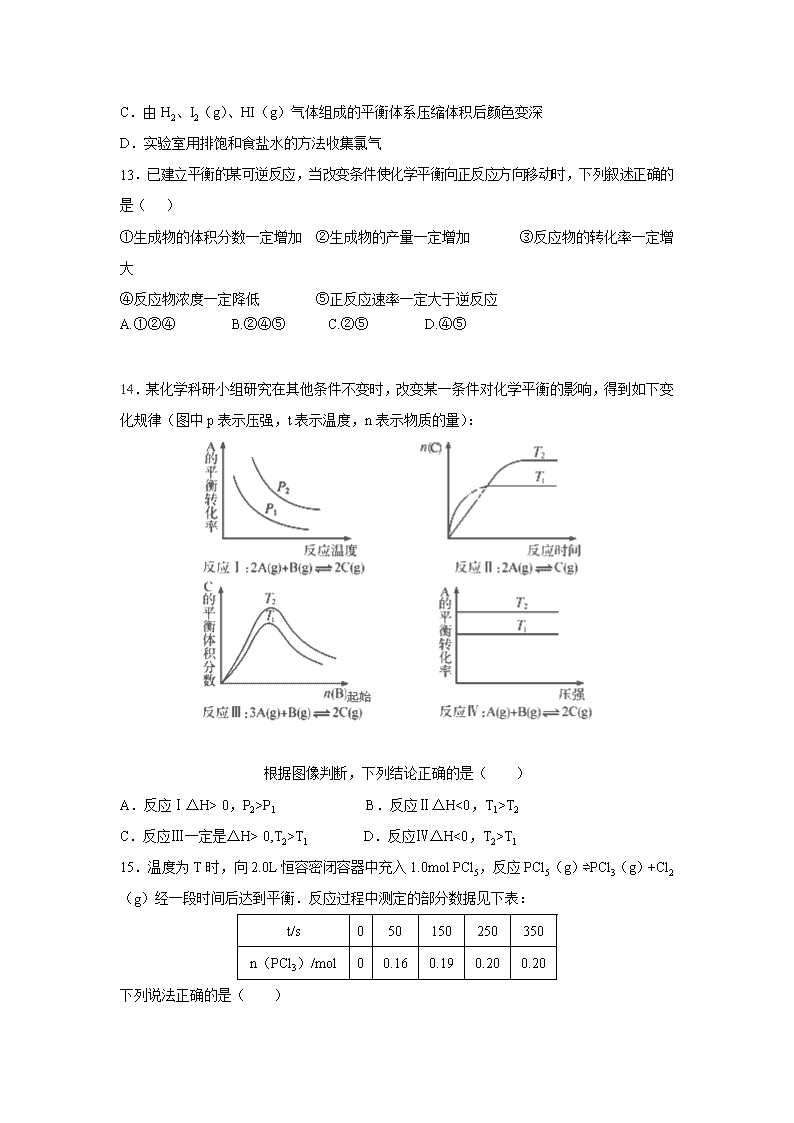
0,P2>P1 B.反应Ⅱ△H<0,T1>T2
C.反应Ⅲ一定是△H> 0,T2>T1 D.反应Ⅳ△H<0,T2>T1
15.温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)⇌PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
t/s
0
50
150
250
350
n(PCl3)/mol
0
0.16
0.19
0.20
0.20
下列说法正确的是( )
A. 反应在前50s的平均速率为v(PCl3)=0.0032mol/(L•s)
B. 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol/L,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20mol Cl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3、2.0mol Cl2,达到平衡时,PCl3的转化率小于80%
16. 可逆反应①X(g)+2Y(g)⇌2Z(g)、②2M(g)⇌N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示。下列判断正确的是( )
A.反应①的正反应是吸热反应
B.达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(Ⅰ)时,X的转化率为
D.在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数相等
二、非选择题(5小题共52分)
17.(11分)二甲醚(CH3OCH3)被称为21世纪的新型燃料,25℃,101kPa时呈气态,它清洁、高效、具有优良的环保性能。92g气态二甲醚25℃,101kPa时燃烧放热2910kJ。
(1)写出二甲醚燃烧热的热化学方程式 ;当燃烧放出582kJ热量时,转移的电子数为 。
(2)已知H2(g)和C(s)的燃烧热分别是285.8kJ/mol、393.5kJ/mo;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热为 ;
(3)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)⇌CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是 (选填字母编号)
A.c(H2)与c(H2O)的比值保持不变
B.单位时间内有2mol H2消耗时有1mol H2O生成
C.容器中气体密度不再改变
D.容器中气体压强不再改变
E.反应产生的热量不再变化
②温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产量将 (填“变大”、“变小”或“不变”,下同),混合气体的平均摩尔质量将 .
18.(8分)(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、________、________。
(2)量取反应物时,取50 mL 0.50 mol/L的盐酸,常常还需加入的试剂是________(填序号)。
A.50 mL 0.50 mol/L NaOH溶液 B.50 mL 0.55 mol/LNaOH溶液
C.55 mL 0.50mol/LNaOH溶液 D.1g固体NaOH
(3) 由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两
组测定中和热的实验,实验试剂及其用量如下表所示。
反应物
起始温度t1/℃
终了温度t2/℃
中和热/kJ/mol
A.1.0 mol/LHCl溶液50 mL、1.1 mol/L NaOH溶液50 mL
13.0
ΔH1
B.1.0 mol/L HCl溶液50 mL、1.1 mol/L NH3·H2O溶液50 mL
13.0
ΔH2
①甲在实验之前预计ΔH1=ΔH2,他的根据可能是 ;乙在实验之前预计ΔH1≠ΔH2,他的根据是 。
②实验测得的温度是:A的起始温度为13.0 ℃、终了温度为19.8 ℃;B的起始温度13.0 ℃、终了温度为19.3 ℃。设充分反应后溶液的比热容c=4.184 J/(g·℃),忽略实验仪器的比热容及溶液体积的变化,则ΔH1= (假设溶液密度均为1 g/cm3)
19.(12分)H2O2作为氧化剂在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答下列问题:
(1)定性分析:图甲可通过观察 定性比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液更合理,其理由是 。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为_________,检查该装置气密性的方法是:关闭A的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看 ,实验中需要测量的数据是 。
(3)加入MnO2粉末于H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
由D到A过程中,随着反应的进行反应速率逐渐_________。(填 “加快”或“减慢”),其变化的原因是 。(选填字母编号)
A. 改变了反应的活化能 B.改变活化分子百分比
C.改变了反应途径 D.改变单位体积内的分子总数
(4) 课本在研究浓度对反应速率影响的实验中,酸性高锰酸钾和弱酸草酸反应的离子方程式为 ,反应开始一段时间后反应速率明显提升的原因是 。
20.(12分)向一容积不变的密闭容器中充入一定量A和B,发生如下反应:
xA(g)+yB(s) zC(g) ΔH<0。反应中A和B消耗的物质的量相同,在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
(1)根据图示可确定x∶y∶z= 。(用最简整数比表示)
(2)0~10 min容器内压强 (填“变大”、“不变”或“变小”)。
(3)推测第10 min引起曲线变化的反应条件可能是________;第16 min引起曲线变化的反应条件可能是________。(选填数字编号)
①减压 ②增大A的浓度 ③增大C的量 ④升温 ⑤降温 ⑥加催化剂
(4)平衡Ⅰ的平衡常数为K1= ,平衡Ⅱ平衡常数为K2,则K1________K2(填“>”、“=”或“<”)。
(5)在平衡I的温度下,假设容积恒定为1L,下列措施中能使平衡时 n(A)/n(C)增大的有 (选填字母编号)
A.升高温度 B.充入氦气 C.再充入0.2molA和0.5molC D.使用催化剂
21.(9分)A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
(1)若常温下A为有色气体.
①当F是一种金属单质时,一定浓度的B溶液和适量F反应生成C与气体E,则F与该B溶液反应的离子方程式
②当C是一种产生温室效应的气体分子时,E具有漂白性,物质F焰色反应呈黄色,写出C与F溶液生成D的化学方程式 .
(2) 若A为淡黄色固体,D为白色难溶于水的物质,且A和D的式量相等.则A和D
中金属元素的最高价氧化物的水化物的碱性强弱顺序为 (用化学式表示)
(3)若A中一种元素原子的最外层电子数为内层电子总数的1/5,F为一种常见的气体单质,将B和D分别溶于水,所得溶液按恰当比例混合得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式: .
CBBCA DCCCD BCCBC C
17.(1)二甲醚燃烧热方程式(略) 4.8NA
(2)-378.8KJ/mol
(3)ADE 变小 变小
18. 量筒 环形玻璃搅拌棒 B
生成相同量的水产生相同的热量
氨水电离需要吸收热量
19. 产生气泡的快慢 阴离子相同更能说明铁离子和铜离子的催化效果
分液漏斗 注射器活塞是否复原 生成40mL 气体所需要的时间 减慢 D
酸性高锰酸钾和草酸的离子方程式(略)
反应生成锰离子起催化作用
20.1:1:2 变大 46 4 0.8 > AC
21.铁与稀硝酸反应的离子方程式(略) 二氧化碳和碳酸钠溶液的反应化学方程式(略) NaOH > Al(OH)3
氮化镁和水反应的化学方程式(略)