【化学】甘肃省天水一中2020-2021学年高二上学期开学考试(理)试题
甘肃省天水一中2020-2021学年高二上学期开学考试(理)试题
一、选择题(本题共1-15题,每题2分,16-20题,每题3分共45分)
1.下列各组中每种物质都既有离子键又有共价键的一组是( )
A.NaOH H2SO4 (NH4)2SO4 B.MgO Na2SO4 HNO3
C.Na2O2 KOH Na3PO4 D.HCl Al2O3 MgCl2
2.下列有关化学用语表示正确的是( )
A.中子数为10的氧原子:108O B.的结构示意图:
C.硫化钠的电子式: D.HCl的形成过程:
3.短周期元素X、Y、Z、W在元素周期表中的相对位置如下表所示。已知Y、W的原子序数之和是Z的3倍,下列说法正确的是( )
Y
Z
X
W
A.原子半径:X
Z
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W
4.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图1所示。下列说法正确的是
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>:rZ>rW>rQ
C.离子Y2-和Z 3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
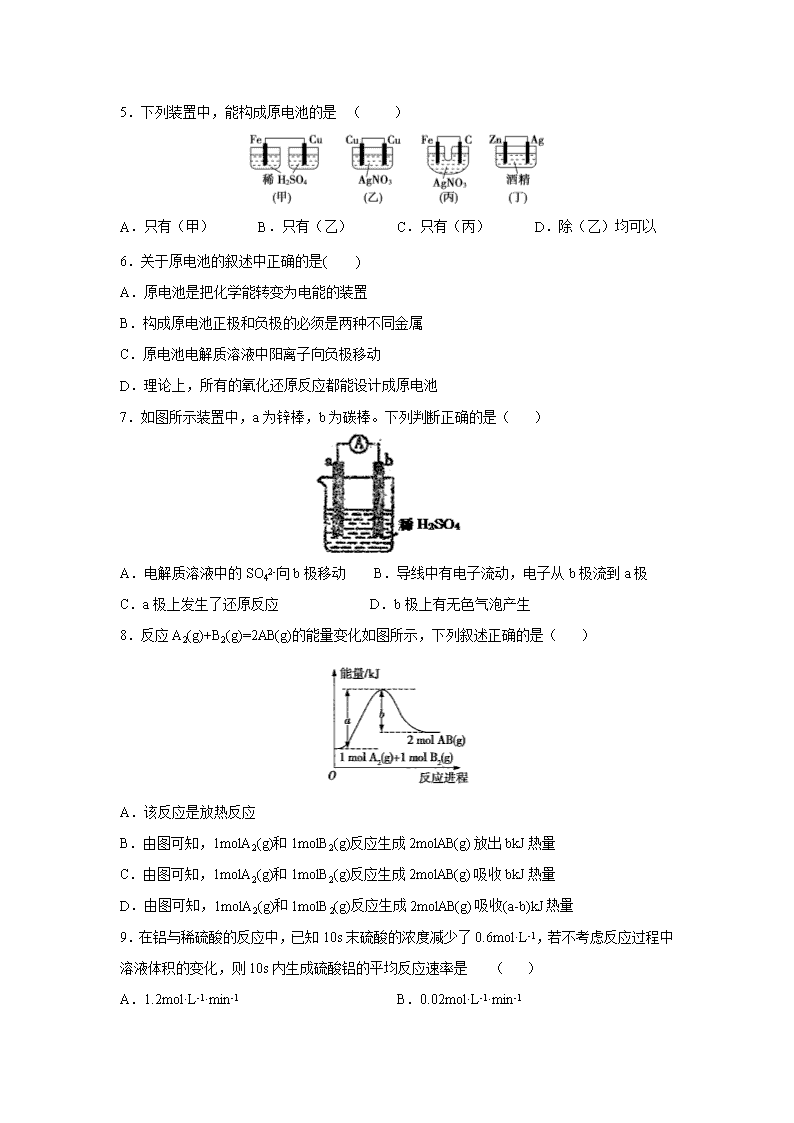
5.下列装置中,能构成原电池的是 ( )
A.只有(甲) B.只有(乙) C.只有(丙) D.除(乙)均可以
6.关于原电池的叙述中正确的是( )
A.原电池是把化学能转变为电能的装置
B.构成原电池正极和负极的必须是两种不同金属
C.原电池电解质溶液中阳离子向负极移动
D.理论上,所有的氧化还原反应都能设计成原电池
7.如图所示装置中,a为锌棒,b为碳棒。下列判断正确的是( )
A.电解质溶液中的SO42-向b极移动 B.导线中有电子流动,电子从b极流到a极
C.a极上发生了还原反应 D.b极上有无色气泡产生
8.反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述正确的是( )
A.该反应是放热反应
B.由图可知,1molA2(g)和1molB2(g)反应生成2molAB(g)放出bkJ热量
C.由图可知,1molA2(g)和1molB2(g)反应生成2molAB(g)吸收bkJ热量
D.由图可知,1molA2(g)和1molB2(g)反应生成2molAB(g)吸收(a-b)kJ热量
9.在铝与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.6mol·L-1,若不考虑反应过程中溶液体积的变化,则10s内生成硫酸铝的平均反应速率是 ( )
A.1.2mol·L-1·min-1 B.0.02mol·L-1·min-1
C.1.8mol·L-1·min-1 D.0.18mol·L-1·min-1
10.1mol乙烯与氯气发生完全加成反应,然后该加成反应的产物与足量的氯气在光照条件下发生完全取代反应,则两个过程消耗氯气的总物质的量为( )
A.3mol B.4mol C.5mol D.6mol
11.下列物质不可能是乙烯的加成产物的是( )
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
12.某有机物的结构简式如图,下列关于该有机物的说法正确的是( )
A.分子式为C7H6O5 B.1 mol该物质能与4 mol Na发生反应
C.分子中含有两种官能团 D.在水溶液中羧基和羟基均能电离出H+
13.如图是四种常见有机物分子的比例模型示意图。下列说法正确的是( )
A.甲是甲烷,甲烷的二氯取代产物只有一种结构
B.乙是乙烯,乙烯可与溴水发生取代反应使溴水褪色
C.丙是苯,苯结构比较稳定,不能发生氧化反应
D.丁是乙酸,一定条件下乙酸能跟乙醇发生酯化反应
14.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是( )
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中的碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
15.分子式为C4H10O且能与金属钠反应放出氢气的有机物有( )
A.4种 B.5种 C.6种 D.7种
16.下列实验操作和现象与结论的关系相符的是( )
操作和现象
结论
A
将一小块钠分别投入盛有水和乙醇的小烧杯中,钠与乙醇反应要平缓得多
乙醇分子中的氢与水分子中的氢具有相同的活性
B
在催化剂存在的条件下,石蜡油加强热生成的气体通入溴的四氯化碳溶液中,溶液褪色
石蜡油的分解产物中含有烯烃
C
甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红
生成的氯甲烷具有酸性
D
向蔗糖溶液中加入稀硫酸,水浴加热一段时间后,再加入新制Cu(OH)2悬浊液,用酒精灯加热,未见砖红色沉淀
蔗糖未水解
A.A B.B C.C D.D
17.下列关于常见有机物的说法中正确的是( )
A.淀粉和纤维素水解的最终产物都是葡萄糖
B.乙烯和乙烷的混合气体可用酸性高锰酸钾溶液分离
C.苯能发生取代反应生成氯苯、硝基苯等,但是不能发生氧化反应
D.光照条件下,控制CH4和Cl2的比例为1∶1,能够制得纯净的CH3Cl和HCl
18.海水开发利用的部分过程如图所示。下列说法错误的是( )
A.向苦卤中通入Cl2是为了提取溴 B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
19
.金属锂是密度最小的金属,等质量的不同金属,锂可以释放出更多电子,故常用来制造高性能电池。已知锂的金属性介于钠和镁之间,则冶炼金属锂应采用的方法是( )
A.电解法 B.热还原法 C.热分解法 D.铝热法
20.由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后将生成的气体先通过足量浓硫酸,再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为( )。
A.0.1mol B.大于或等于0.2mol,小于0.3mol
C.等于0.2mol D.大于0.1mol小于0.3mol
二、综合题
21(共8分).下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
(1)①的元素符号是________;②的氢化物电子式________
(2)②和⑤的原子半径大小关系是②________⑤(填“>”“<”或“=”);
(3)③和⑤形成的化合物含有的化学键是__________(填“离子键”或“共价键”);
(4)③、④的最高价氧化物对应的水化物相互反应的离子方程式为_____________________。
22(共18分).化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解液。放电时总反应为:Pb + PbO2 + 2H2SO4 = 2PbSO4 + 2H2O
① 写出放电时负极的电极反应式:______________________________;
② 铅蓄电池放电时,溶液的pH将_________(填增大、减小或不变)。当外电路上有0.5mol电子通过时,溶液中消耗H2SO4的物质的量为___________。
③ 放电完后,对该电池进行充电,在连接电源的负极一端生成________。(填“Pb”或“PbO2”)
(2)下图是某宇宙飞船中使用的氢氧燃料电池。其导电介质为KOH,总反应为:2H2 + O2=2H2O。
① 则负极通入的是_______,(填“H2”或“O2”)负极电极反应式为: ,正极电极反应式为: 。
②如把导电介质改为稀H2SO4,则电极反应式为:负极 ,正极______________。
23(共12分).I.A~D是四种烃分子的球棍模型(如图)
(1)与A互为同系物的是 (填序号)。
(2)能使酸性高锰酸钾溶液褪色的物质是 (填序号)。
(3)D和液溴反应的化学方程式是_____________。
Ⅱ. 某些有机物的转化如下图所示。 已知A的产量可以用来衡量一个国家的石油化工水平,D是食醋的有效成分。
请回答下列问题:
(4)A中官能团的名称是 。
(5)B的结构简式为 。
(6)反应③的化学方程式为 。
24(共17分).某人设计淀粉利用方案如下图所示:其中A是乙烯能催熟水果,B是高分子化合物,D是有水果香味的物质。请回答以下问题:
(1)“C6H12O6”的名称是 (1分),工业上由石蜡制取A的方法称作____。C中含有官能团名称是____________;
(2)A→B反应类型为 ;C→D反应类型为 ;
(3)写出下列转化的化学方程式
①A→B: ;
②C→D: ;
③CH3CH2OH→CH3CHO: 。
(4)已知A能使酸性高锰酸钾褪色,还原产物为Mn2+,写出该氧化还原反应的离子方程式 。
参考答案
1.C 2.B 3.C 4.A 5.C 6.A 7.D 8.D 9.A 10.C 11.B 12.B
13.A 14.D 15.A 16.B 17.A 18.C 19.A 20.C
21.(共8分,每空2分)O < 离子键 Al(OH)3+OH-=+2H2O
22.(共18分,每空2分)Pb -2e- + SO42- = PbSO4 增大 0.5mol Pb H2 H2 -2e- + 2OH- =2H2O O2 + 4e- + 2H2O = 4OH- H2 – 2e- = 2H+ O2 + 4H+ + 4e- = 2H2O
23.(共12分,每空2分)C B +Br2 +HBr 碳碳双键 CH3CH2OH或C2H5OH CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O。
24.(共17分,除第一空外,每空2分)
葡萄糖(1分) 裂解 羧基 加聚反应 取代(酯化)反应 CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O 2CH3CH2OH+O22CH3CHO+2H2O 5C2H4+12MnO4-+36H+=10CO2+12Mn2++28H2O