- 2021-07-02 发布 |
- 37.5 KB |
- 19页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
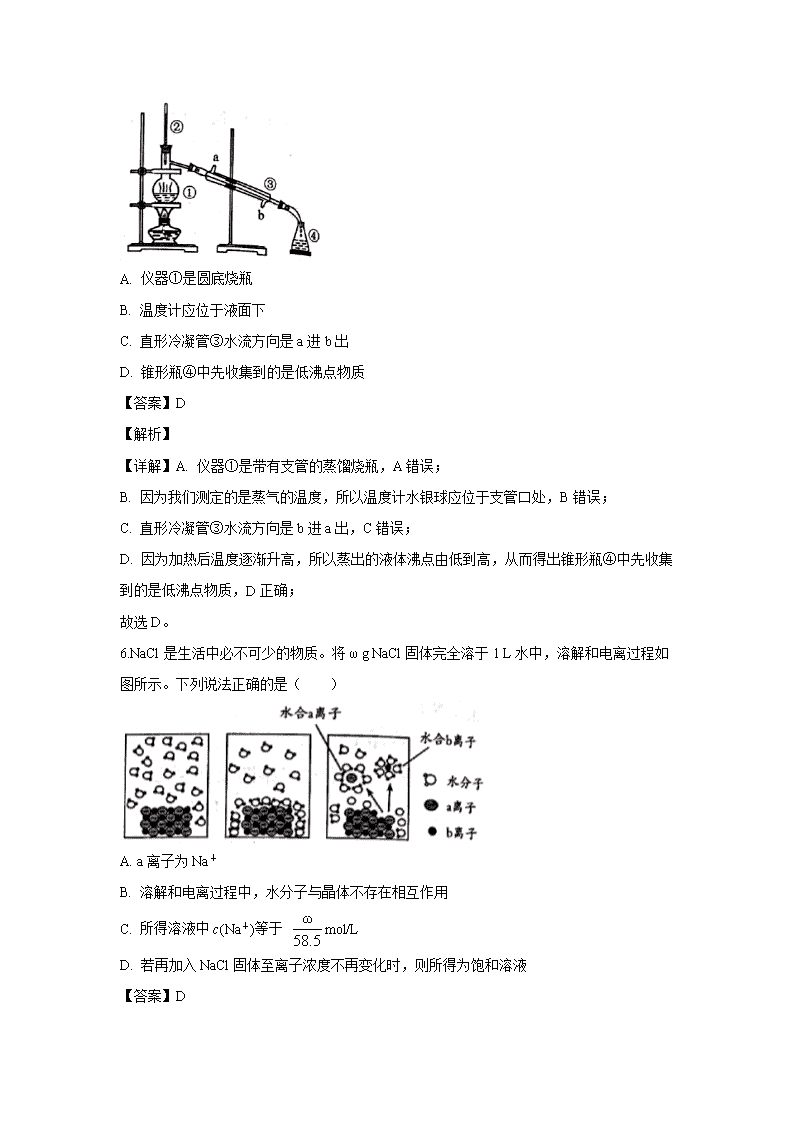
【化学】四川省成都市2019-2020学年高一上学期期末调研考试试题(解析版)
四川省成都市2019-2020学年高一上学期期末调研考试试题 可能用到的相对原子质益:0-16 Na-23 Cl-35.5 第I卷(选择题,共40分) 本卷共20题,每题2分,共40分。每题只有一个选项符合题意。 1.下列物质的应用中,利用了该物质氧化性的是( ) A. 氨——作制冷剂 B. 漂粉精——作游泳池消毒剂 C. 硅——太阳能电池板 D. SO2——漂白草帽 【答案】B 【解析】 【详解】A. 液态制冷是利用氨由液态变为气态时吸热,使环境温度降低,A不合题意; B. 漂粉精中的ClO-具有氧化性,能杀死细菌,可作游泳池消毒剂,B符合题意; C. 硅能产生光电效应,利用太阳能电池板将光能转化为电能,C不合题意; D SO2能与有色物质结合(非氧化还原)成无色物质,用于漂白草帽,D不合题意; 故选B。 2.铝是生活中常见的金属材料,下列说法错误的是( ) A. 铝是地壳中含量最多的元素 B. 铝可用于制作易拉罐 C. 铝箔可用于药品包装 D. 将铝质饮料罐等回收利用有利于节能减排保护环境 【答案】A 【解析】 【详解】A. 地壳中含量最多的元素是氧,A错误; B. 铝密度小,抗腐蚀,可用于制作易拉罐,B正确; C. 利用铝具有良好的延展性,将铝制成铝箔,可用于药品包装,C正确; D. 将铝质饮料罐属于金属材料,可回收利用,同时有利于节能减排,D正确; 故选A。 3.如图将充满二氧化氮的试管倒扣在水槽中,下列叙述错误的是( ) A. 试管内液面上升 B. 试管内气体颜色逐渐变浅,直至消失 C. 堵住管口将试管取出,管口向上松开手指,观察到试管口有红棕色出现 D. 取少量试管内液体,滴加石蕊试液后褪色 【答案】D 【解析】 【分析】 二氧化氮溶于水后,发生如下反应:3NO2+H2O==2HNO3+NO,NO2气体为红棕色,NO气体为无色。 【详解】A. 从反应方程式可以看出,3体积的NO2与水反应后,只生成1体积的NO,随着反应的进行,试管内气压会减小,所以试管内液面上升,A正确; B. 试管内气体由NO2转化为NO,所以气体的颜色逐渐变浅,直至消失,B正确; C. 松开手指后,试管内的NO与空气接触,生成NO2,试管口有红棕色出现,C正确; D. 反应后,试管内液体为稀硝酸,滴加石蕊试液,溶液只变红不褪色,D错误; 故选D。 4.下列物质的分类正确的是( ) A. Al2O3——碱性氧化物 B. Na2SiO3——硅酸盐 C. 浓硫酸——电解质 D. 氢氧化铁胶体——悬浊液 【答案】B 【解析】 【详解】A. Al2O3为两性氧化物,A错误; B. Na2SiO3属于硅酸盐,B正确; C. 浓硫酸为混合物,既不属于电解质,也不属于非电解质,C错误; D. 氢氧化铁胶体和悬浊液都属于分散系,胶体不属于悬浊液,D错误; 故选B。 5.如图是某小组组装的蒸馏实验装置。下列分析正确的是( ) A. 仪器①是圆底烧瓶 B. 温度计应位于液面下 C. 直形冷凝管③水流方向是a进b出 D. 锥形瓶④中先收集到的是低沸点物质 【答案】D 【解析】 【详解】A. 仪器①是带有支管的蒸馏烧瓶,A错误; B. 因为我们测定的是蒸气的温度,所以温度计水银球应位于支管口处,B错误; C. 直形冷凝管③水流方向是b进a出,C错误; D. 因为加热后温度逐渐升高,所以蒸出的液体沸点由低到高,从而得出锥形瓶④中先收集到的是低沸点物质,D正确; 故选D。 6.NaCl是生活中必不可少的物质。将ω g NaCl固体完全溶于1 L水中,溶解和电离过程如图所示。下列说法正确的是( ) A. a离子为Na+ B. 溶解和电离过程中,水分子与晶体不存在相互作用 C. 所得溶液中c(Na+)等于 mol/L D. 若再加入NaCl固体至离子浓度不再变化时,则所得为饱和溶液 【答案】D 【解析】 【详解】A. Na+ 核外有2个电子层,Cl-核外有3个电子层,则r(Na+)查看更多