- 2021-07-02 发布 |
- 37.5 KB |
- 5页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020学年高一化学下学期期末联考试题新人教版
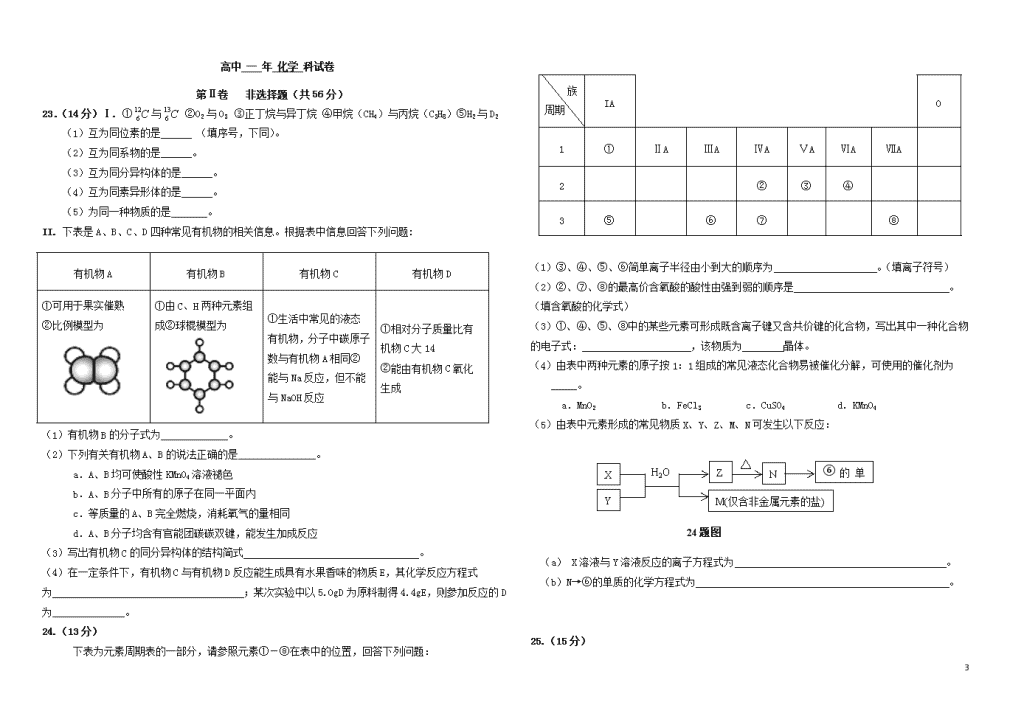
2017---2019学年度第二学期期末联考 高中 一 年 化学 科试卷 考试时间:7月 3日 完成时间:90分钟 满分:100分 可能用到的原子量:H—1 C—12 N—14 O—16 S—32 Fe—56 Ba—137 第 Ⅰ 卷 选择题(只有一个选项符合题意,每小题2分,共44分) 1.化学与社会、生产、生活紧密相关,下列说法正确的是 ( ) A.油脂、糖类和蛋白质都是高分子化合物,一定条件下能发生水解 B.鸡蛋清中加入 Na2SO4、CuSO4都会因盐析产生沉淀 C.石油的分馏和煤的干馏都属于物理变化 D.75%(体积分数)的乙醇溶液常用于医疗消毒 2. 下列有关化学用语的表示不正确的是 ( ) A.二氧化碳分子的比例模型: B.羟基的电子式: C.中子数为18的氯原子: D.乙酸乙酯的最简式为C2H4O 3.化合物(SiO2)是生产光导纤维的原料。下列叙述中正确的是( ) A.SiO2与水反应生成硅酸 B.SiO2是酸性氧化物,所以不溶于任何酸 C.SiO2可与氢氧化钠反应 D.SiO2与干冰、冰属于同一类晶体 4.下列对物质的用途描述中错误的是( ) A.氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性 B.明矾可以消毒杀菌常用于净水 C.氢氧化铝在医疗上是治疗胃酸过多的一种药剂 D.镁燃烧时发出耀眼的火焰,可以用镁来制造照明弹和焰火等 5.下列物质中,既含有离子键又含有共价键的是( ) A.HClO B.NaCl C.Na2O2 D.Ar 6.下列变化化学键未被破坏的是( ) A.HCl溶于水 B.NaOH固体熔化 C.NH4HCO3分解 D.碘升华 7.下列各组物质各自形成的晶体,均属于分子晶体的化合物是( ) A.NH3、HT、CCl4 B.H2O2、CO2、H2SO4 C.SO2、SiO2、P2O5 D.C2H6、K2S、HCl 8.设NA为阿伏加德罗常数的值,下列说法正确的是 ( ) A.标准状况下,22.4L四氯化碳中含共价键数目为4NA B.常温下,46g NO2、N2O4组成的混合气体中所含有的分子数为NA C.36g18O2中含有的中子数目为20NA D.2.24 L(标准状况)Cl2与足量铁反应时,转移电子数目为0.3NA 9.在酸性溶液中,能共存的离子组是( ) A.Na+、K+、SO42-、HCO3- B.Fe3+、K+、SO32-、NO3-- C.NH4+、K+、Cl-、NO3-- D.Fe3+、Na+、SCN-、Cl-- 10.下列对应部分反应的离子方程式书写正确的是( ) A.向H2SO4溶液中加入Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O B.往KOH中通入过量CO2:CO2+2OH-=CO32-+H2O C.碳酸钡溶于醋酸:BaCO3+2H+=Ba2++H2O+CO2↑ D.实验室用过量NaOH溶液处理Cl2尾气:Cl2+2OH-=Cl-+ClO-+H2O 11题图 11.下图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压胶管的胶头,下列与试验事实不相符的是( ) A.CO2(NaHCO3溶液)无色喷泉 B.NH3(H2O含酚酞)红色喷泉 C.H2S(CuSO4溶液)黑色喷泉 D.HCl(AgNO3溶液)白色喷泉 12.下列物质一定是纯净物的是( ) A.氯仿(CHCl3) B.C C.C4H10 D.分子组成为C2H6O的有机物 13.为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法正确的是 ( ) 序号 不纯物 除杂试剂 分离方法 A. C2H6 (C2H4) 酸性KMnO4溶液 洗气 B. 乙酸乙酯 (乙酸) 饱和Na2CO3溶液 蒸馏 C. 溴苯 (溴) KI溶液 分液 D. 酒精(乙酸) 新制生石灰 蒸馏 5 14.若用乙烯和氯气在适当的条件下反应制取三氯乙烷,这一过程中所发生的反应的类型及消耗氯气的量是(设乙烯为1mol,反应产物中的有机物只有三氯乙烷) ( ) A.取代反应,4molCl2 B.加成反应,2molCl2 C.加成反应、取代反应,2molCl2 D.加成反应、取代反应,3molCl2 15.短周期元素X、Y、Z中,其中X、Y位于同一主族,X、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比X原子少1个,下列说法不正确的是 ( ) A.原子半径:X查看更多