2019届二轮复习化学反应速率与化学平衡作业(江苏专用)
化学反应速率与化学平衡
一、选择题(每个小题有1~2个选项符合题意,每题5分,共40分)
1.(2018·三明模拟)将0.6 mol A和0.5 mol B充入0.4 L密闭容器中发生2A(g)+B(g) mD(g)+E(g),经过5 min后达到化学平衡,此时测得D为0.2 mol。又知5 min内用E表示的平均反应速率为0.1 mol·L-1·min-1,下列结论正确的是( )
A.A、B均转化了20%
B.m值为1
C.5 min内用A表示的平均反应速率为0.1 mol·L-1·min-1
D.平衡时混合物总物质的量为1 mol
解析:选B 5 min内E的物质的量变化值Δn=0.1 mol·L-1·min-1×5 min×0.4 L=0.2 mol。
2A(g)+B(g) mD(g)+E(g)
n(始)/mol 0.6 0.5 0 0
Δn/mol 0.4 0.2 0.2 0.2
n(平)/mol 0.2 0.3 0.2 0.2
故α(A)=×100%≈66.7%,α(B)=×100%=40%;=,m=1;v(A)=2v(E)=0.2 mol·L-1·min-1; n(总)=(0.2+0.3+0.2+0.2)mol=0.9 mol。
2.如图所示为800 ℃时X、Y、Z三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )
A.发生的反应可表示为2X(g) 2Y(g)+Z(g)
B.前2 min X的分解速率为0.1 mol·L-1·min-1
C.开始时,正逆反应同时开始
D.2 min时,X、Y、Z的浓度之比为2∶3∶1
解析:选C 根据图像,反应过程中X的浓度减小,Y、Z浓度增大,因此X为反应物,Y、Z为生成物,根据浓度的变化量可以确定反应为2X(g) 2Y(g)+Z(g),A正确;前2 min,v(X)==0.1 mol·L-1·min-1,B正确;开始时加入的物质为X和Y,没有Z,C错误;根据图像,2 min时,X、Y、Z的浓度分别为0.2 mol·L-1、0.3 mol·L-1、0.1 mol·L-1,D正确。
3.下列有关说法不正确的是( )
A.某吸热反应能自发进行,因此该反应是熵增反应
B.2NO(g)+2CO(g)===N2(g)+2CO2(g) 在常温下能自发进行,则该反应的ΔH>0
C.反应NH3(g)+HCl(g)===NH4Cl(s) 在室温下能自发进行,则该反应的ΔH<0
D.CaCO3(s)===CaO(s)+CO2(g) 室温下不能自发进行,说明该反应的ΔH>0
解析:选B A项,当ΔH-TΔS<0时,反应能自发进行,吸热反应的ΔH>0,能自发,说明ΔS>0,正确;B项,反应为气体体积减小的反应,ΔS<0,若反应能自发进行,则ΔH-TΔS<0,故反应的ΔH<0,错误;C项,根据该反应中各物质的聚集状态可知,该反应的ΔS<0,在室温下该反应能自发进行,则该反应为放热反应,正确; D项,不能自发进行说明该反应ΔH-TΔS>0,该反应ΔS>0,则ΔH>0,正确。
4.PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生反应:PCl3(g)+Cl2(g) PCl5(g),并于10 min时达到平衡。有关数据如表所示:
PCl3(g)
Cl2(g)
PCl5(g)
初始浓度(mol·L-1)
2.0
1.0
0
平衡浓度(mol·L-1)
c1
c2
0.4
下列判断不正确的是( )
A.10 min内,v(Cl2)=0.04 mol·L-1·min-1
B.当容器中Cl2为1.2 mol时,反应达到平衡
C.升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的<1
D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol·L-1
解析:选C PCl3(g)+Cl2(g) PCl5(g)
起始(mol·L-1) 2.0 1.0 0
转化(mol·L-1) 0.4 0.4 0.4
平衡(mol·L-1) 1.6 0.6 0.4
10 min内,v(Cl2)=0.04 mol·L-1·min-1,A正确;平衡时,n(Cl2)=1.2 mol,B正确;升高温度,平衡常数减小,说明平衡逆向移动,则PCl3的>1,C错误;移走2.0 mol PCl3和1.0 mol Cl2后,若平衡不移动,c(PCl5)=0.2 mol·L-1,但压强减小,平衡向逆反应方向进行,故达到平衡时,c(PCl5)<0.2 mol·L-1,D正确。
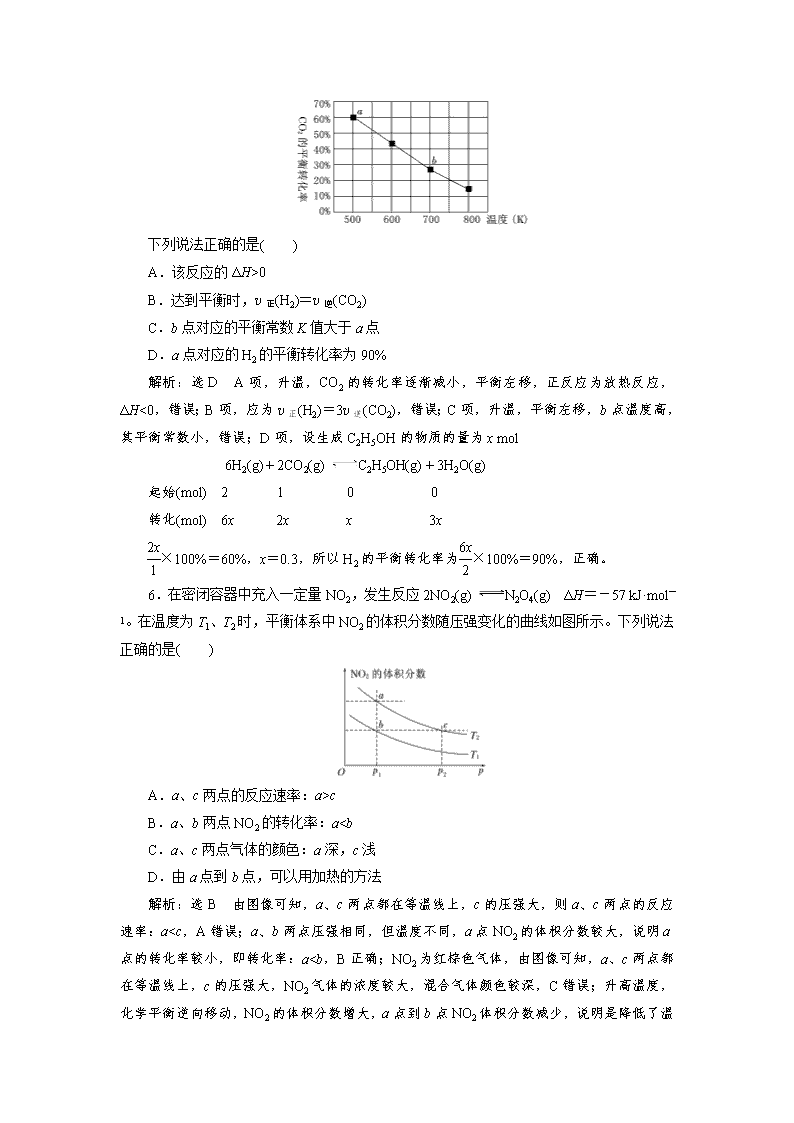
5.一定条件下,反应:6H2(g)+2CO2(g) C2H5OH(g)+3H2O(g)的数据如下图所示[反应物起始物质的量之比:n(H2)∶n(CO2)=2]。
下列说法正确的是( )
A.该反应的ΔH>0
B.达到平衡时,v正(H2)=v逆(CO2)
C.b点对应的平衡常数K值大于a点
D.a点对应的H2的平衡转化率为90%
解析:选D A项,升温,CO2的转化率逐渐减小,平衡左移,正反应为放热反应,ΔH<0,错误;B项,应为v正(H2)=3v逆(CO2),错误;C项,升温,平衡左移,b点温度高,其平衡常数小,错误;D项,设生成C2H5OH的物质的量为x mol
6H2(g)+2CO2(g) C2H5OH(g)+3H2O(g)
起始(mol) 2 1 0 0
转化(mol) 6x 2x x 3x
×100%=60%,x=0.3,所以H2的平衡转化率为×100%=90%,正确。
6.在密闭容器中充入一定量NO2,发生反应2NO2(g) N2O4(g) ΔH=-57 kJ·mol-1。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是( )
A.a、c两点的反应速率:a>c
B.a、b两点NO2的转化率:a
②>③
C.在P点,CO转化率为75%
D.在P点,向容器②中再充入CO、H2及CH3OH各0.025 mol,此时v(CO)正②>③,故容积大小为①<②<③,错误;C项,P点甲醇的体积分数为50%,设CO转化的物质的量为x,则氢气转化了2x,甲醇生成了x,50%=得到x=0.075,所以CO的转化率为×100%=75%,正确;D项,设②容器体积为V,P点平衡的时候,CH3OH的物质的量为0.075 mol,浓度为 mol·L-1,CO的物质的量为0.025 mol,浓度为 mol·L-1,H2的物质的量为 0.05 mol,浓度为 mol·L-1,K==1 200 V2,再充入CO、H2及CH3OH各0.025 mol,同样的方法计算得到离子积Qc≈356 V2,Qcv(CO)逆,错误。
8.(2018·南阳模拟)将1 mol N2和3 mol H2充入体积可变的恒温密闭容器中, 在380 ℃下发生反应:
N2(g)+3H2(g)2NH3(g),平衡时,体系中氨的体积分数φ(NH3)随压强变化的情况如下表:
压强/MPa
10
20
30
40
φ(NH3)
0.30
0.45
0.54
0.60
下列说法正确的是( )
A.10 MPa时,H2的转化率为75%
B.20 MPa时,NH3的物质的量浓度是10 MPa时的倍
C.40 MPa时,若容器的体积为V L,则平衡常数K=
D.30 MPa时,若向容器中充入惰性气体,则平衡向正反应方向移动
解析:选BC N2(g)+3H2(g)2NH3(g)
开始(mol) 1 3 0
反应(mol) x 3x 2x
平衡(mol) 1-x 3-3x 2x
A项,10 MPa时,2x=0.3×(4-2x)mol,解得x=mol,H2的转化率为×100%,错误;B项,20 MPa时,2x=0.45×(4-2x)mol,解得x=mol,NH3的物质的量浓度是10 MPa时的倍,正确;C项,40 MPa时,2x=0.6×(4-2x)mol,解得x=0.75 mol,若容器的体积为V L,则平衡常数K==,正确;D项,30 MPa时,若向容器中充入惰性气体,容器的体积增大,相当于对平衡体系减小压强,平衡向逆反应方向移动,错误。
二、非选择题(4个小题,共60分)
9.(15分)雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃烧尾气是造成空气污染的原因之一。汽车尾气净化的主要原理为2NO(g)+2CO(g)2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
据此判断:
(1)该反应的ΔH________0(填“>”或“<”),ΔS________0(填“>”或“<”)。
(2)在T1温度下,0~2 s内的平均反应速率v(N2)=________________。
(3)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若增大催化剂的表面积,则CO转化率________(填“增大”“减小”或“不变”)。
(4)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填字母)。
解析:(1)由图可知,温度T1时先到达平衡,故T1>T2,温度越高,平衡时CO2的浓度越低,说明升高温度平衡向逆反应方向移动,故正反应为放热反应,即ΔH<0,2NO(g)+2CO(g)2CO2(g)+N2(g),反应前后气体体积减小,反应熵变ΔS<0。
(2)由图可知,T1温度时2 s到达平衡,平衡时CO2的浓度变化量为0.2 mol·L-1,故v(CO2)==0.1 mol·L-1·s-1,速率之比等于化学计量数之比,故v(N2)=v(CO2)=×0.1 mol·L-1·s-1=0.05 mol·L-1·s-1。
(3)接触面积越大反应速率越快,到达平衡的时间越短,但催化剂不影响平衡移动,CO的转化率不变。
(4)到达平衡后正、逆反应速率相等,不再变化,t1时刻v正最大,之后随反应进行速率发生变化 ,未到达平衡,故a错误;该反应正反应为放热反应,随反应进行温度升高,化学平衡常数减小,到达平衡后,温度为定值,达最高,平衡常数不变,为最小,图像与实际符合,故b正确;t1时刻后CO2、NO的物质的量发生变化 ,t1时刻未到达平衡状态,故c错误;NO的质量分数为定值,t1时刻处于平衡状态,故d正确。
答案:(1)< < (2)0.05 mol·L-1·s-1 (3)不变 (4)bd
10.(16分)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1
ΔH1<0 (Ⅰ)
2NO(g)+Cl2(g)2ClNO(g) K2 ΔH2<0 (Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________________________________________________________________________(用K1、
K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L 恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min 时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后 n(Cl2)=_______mol,NO的转化率α1=________。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2____α1(填“>”“<”或“=”),平衡常数K2______(填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是________________________________________________________________________。
解析:(1)将题干中已知的两个化学方程式做如下处理:(Ⅰ)×2-(Ⅱ)可得4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g),则其平衡常数K=。
(2)根据“三段式”:
2NO(g) + Cl2(g) 2ClNO(g)
起始(mol·L-1) 0.1 0.05 0
转化(mol·L-1) 0.1α1 0.05α1 0.1α1
平衡(mol·L-1) 0.1-0.1α1 0.05-0.05α1 0.1α1
v(ClNO)==7.5×10-3 mol·L-1·min-1,得α1=75%,平衡时n(Cl2)=(0.05-0.05α1) mol·L-1×2 L=0.025 mol。该反应为气体分子数减小的反应,恒压条件下相对于恒容条件下,压强增大,平衡右移,NO的转化率增大,即α2>α1;化学平衡常数只与温度有关,温度不变,平衡常数K2不变;该反应为放热反应,升高温度可使平衡常数K2减小。
答案:(1)
(2)2.5×10-2 75% > 不变 升高温度
11.(11分)NO能引起光化学烟雾,破坏臭氧层。处理NO有多种方法。利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH=-748 kJ·mol-1,为了测定某催化剂作用下的反应速率,在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生上述反应。用气体传感器测得不同时间NO浓度如表:
时间(s)
0
1
2
3
4
……
c(NO)/
(mol·L-1)
1.00×
10-3
4.00×
10-4
1.70×
10-4
1.00×
10-4
1.00×
10-4
……
根据题意回答下列问题:
(1)前2 s内的平均反应速率v(N2)=________________(保留3位有效数字,下同);计算此温度下该反应的K=________。
(2)达到平衡时,下列措施能提高NO转化率的是_______(填字母)。
a.选用更有效的催化剂
b.降低反应体系的温度
c.充入氩气使容器内压强增大
d.充入CO使容器内压强增大
解析:(1)根据表格中数据算出前2 s内的平均反应速率v(NO)==4.15×10-4mol·L-1·s-1,根据化学反应速率之比等于化学计量数之比,v(N2)=v(NO)≈2.08×10-4 mol·L-1·s-1;由表格数据看出第3 s后c(NO)不变则达平衡,此时c(CO)=1.00×10-4 mol·L-1,c(CO2)=1.00×10-3mol·L-1-1.00×10-4mol·L-1=9.00×10-4mol·L-1,c(N2)=c(CO2)=4.50×10-4mol·L-1,K=≈3.65×106。
(2)达到平衡时,要提高NO转化率,即改变条件使平衡正向移动,选用更有效的催化剂,平衡不移动,a错误;降低反应体系的温度,该反应为放热反应,正向移动,b正确;充入氩气使容器内压强增大,但平衡不移动,c错误;充入CO使容器内压强增大,相当于增大CO浓度,平衡正向移动,NO转化率提高,d正确。
答案:(1)2.08×10-4 mol·L-1·s-1 3.65×106 (2)bd
12.(18分)甲醇是重要的化工原料,又是一种可再生能源,具有广泛的开发和应用前景。
(1)已知反应CO(g)+2H2(g) CH3OH(g) ΔH=-99 kJ·mol-1中的相关化学键键能如下:
化学键
H—H
C—O
CO
H—O
C—H
E/(kJ·mol-1)
436
343
x
465
413
则x=________。
(2)在一容积可变的密闭容器中,1 mol CO与2 mol H2发生反应:CO(g)+2H2(g)CH3OH(g) ΔH1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图所示。
①a、b两点的反应速率:v(a)_____v(b)(填“>”“<”或“=”)。
②T1________T2(填“>”“<”或“=”),原因是____________________________________
________________________________________________________________________。
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是________(填代号)。
A.H2的消耗速率是CH3OH生成速率的2倍
B.CH3OH的体积分数不再改变
C.混合气体的密度不再改变
D.CO和CH3OH的物质的量之和保持不变
④计算图中a点的平衡常数Kp=______________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
解析:(1)ΔH=x kJ·mol-1+2EH—H-(3EC—H+EC—O+EO—H)=x kJ·mol-1+2×436 kJ·mol-1-(3×413+343+465)kJ·mol-1=-99 kJ·mol-1,解得x=1 076。(2)①观察图像知,当温度为T2时,a点的压强小于b点,则反应速率:v(a)
查看更多