2019届二轮复习实验方案设计与评价学案(全国通用)
第16讲 实验方案设计与评价
最新考纲
考向分析
1.掌握常见气体的实验室制法(包括所用试剂、仪器、反应原理和收集方法)。
2.设计、评价或改进实验方案。
3.了解控制实验条件的方法。
4.分析或处理实验数据,得出合理的结论。
5.绘制和识别典型的实验仪器装置图。
6.以上各部分知识与技能的综合应用。
1.客观题:主要依托实验验证物质的化学性质,并对已设计的方案是否符合实验要求作出判断。
2.主观题:将在综合实验设计题或工艺流程图题中,以探究物质的化学性质、组成、结构与含量及其制备等为目的,考查原理、实验操作、有关的计算及实验方案的设计与评价等。
考点一 物质制备型实验方案的设计与评价
Z (课前)
1.(2016·江苏)根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是( C )
A.制备氨气 B.制取NaHCO3
C.分离NaHCO3 D.干燥NaHCO3
[解析] A项,制NH3需要用NH4Cl固体和Ca(OH)2固体加热进行反应,错误;B项,CO2应从长导管进短导管出,错误;C项,制得的NaHCO3为固体,用过滤法分离,正确;D项,加热时NaHCO3会分解,错误。
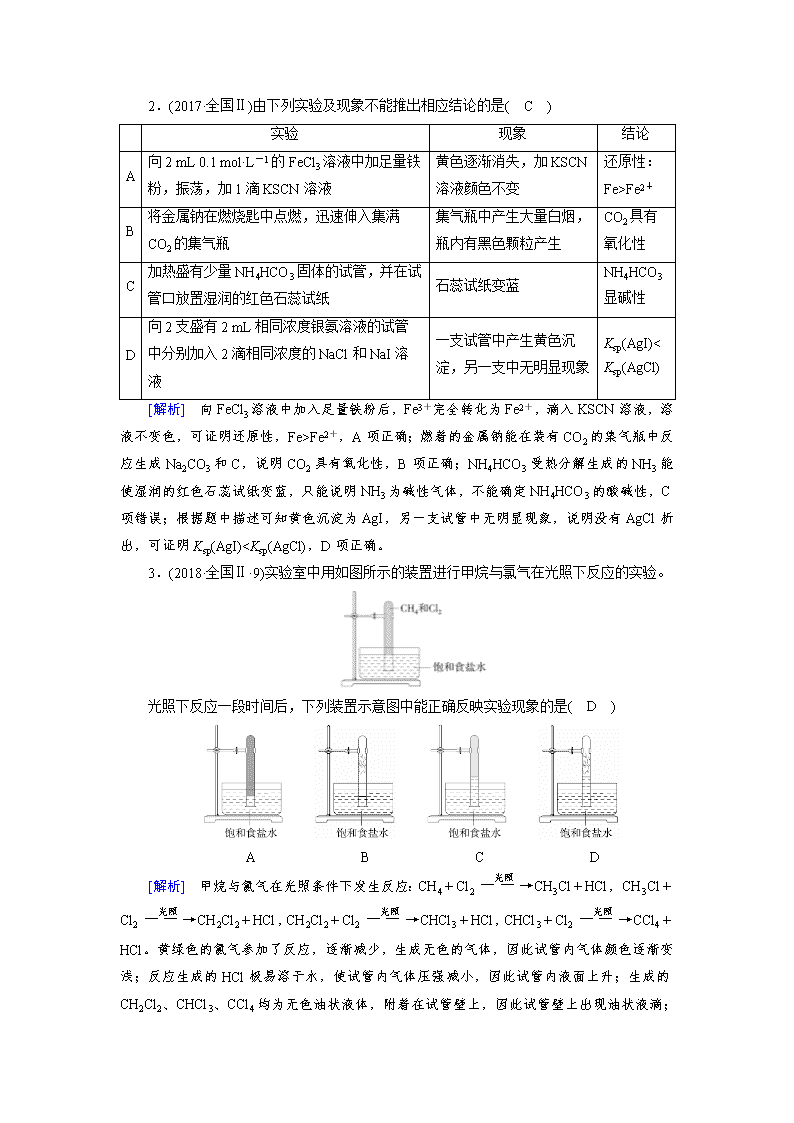
2.(2017·全国Ⅱ)由下列实验及现象不能推出相应结论的是( C )
实验
现象
结论
A
向2 mL 0.1 mol·L-1的FeCl3溶液中加足量铁粉,振荡,加1滴KSCN溶液
黄色逐渐消失,加KSCN溶液颜色不变
还原性:Fe>Fe2+
B
将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶
集气瓶中产生大量白烟,瓶内有黑色颗粒产生
CO2具有氧化性
C
加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸
石蕊试纸变蓝
NH4HCO3显碱性
D
向2支盛有2 mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液
一支试管中产生黄色沉淀,另一支中无明显现象
Ksp(AgI)
Fe2+,A项正确;燃着的金属钠能在装有CO2的集气瓶中反应生成Na2CO3和C,说明CO2具有氧化性,B项正确;NH4HCO3受热分解生成的NH3能使湿润的红色石蕊试纸变蓝,只能说明NH3为碱性气体,不能确定NH4HCO3的酸碱性,C项错误;根据题中描述可知黄色沉淀为AgI,另一支试管中无明显现象,说明没有AgCl析出,可证明Ksp(AgI)I2
3.某化学兴趣小组欲制备并探究SO2的某些性质。
【SO2的制备】用亚硫酸钠与较浓的硫酸反应制备SO2的装置图如上图(夹持仪器省略):
(1)图中装置有一处错误是_集气瓶C中导管长短反了__;
B中发生反应的化学方程式为 Na2SO3+H2SO4===Na2SO4+H2O+SO2↑ ;D的作用是_吸收尾气中的SO2,防止污染环境__。
【SO2的性质】探究SO2气体性质的装置如图所示:
(2)装置Ⅰ中的现象是_有浅黄色沉淀生成__,说明SO2具有_氧化__(填“氧化”或“还原”)性。装置Ⅰ中通入足量SO2发生反应的离子方程式为 2S2-+5SO2+2H2O===3S↓+4HSO 。
(3)在上述装置中通入过量的SO2,为了验证Ⅱ中发生了氧化还原反应,取Ⅱ中溶液分成两份,并设计了如下实验:
方案一:往第一份试液中加入少量酸性KMnO4溶液紫红色褪去。方案二:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是_方案一__,原因是_SO2过量,SO2可使酸性KMnO4溶液褪色__,写出解释该原因的离子方程式: 5SO2+2MnO+2H2O===5SO+2Mn2++4H+ 。
(4)SO2可以用来制备硫代硫酸钠,硫代硫酸钠可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。实验室可通过Na2S、Na2CO3和SO2共同反应来制取Na2S2O3。写出如图所示装置中三颈烧瓶中反应制取Na2S2O3的化学方程式: 2Na2S+Na2CO3+4SO2===3Na2S2O3
+CO2 。
[解析] (1)SO2的密度大于空气,即错误在于集气瓶C中导管长短反了。反应的化学方程式为Na2SO3+H2SO4===Na2SO4+H2O+SO2↑。SO2是大气污染物,需要尾气处理,则D中氢氧化钠溶液的作用是吸收尾气中的SO2,防止污染环境。
(2)SO2具有氧化性,能把硫化钠氧化为单质S,装置Ⅰ中有浅黄色沉淀生成;如果通入足量的SO2,则反应的离子方程式为2S2-+5SO2+2H2O===3S↓+4HSO。
(3)如果SO2过量,则SO2可使酸性KMnO4溶液褪色,不能说明有亚铁离子生成,所以方案一不合理,有关反应的离子方程式为5SO2+2MnO+2H2O===5SO+2Mn2++4H+。
(4)反应物是Na2S、Na2CO3和SO2,生成物是硫代硫酸钠,根据原子守恒可知还有CO2生成,则反应的方程式为2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2。
考点二 有机物制备与提纯实验方案设计
Z (课前)
1.(2018·青岛一模)正丁醇中混有少量正丁醛,设计如下提纯路线:
已知:①正丁醇和正丁醛(CH3CH2CH2CHO)常温为液体;
②CH3CH2CH2CHO+NaHSO3(饱和)―→CH3CH2CH2CH(OH)SO3Na↓。
下列说法不正确的是( C )
A.操作(1)需要过滤装置
B.操作(2)需要用到分液漏斗
C.操作(3)需要用到蒸发皿
D.操作(4)需要蒸馏装置
2.(2018·全国Ⅰ·9)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是( D )
A B C D
[解析] A是生成乙酸乙酯的操作,B是收集乙酸乙酯的操作,C是分离乙酸乙酯的操作。D是蒸发操作,在生成和纯化乙酸乙酯的实验过程中未涉及。
3.(2017·江苏)[实验化学]1-溴丙烷是一种重要的有机合成中间体,沸点为71 ℃,密度为1.36 g·cm-3。实验室制备少量1-溴丙烷的主要步骤如下:
步骤1:在仪器A中加入搅拌磁子、12 g正丙醇及20 mL水,冰水冷却下缓慢加入28 mL浓H2SO4;冷却至室温,搅拌下加入24 g NaBr。
步骤2:如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12 mL H2O、12 mL 5% Na2CO3溶液和12 mL H2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。
(1)仪器A的名称是_蒸馏烧瓶__;加入搅拌磁子的目的是搅拌和_防止暴沸__。
(2)反应时生成的主要有机副产物有2-溴丙烷和_丙烯、正丙醚__。
(3)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是_减少1-溴丙烷的挥发__。
(4)步骤2中需缓慢加热使反应和蒸馏平稳进行,目的是_减少HBr挥发__。
(5)步骤4中用5% Na2CO3溶液洗涤有机相的操作:向分液漏斗中小心加入12 mL 5% Na2CO3溶液,振荡,_将分液漏斗下口向上倾斜、打开活塞排出气体__,静置,分液。
[解析] 本题考查1-溴丙烷的制备实验,涉及仪器的识别、实验基本操作、实验原理的分析。(1)仪器A为蒸馏烧瓶,搅拌磁子的作用是搅拌和防止暴沸。(2)反应物中的正丙醇可能发生消去反应生成丙烯,也可能发生分子间脱水反应生成正丙醚。(3)向接收瓶内加入少量冰水并置于冰水浴中,降低了接收瓶内的温度,减少了1-溴丙烷的挥发。(4)HBr易挥发,故需缓慢加热。(5)振荡后,要排出分液漏斗中的气体。
R (课堂)
知能补漏
1.有机制备与分离提纯的思维流程:
—
↓
—
↓
—
↓
—
2.有机物制备实验中常用的仪器:
(1)制备装置。
(2)蒸馏装置。
3.有机混合物的分离提纯常用方法:
方法
适用条件
实例
说明
萃取
互不相溶的液体混合物
分离CCl4和水等
分液时下层液体从下口流出,上层液体从上口倒出
蒸馏
两种或两种以上互溶的液体,沸点相差较大
分离酒精和水
在蒸馏烧瓶中放少量碎瓷片,防止液体暴沸
4.有机物制备的解题流程
有机物的制备是中学化学实验的重要组成部分,以新物质制备为背景的实验图,涉及知识面广、题型多变、思维发散空间大,能很好的考查学生综合运用化学实验基础知识解决实际问题的能力,因而倍受高考命题者的青睐。解答此类试题的一般流程是:
第一步,明确实验目的。通过分析合成目标产物的有机反应方程式确定反应原理,分析反应的特点(如可逆反应等),并分析可能发生的副反应。
第二步,确定实验装置。依据反应物状态及反应条件选择合适的反应容器,并控制合适的反应温度。根据反应原理及装置特点,确定每个装置的作用。
第三步,设计除杂方案。根据产品和杂质的性质差异(如溶解性、熔沸点、密度大小、物质的状态等)选择合适的分离提纯方法。根据有机反应中反应物的挥发性及有机副反应较多的特点,分析除杂步骤、试剂及除杂装置。
第四步,产品产率(纯度)计算。根据题目提供的反应原理和试剂的用量,利用有机反应方程式或关系式,计算产品的理论产量,则产品产率为×100%。
B (课后)
1.冬青油是一种无色液体,某实验小组利用如图所示的装置制备冬青油。化学反应原理和实验装置如下所示:
产物的有关数据如表所示:
相对分子质量
密度/g·cm-3
沸点/℃
溶解性
冬青油
152
1.180
222.2
微溶于水
实验步骤如下所示:
①向三颈瓶中加入6.9 g (0.05 mol)水杨酸和24 g (0.75 mol)甲醇,再小心地加入6 mL浓硫酸,摇匀。②加入2粒沸石(或碎瓷片),装上仪器a,在石棉网上保持温度在85~95 ℃,回流1.5 h。③反应完毕,将烧瓶冷却,加入50 mL蒸馏水,然后转移至分液漏斗,弃去水层,将有机层再倒入分液漏斗中,依次用50 mL 5%碳酸氢钠溶液和30 mL水洗涤。④将产物移至干燥的锥形瓶中,加入0.5 g无水氯化钙。⑤最后将粗产品进行蒸馏,收集221~224 ℃的馏分,其质量为6.8 g。
请回答下列问题:
(1)本实验中浓硫酸的作用是_催化剂、吸水剂__。
(2)装置中仪器a的名称是_球形冷凝管__,进水口为
_Ⅰ__(填“Ⅰ”或“Ⅱ”)。温度计的适宜规格为_②__(填代号)。
①50 ℃ ②100 ℃ ③300 ℃
(3)用碳酸氢钠溶液洗涤的目的是_除去水杨酸和硫酸__;用水洗涤时,产品在_下__(填“上”或“下”)层。
(4)加入无水氯化钙的目的是_除去粗产品中的水分__。
(5)本次实验中冬青油的产率为_89.5%__。
2.(2017·石家庄模拟)实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OHCH2===CH2↑+H2O
CH2===CH2+Br2―→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140 ℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
乙醇
1,2-二溴乙烷
乙醚
状态
无色液体
无色液体
无色液体
密度/g·cm-3
0.79
2.2
0.71
沸点/℃
78.5
132
34.6
熔点/℃
-130
9
-116
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要的目的是_d__(填正确选项前的字母);
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入_c__(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体;
a.水 b.浓硫酸
c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是_溴的颜色完全褪去__;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_下__层(填“上”或“下”);
(5)若产物中有少量未反应的Br2,最好用_b__(填正确选项前的字母)洗涤除去;
a.水 b.氢氧化钠溶液
c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用_蒸馏__的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是_避免溴大量挥发__;但又不能过度冷却(如用冰水),其原因是_1,2-二溴乙烷的熔点低,过度冷却会凝固而堵塞导管__。
[解析] (2)根据题中提示,选碱来吸收酸性气体;(3)制备反应是溴与乙烯的反应,明显的现象是溴的颜色褪去;(4)1,2-二溴乙烷的密度大于水,因而在下层;(5)溴在水中溶解度小,不能用水,碘化钠与溴反应生成碘会溶解在1,2-二溴乙烷中,不能用碘化钠溶液除溴,乙醇与1,2-二溴乙烷混溶也不能用;(6)根据表中数据,乙醚沸点低,可通过蒸馏除去(不能用蒸发,乙醚不能散发到空气中,且蒸发会导致1,2-二溴乙烷挥发到空气中);(7)溴易挥发,冷却可减少挥发。但如果用冰水冷却会使产品凝固而堵塞导管。
3.(2018·潍坊联考)实验室制备硝基苯的反应原理和实验装置如图所示:
+HO—NO2+H2O ΔH<0
存在的主要副反应有在温度稍高的情况下会生成间二硝基苯。
有关数据如表所示:
物质
熔点/℃
沸点/℃
密度/g·cm-3
溶解性
苯
5.5
80
0.88
微溶于水
硝基苯
5.7
210.9
1.205
难溶于水
间二硝基苯
89
301
1.57
微溶于水
浓硝酸
83
1.4
易溶于水
浓硫酸
338
1.84
易溶于水
实验步骤如下:
取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合酸,将混合酸小心加入B中。把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀。在50~60 ℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210 ℃馏分,得到纯硝基苯18 g。
回答下列问题:
(1)装置B的名称是_分液漏斗__,装置C的作用是_冷凝回流__。
(2)配制混合酸时,能否将浓硝酸加入浓硫酸中,说明理由:_不能,易发生酸液迸溅__。
(3)为了使反应在50~60 ℃下进行,常用的方法是_水浴加热__。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是_溶有浓硝酸分解产生的NO2(或硝酸)等杂质__。
(4)在洗涤操作中,第二次水洗的作用是_洗去残留的NaOH及生成的钠盐等可溶性杂质__。
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140 ℃,应选用空气冷凝管,不选用水直形冷凝管的原因是_以免直形冷凝管通水冷却时因玻璃管内外温差大而炸裂__。
(6)本实验所得到的硝基苯产率是_72%__。
[解析] (1)装置B的名称是分液漏斗,装置C的作用是冷凝回流。
(2)不能,因为硝酸的密度比硫酸小,将浓硝酸加入浓硫酸易发生酸液迸溅。
(3)水浴加热可以控制温度在50~60 ℃。粗硝基苯呈黄色的原因是溶有浓硝酸分解产生的NO2等杂质。
(4)第二次水洗可以除去氢氧化钠及钠盐等可溶性杂质。
(5)用直形冷凝管可能因为内外温差过大而炸裂。
(6)理论上产生硝基苯的质量=×123 g·mol-1≈25 g,则硝基苯的产率=18÷25×100%=72%。
考点三 定量测定实验
Z (课前)
1.(2016·天津)水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg·L-1。我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5 mg·L-1。某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO。
Ⅰ.测定原理:
碱性条件下,O2将Mn2+氧化为MnO(OH)2;
①2Mn2++O2+4OH-===2MnO(OH)2↓
酸性条件下,MnO(OH)2将I-氧化为I2;
②MnO(OH)2+I-+H+―→Mn2++I2+H2O(未配平)
用Na2S2O3标准溶液滴定生成的I2;
③2S2O+I2===S4O+2I-
Ⅱ.测定步骤:
a.安装装置,检验气密性,充N2排尽空气后,停止充N2。
b.向烧瓶中加入200 mL水样。
c.向烧瓶中依次迅速加入1 mL MnSO4无氧溶液(过量)、2 mL碱性KI无氧溶液(过量),开启搅拌器,至反应①完全。
d.搅拌并向烧瓶中加入2 mL H2SO4无氧溶液,至反应②完全,溶液为中性或弱酸性。
e.从烧瓶中取出40.00 mL溶液,以淀粉作指示剂,用0.01000 mol·L-1 Na2S2O3溶解进行滴定,记录数据。
f.……
g.处理数据(忽略氧气从水样中的逸出量和加入试剂后水样体积的变化)。
回答下列问题:
(1)配制以上无氧溶液时,除去所用溶剂水中氧的简单操作为_将溶剂水煮沸后冷却__。
(2)在橡胶塞处加入水样及有关试剂应选择的仪器是
_②__。
①滴定管 ②注射器 ③量筒
(3)搅拌的作用是_使溶液混合均匀,快速完成反应__。
(4)配平反应②的方程式,其化学计量数依次为_1,2,4,1,1,3__。
(5)步骤f为_重复步骤e的操作2-3次__。
(6)步骤e中达到滴定终点的标志为_溶液蓝色褪去(半分钟内不恢复颜色)__。若某次滴定消耗Na2S2O3溶液4.50 mL,水样的DO=_9.0__ mg·L-1(保留一位小数)。作为饮用水源,此次测得DO是否达标:_是__(填“是”或“否”)。
(7)步骤d中加入H2SO4溶液反应后,若溶液pH过低,滴定时会产生明显的误差。写出产生此误差的原因(用离子方程式表示,至少写出2个) 2H++S2O===S↓+SO2↑+H2O 、 S
O2+I2+2H2O===4H++SO+2I- 。
2.(2017·全国Ⅰ·26)凯氏定氮法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。已知:NH3+H3BO3===NH3·H3BO3;NH3·H3BO3+HCl===NH4Cl+H3BO3。
回答下列问题:
(1)a的作用是_避免b中压强过大__。
(2)b中放入少量碎瓷片的目的是_防止暴沸__。f的名称是_直形冷凝管__。
(3)清洗仪器:g中加蒸馏水:打开k1,关闭k2、k3,加热b,蒸气充满管路:停止加热,关闭k1,g中蒸馏水倒吸进入c,原因是_c中温度下降,管路中形成负压__;打开k2放掉水。重复操作2~3次。
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂,铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭k3,d中保留少量水,打开k1,加热b,使水蒸气进入e。
①d中保留少量水的目的是_液封,防止氨气逸出__。
②e中主要反应的离子方程式为 NH+OH-NH3↑+H2O ,e采用中空双层玻璃瓶的作用是_保温使氨完全蒸出__。
(5)取某甘氨酸(C2H5NO2)样品m克进行测定,滴定g中吸收液时消耗浓度为c mol·L-1的盐酸V mL,则样品中氮的质量分数为 %,样品的纯度≤ %。
[解析] (1)导管a与大气相通,其作用是避免烧瓶内气压过大,发生危险。(2)加热液体时加入碎瓷片,其作用是防止液体暴沸。冷凝管有直形冷凝管和球形冷凝管等,要指明。(3)停止加热,瓶内水蒸气冷凝,气体压强减小,会引起g中液体倒吸入c中,利用蒸馏水倒吸来洗涤仪器e、f。(4)①止水夹k3处可能漏气,导致测定的N元素质量分数偏低,故d中保留少量水起液封作用,防止氨气逸出。②e中发生的主要反应是铵盐与氢氧化钠反应,需要加热,使氨气全部逸出。“中空双层玻璃瓶”考生比较陌生,可以联想平时生活中保温玻璃瓶来分析问题。(5)n(N)=n(NH3)=n(HCl)=mol,w(N)=×100%=%。C2H5NO2的相对分子质量为75,w(C2H5NO2)=%×=%。
3.(2018·天津·9)烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。回答下列问题:
Ⅰ.采样
采样系统简图
采样步骤:
①检验系统气密性;②加热器将烟道气加热至140 ℃;③打开抽气泵置换系统内空气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。
(1)A中装有无碱玻璃棉,其作用为_除尘__。
(2)C中填充的干燥剂是(填序号)_c__。
a.碱石灰 b.无水CuSO4 c.P2O5
(3)用实验室常用仪器组装一套装置,其作用与D(装有碱液)相同,在虚线框中画出该装置的示意图,标明气体的流向及试剂。
(4)采样步骤②加热烟道气的目的是_防止NOx溶于冷凝水__。
Ⅱ.NOx含量的测定
将v L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化成NO,加水稀释至100.00 mL。量取20.00 mL该溶液,加入v1 mL c1 mol·L-1FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。
(5)NO被H2O2氧化为NO的离子方程式为 2NO+3H2O2===2H++2NO+2H2O 。
(6)滴定操作使用的玻璃仪器主要有_锥形瓶、酸式滴定管__。
(7)滴定过程中发生下列反应:
3Fe2++NO+4H+===NO↑+3Fe3++2H2O
Cr2O+6Fe2++14H+===2Cr3++6Fe3++7H2O
则气样中NOx折合成NO2的含量为 ×104 mg·m-3。
(8)判断下列情况对NOx含量测定结果的影响(填“偏高”“偏低”或“无影响”)。
若缺少采样步骤③,会使测定结果_偏低__。
若FeSO4标准溶液部分变质,会使测定结果_偏高__。
[解析] (1)装置A是过滤器,装有无碱玻璃棉的作用是过滤除去粉尘。
(2)C中填充的是干燥剂,除去H2O且不能与NOx反应,所以应选有酸性、干燥能力强的P2O5。
(3)D装置中装有碱液,用于除去NOx,作用与实验室中的洗气瓶相同,该装置的示意图为。
(4)烟道气中有水,采样步骤②加热器将烟道气加热至140 ℃的目的是防止NOx溶于冷凝水。
(5)NO被H2O2氧化为NO,H2O2的还原产物为H2O,离子方程式为2NO+3H2O2===2H++2NO+2H2O。
(6)滴定操作使用的玻璃仪器主要有锥形瓶、滴定管,因为该滴定液呈酸性,所以选用酸式滴定管。
(7)滴定过程中发生下列反应:
3Fe2++NO+4H+===NO↑+3Fe3++2H2O
Cr2O+6Fe2++14H+===2Cr3++6Fe3++7H2O
与Cr2O反应的Fe2+的物质的量为6c2v2×10-3 mol,标准液中Fe2+的物质的量为c1v1×10-3 mol,则与NO反应的Fe2+的物质的量为(c1v1-6c2v2)×10-3 mol,NO的物质的量为 mol,则v L气样中折合成NO2的含量为 mol×46 g·mol-1××1 000 mg·g-1×1 000 L·m-3=×104 mg·m-3。
(8)若缺少采样步骤③,系统内存在空气,会使收集的气样中NOx偏少,测定结果偏低。若FeSO4标准溶液部分变质,溶液中的Fe2+浓度减小,消耗的FeSO4标准溶液体积增大,会使测定结果偏高。
R (课堂)
知能补漏
定量实验测量的方法
1.测量沉淀质量法:
先将某种成分转化为沉淀,然后称量过滤、洗涤、干燥后沉淀的质量再进行相关计算。
称量固体一般用托盘天平,精确度为0.1 g,但精确度高的实验中可使用分析天平或电子天平,可精确到0.000 1 g。
2.测量气体体积法:
(1)量气装置的设计:
下列装置中,A是常规的量气装置,B、C、D是改进后的装置。
(2)读数时先要将其恢复室温后,再调整量气装置使两侧液面相平,最后读数要求视线与凹液面最低点相平。
3.测量气体质量法:
一般有两种方法:一种方法是称反应装置在放出气体前后的质量减小值;另一种方法是称吸收装置前后的质量增大值。
4.滴定法:
即利用滴定操作原理,通过酸碱中和滴定、沉淀滴定和氧化还原反应滴定等获得相应数据后再进行相关计算。
B (课后)
1.为精准测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W0 g样品进行实验,下列实验方法所对应的实验方案和测量数据最合理(除W0外)的是( A )
选项
实验方法
实验方案
测量数据
A
滴定法
将样品配成100 mL溶液,取10 mL,加入甲基橙,用标准盐酸滴定
消耗盐酸的体积
B
量气法
将样品与盐酸反应,生成的气体全部被碱石灰吸收
碱石灰增重的质量
C
重量法
样品放入烧瓶中,置于天平上,加入足量盐酸
减轻的质量
D
量气法
将样品与盐酸反应,气体通过排水量气装置量气
排水体积
2.青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157 ℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35 ℃,从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺如图所示:
(1)对青蒿进行干燥破碎的目的是_增大青蒿与乙醚的接触面积,提高青蒿素的浸取率__。
(2)操作Ⅰ需要的玻璃仪器主要有烧杯、_漏斗、玻璃棒__,操作Ⅱ的名称是_蒸馏__。
(3)操作Ⅲ的主要过程可能是_B__(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2 g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
①装置A、E、F中盛放的物质分别是_NaOH溶液__、_CaCl2(或P2O5)__、_碱石灰__。
②G的作用是_防止空气中的CO2和水蒸气进入F装置__。
③
装置
实验前/g
实验后/g
E
22.6
42.4
F
80.2
146.2
则测得青蒿素的最简式是_C15H22O5__,欲确定其分子式,则还需要的物理量为_相对分子质量或摩尔质量__。
3.(2017·天津)用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.2468 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100 mL 0.1000 mol·L-1 NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.1000 mol·L-1 AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000 mol·L-1 NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号
1
2
3
消耗NH4SCN标准溶液体积/mL
10.24
10.02
9.98
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有_250mL(棕色)容量瓶、胶头滴管__。
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是_AgNO3见光分解__。
(3)滴定应在pH<0.5的条件下进行,其目的是_防止因Fe3+的水解而影响滴定终点的判断(或抑制Fe3+的水解)__。
(4)b和c两步操作是否可以颠倒_否__,说明理由_若颠倒,Fe3+与I-反应,指示剂耗尽,无法判断滴定终点__。
(5)所消耗的NH4SCN标准溶液平均体积为_10.00__ mL,测得c(I-)=_0.060_0__ mol·L-1。
(6)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为_用NH4SCN标准溶液进行润洗__。
(7)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果_偏高__。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果_偏高__。
[解析] 本题考查沉淀滴定法测定NaI溶液中c(I-)。(1)配制一定物质的量浓度的标准溶液,除烧杯和玻璃棒外,还需用到的仪器有250mL(棕色)容量瓶、胶头滴管。(2)AgNO3见光容易分解,因此需要保存在棕色试剂瓶中。(3)滴定实验中用NH4Fe(SO4)2溶液作指示剂,Fe3+容易发生水解,影响滴定终点判断,因此控制pH<0.5,目的是抑制Fe3+的水解。(4)Fe3+能与I-发生氧化还原反应:2Fe3++2I-===2Fe2++I2,因此b、c不能颠倒,否则指示剂耗尽,无法判断滴定终点。(5)第1组数据误差较大,舍去,取第2组、第3组实验数据的平均值,消耗NH4SCN标准溶液的体积为(10.02+9.98)mL×=10.00mL。根据滴定原理,则n(Ag+)=n(I-)+n(SCN-),故n(I-)=n(Ag+)-n(SCN-)=0.025L×0.1000 mol·L-1-0.01L×0.1000 mol·L-1=0.001 5 mol,则c(I-)==0.0600 mol·L-1。(6)在滴定管中装入NH4SCN标准溶液之前,要先用NH4SCN标准溶液润洗滴定管。(7)①配制AgNO3标准溶液时,若烧杯中溶液有少量溅出,配制的AgNO3标准溶液的浓度偏低,则滴定时消耗的NH4SCN标准溶液的体积偏小,测得的c(I-)偏高。②滴定管0
刻度在上,读数时从上往下读数,读取体积偏小,计算所用NH4SCN的物质的量偏低,测得的c(I-)偏高。