- 2022-08-18 发布 |
- 37.5 KB |
- 3页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
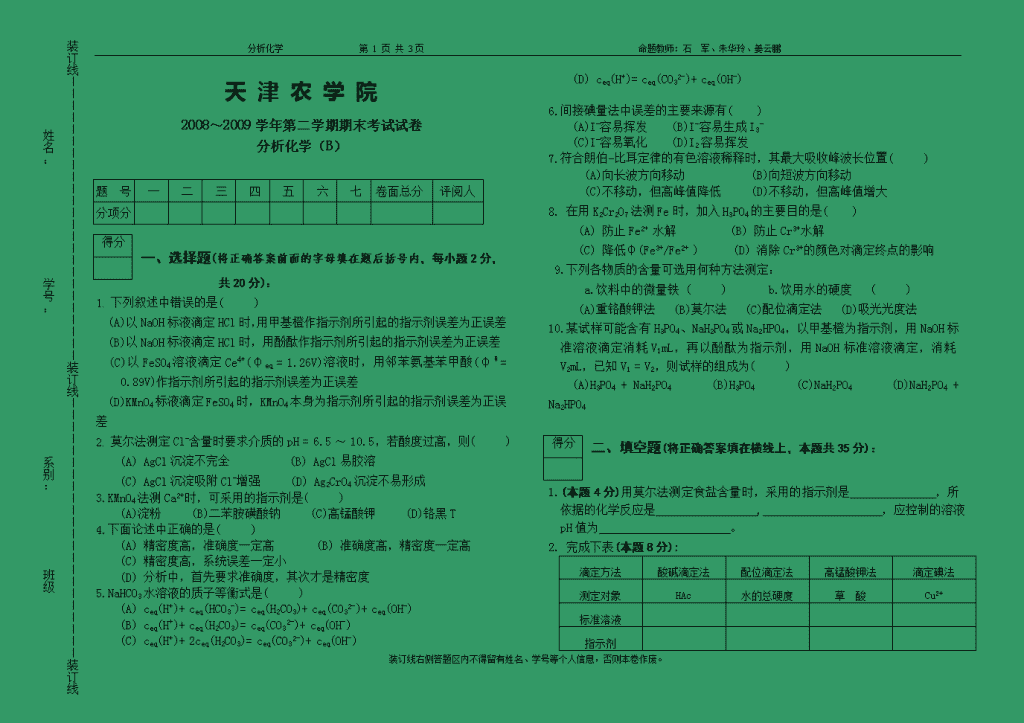
天津农学院农分析化学试卷B
分析化学第3页共3页命题教师:石军、朱华玲、姜云鹏装订线————————————————————————装订线——————————————————————装订线姓名:学号:系别:班级天津农学院2008~2009学年第二学期期末考试试卷分析化学(B)题号一二三四五六七卷面总分评阅人分项分得分一、选择题(将正确答案前面的字母填在题后括号内,每小题2分,共20分):1.下列叙述中错误的是( )(A)以NaOH标液滴定HCl时,用甲基橙作指示剂所引起的指示剂误差为正误差(B)以NaOH标液滴定HCl时,用酚酞作指示剂所引起的指示剂误差为正误差(C)以FeSO4溶液滴定Ce4+(φeq=1.26V)溶液时,用邻苯氨基苯甲酸(φθ=0.89V)作指示剂所引起的指示剂误差为正误差(D)KMnO4标液滴定FeSO4时,KMnO4本身为指示剂所引起的指示剂误差为正误差2.莫尔法测定Cl-含量时要求介质的pH=6.5~10.5,若酸度过高,则( )(A)AgCl沉淀不完全(B)AgCl易胶溶(C)AgCl沉淀吸附Cl-增强(D)Ag2CrO4沉淀不易形成3.KMnO4法测Ca2+时,可采用的指示剂是()(A)淀粉(B)二苯胺磺酸钠(C)高锰酸钾(D)铬黑T4.下面论述中正确的是()(A)精密度高,准确度一定高(B)准确度高,精密度一定高(C)精密度高,系统误差一定小(D)分析中,首先要求准确度,其次才是精密度5.NaHCO3水溶液的质子等衡式是( )(A)ceq(H+)+ceq(HCO3-)=ceq(H2CO3)+ceq(CO32-)+ceq(OH-)(B)ceq(H+)+ceq(H2CO3)=ceq(CO32-)+ceq(OH-)(C)ceq(H+)+2ceq(H2CO3)=ceq(CO32-)+ceq(OH-)(D)ceq(H+)=ceq(CO32-)+ceq(OH-)6.间接碘量法中误差的主要来源有()(A)I-容易挥发(B)I-容易生成I3-(C)I-容易氧化(D)I2容易挥发7.符合朗伯-比耳定律的有色溶液稀释时,其最大吸收峰波长位置( )(A)向长波方向移动(B)向短波方向移动(C)不移动,但高峰值降低(D)不移动,但高峰值增大8.在用K2Cr2O7法测Fe时,加入H3PO4的主要目的是() (A)防止Fe2+水解(B)防止Cr3+水解(C)降低φ(Fe3+/Fe2+)(D)消除Cr3+的颜色对滴定终点的影响9.下列各物质的含量可选用何种方法测定:a.饮料中的微量铁()b.饮用水的硬度 ( )(A)重铬酸钾法 (B)莫尔法 (C)配位滴定法 (D)吸光光度法10.某试样可能含有H3PO4、NaH2PO4或Na2HPO4,以甲基橙为指示剂,用NaOH标准溶液滴定消耗V1mL,再以酚酞为指示剂,用NaOH标准溶液滴定,消耗V2mL,已知V1=V2,则试样的组成为( )(A)H3PO4+NaH2PO4(B)H3PO4(C)NaH2PO4(D)NaH2PO4+Na2HPO4得分二、填空题(将正确答案填在横线上,本题共35分):1.(本题4分)用莫尔法测定食盐含量时,采用的指示剂是,所依据的化学反应是,,应控制的溶液pH值为。2.完成下表(本题8分):滴定方法酸碱滴定法配位滴定法高锰酸钾法滴定碘法测定对象HAc水的总硬度草酸Cu2+标准溶液指示剂装订线右侧答题区内不得留有姓名、学号等个人信息,否则本卷作废。\n分析化学第3页共3页命题教师:石军、朱华玲、姜云鹏3.(本题2分)吸光度随入射光波长变化的曲线叫;吸光度随溶液浓度变化的曲线称为。4.(本题2分)用KMnO4法测定还原性物质,一般要在强酸介质中进行,是因为:_____________________________________________________________。5.(本题2分)在HCl介质中,用KMnO4标准溶液测定Fe2+时,由于__________效应,而使测定结果____________________。6.(本题4分)基准物质应具备的条件是:、、、。7.(本题5分)在吸光光度分析中,为了提高测定的准确度和灵敏度,一般应选择_________________波长的入射光照射待测溶液,并控制吸光度A值在________________范围,透光率T值在________________范围内最佳。为此,可采用和的方法来调节A和T的大小。。8.(本题4分)常用于标定HCl溶液浓度的基准物质有和;常用于标定EDTA溶液浓度的基准物质有和。9.(本题2分)滴定分析的误差主要决定于误差和误差。10.(本题2分)间接碘量法测Cu2+时,滴定至近计量点时,加入KSCN的目的是。得分三、判断题(正确者划“√”;错误者划“×”并改正之,每题2分,共10分):1.配位滴定法中,须使溶液的酸度比测定该离子所允许的最高酸度高。()2.0.1mol•L-1的HCl溶液能滴定0.1mol•L-1的NaAc溶液,是因为Kθ(HAc)=1.8×10-5,满足C·Kθa≥10-8。()3.pH=3.05是一个三位有效数字。()4.标定KMnO4可采用的基准物质为Na2C2O4或Na2B2O7·10H2O。()5.以AgNO3标准溶液滴定NaCl时,K2CrO4多加了一些,则产生负误差。()得分四、计算题(本题共9分):用吸光光度法测定试样中含铁量。吸取5.00mL试样稀释至250.0mL,然后吸取此稀释液2.00mL置于50.0mL的容量瓶中定容,测得吸光度A=0.550,求试样中铁的含量为多少g•L-1?[已知:显色时,标准溶液浓度为5.0mg•L-1吸光度A=0.480,显色条件与试液显色条件相同。]得分五、计算题(本题共9分):为了测定冰晶石(Na3AlF6)矿样中F的含量,称取试样1.5240g,溶解后定容至100.0mL,移取25.00mL,加入0.2000mol•L-1Ca2+离子溶液25mL,使生成CaF2沉淀,经过滤收集滤液和洗涤液,调pH为10,以钙指示剂指示终点,用0.01240mol•L-1EDTA滴定,消耗20.17mL。求冰晶石中F的含量。[已知:M(F)=19.00]装订线右侧答题区内不得留有姓名、学号等个人信息,否则本卷作废。\n分析化学第3页共3页命题教师:石军、朱华玲、姜云鹏得分六、计算题(本题共9分):称取含砷试样0.5000g,溶解后在弱碱性介质中使砷处理为AsO43-,然后沉淀为Ag3AsO4,将沉淀过滤、洗涤,溶于酸中。以0.1000mol•L-1NH4SCN溶液滴定其中的Ag+至终点,消耗45.45 mL。计算试样中砷的含量。相关化学反应为:AsO43-+3Ag+=Ag3AsO4↓Ag3AsO4+3HNO3=3AgNO3+H3AsO4Ag++NH4SCN=AgSCN↓+NH4+。得分七、计算题(本题共8分):100.26mLKMnO4溶液所氧化的H2C2O4·H2O的质量需用43.42mL0.3010mol·L-1NaOH溶液中和,求c(KMnO4)=?(已知:K=39.00C=12.00O=16.00H=1.008Na=23.00Mn=54.90)装订线右侧答题区内不得留有姓名、学号等个人信息,否则本卷作废。查看更多