- 2022-08-16 发布 |
- 37.5 KB |
- 20页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
大学物理 量子物理基础
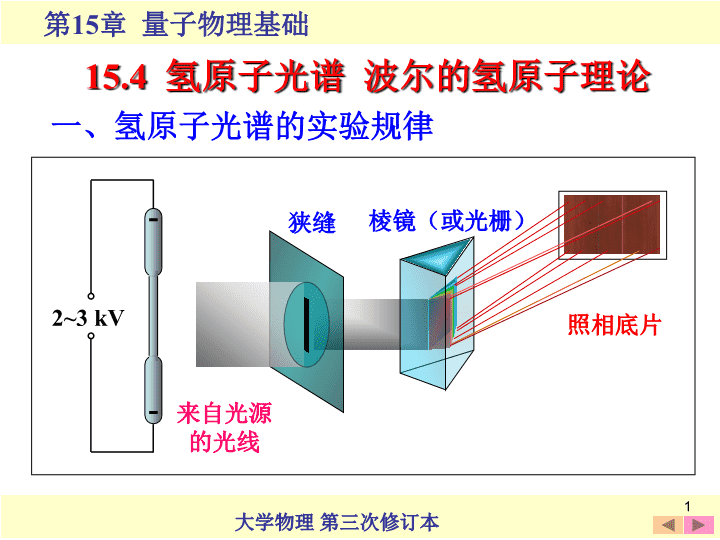
15.4氢原子光谱波尔的氢原子理论一、氢原子光谱的实验规律狭缝照相底片棱镜(或光栅)来自光源的光线2~3kV1\n氢原子光谱是最简单的光谱,对氢原子光谱的研究具有重要的意义。谱线特点1.从红光到紫光有一系列分立的谱线。2.每一条谱线的波数可以表示为爱因斯坦(Einstein)上式称为里德伯—里兹合并原则。氢光谱的里德伯常量。2\n(3)光谱中的谱线系。莱曼系(紫外线)巴耳末系(可见光)帕邢系(红外线)如何解释氢原子光谱的规律?3\n二、原子的经典模型1.汤姆孙的面包夹葡萄干模型整个原子呈胶冻状的球体,正电荷均匀分布于球体上,而电子镶嵌在原子球内,在各自的平衡位置附近做简谐振动,并发射同频率的电磁波。------------4\n2.卢瑟福的核式原子模型原子由原子核和核外电子构成,原子核带正电荷,占据整个原子的极小一部分空间,而电子带负电,绕着原子核转动,如同行星绕太阳转动一样。氢原子+e-e根据经典理论电子要不断向外辐射电磁波,能量逐渐减少,发射的光谱应该是连续的;随着能量的减少,电子将与核相遇。原子是一个不稳定的系统。5\n丹麦物理学家玻尔把卢瑟福的原子有核模型、普朗克量子假设、里德伯-里兹合并原则结合起来,于1913年创立了氢原子结构的半经典量子理论,使人们对原子结构的认识向前推进了一大步。N.Bohr6\n三、波尔的氢原子理论(1)定态假设原子只能处在一系列具有不连续能量的稳定状态,称为定态,相应于定态,核外电子在一系列不连续的稳定圆轨道上运动,但并不辐射电磁波。(2)跃迁假设当原子从一个能量为Ek的定态跃迁到另一个能量为En的定态时,会发射或吸收一个频率为νkn的光子:——辐射频率公式。1.基本假设7\n式中,称为约化普朗克常数,n为主量子数。(3)角动量量子化电子在稳定圆轨道上运动时,其轨道角动量L=mvr必须等于h/2π的整数倍,即——角动量量子化条件。8\n讨论(1)假设1是针对氢原子有核模型与经典电磁理论的矛盾而作出的。只有假定电子在圆轨道上运动时不辐射电磁波,才能保证原子的稳定性。(3)假设3指出电子绕核运动的圆轨道是有限制的。只有角动量满足量子化条件才是许可的,这是对普朗克能量量子化的进一步发展。(2)假设2是对普朗克假设的引伸,指出辐射光的条件。9\n2.氢原子能级计算电子以原子核为中心,做半径为r的圆周运动,向心力是库仑力:电子的定态轨道运动满足10\n联立两式,得氢原子处于第n个定态时电子的轨道半径为电子的最小轨道半径,称为玻尔半径。n=1的定态称为基态,n=2,3,4,…各态称为受激态。其中11\n氢原子各定态电子轨道n=1n=2n=3n=4r1r2=4r1r3=9r1r4=16r1赖曼系巴耳末系帕邢系12\n电子轨道运动的速度氢原子能量处在量子数为n的定态时的能量13\n氢原子基态的能量(n=1)基态能量最低,原子最稳定。随着量子数n增大,,能量En也增大,能级间隔减小,当n→∞时,En→0,能级趋于连续,原子处于电离状态,这时能量可连续变化。轨道、速度、能量都是量子化的。14\n莱曼系巴耳末系帕邢系布拉开系普丰德系-13.580-3.39-1.51-0.85-0.54En/eV12354氢原子能级图15\n氢原子光谱解释根据玻尔假设,当原子从高能态En向低能态Ek跃迁时,发射一个光子。频率波数16\n令里德伯常数的理论值与实验值符合的很好。公式与经验公式一致。当时实验测得17\n四、波尔理论的缺陷和意义玻尔量子论的缺陷在于量子化不彻底,他只对电子的径向运动采取了量子化,既对电子的轨道半径用量子化来处理,而对电子绕核运动则用经典力学处理,因此玻尔量子论是半经典的量子论。玻尔的量子论成功解释了氢原子光谱,在一定程度上反映了原子内部结构的规律性,并得到光谱实验和夫兰克—赫兹实验的证实,为后来的量子理论奠定了基础,玻尔由于出色的工作获得了1922年诺贝尔物理学奖。18\n例在基态,氢原子被外来单色光激发后发出的巴耳末线系中,观察到了波长较长的两条谱线。求两条谱线的波长和外来光的频率。解由于在巴耳末线系中观察到的是波长较长的两条谱线,因此只能是第3能级跃到第2能级和第4能级跃迁到第2能级产生的谱线。19\n外来单色光的频率必须满足所以20查看更多