- 2021-05-14 发布 |
- 37.5 KB |
- 8页
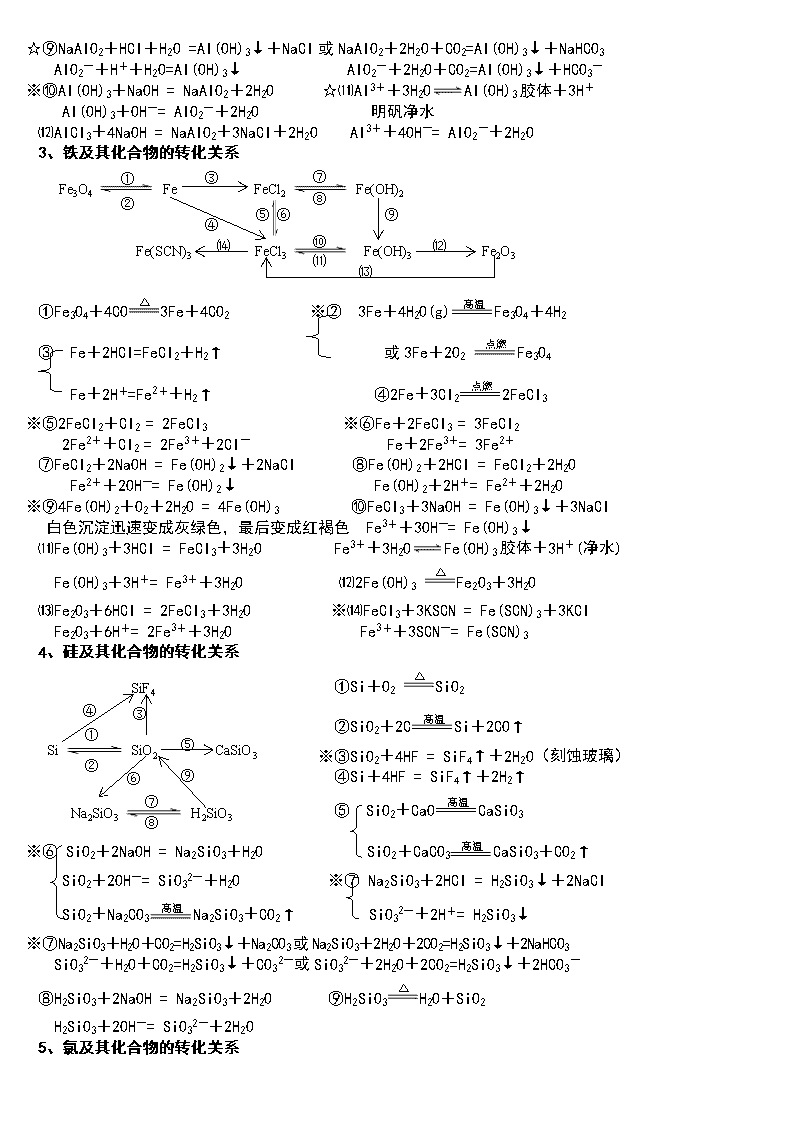

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
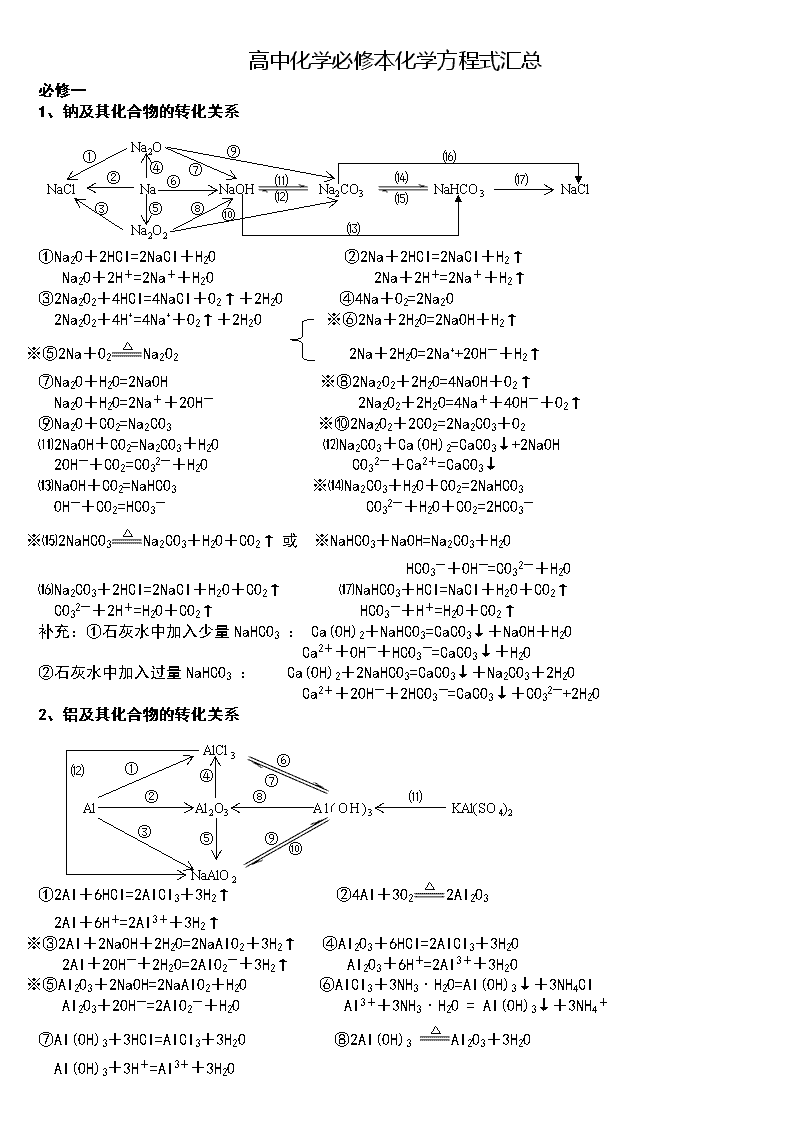
高考必备 元素及其化合物转化结构图
高中化学必修本化学方程式汇总 必修一 1、钠及其化合物的转化关系 NaCl Na NaOH Na2CO3 NaHCO3 NaCl Na2O Na2O2 ① ② ③ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩ ⑾ ⑿ ⒀ ⒁ ⒂ ⒃ ⒄ ④ ①Na2O+2HCl=2NaCl+H2O ②2Na+2HCl=2NaCl+H2↑ Na2O+2H+=2Na++H2O 2Na+2H+=2Na++H2↑ ③2Na2O2+4HCl=4NaCl+O2↑+2H2O ④4Na+O2=2Na2O 2Na2O2+4H+=4Na++O2↑+2H2O ※⑥2Na+2H2O=2NaOH+H2↑ ※⑤2Na+O2Na2O2 2Na+2H2O=2Na++2OH-+H2↑ ⑦Na2O+H2O=2NaOH ※⑧2Na2O2+2H2O=4NaOH+O2↑ Na2O+H2O=2Na++2OH- 2Na2O2+2H2O=4Na++4OH-+O2↑ ⑨Na2O+CO2=Na2CO3 ※⑩2Na2O2+2CO2=2Na2CO3+O2 ⑾2NaOH+CO2=Na2CO3+H2O ⑿Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 2OH-+CO2=CO32-+H2O CO32-+Ca2+=CaCO3↓ ⒀NaOH+CO2=NaHCO3 ※⒁Na2CO3+H2O+CO2=2NaHCO3 OH-+CO2=HCO3- CO32-+H2O+CO2=2HCO3- ※⒂2NaHCO3Na2CO3+H2O+CO2↑ 或 ※NaHCO3+NaOH=Na2CO3+H2O HCO3-+OH-=CO32-+H2O ⒃Na2CO3+2HCl=2NaCl+H2O+CO2↑ ⒄NaHCO3+HCl=NaCl+H2O+CO2↑ CO32-+2H+=H2O+CO2↑ HCO3-+H+=H2O+CO2↑ 补充:①石灰水中加入少量NaHCO3 : Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O Ca2++OH-+HCO3-=CaCO3↓+H2O ②石灰水中加入过量NaHCO3 : Ca(OH)2+2NaHCO3=CaCO3↓+Na2CO3+2H2O Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O 2、铝及其化合物的转化关系 Al Al2O3 Al(OH)3 KAl(SO4)2 NaAlO2 AlCl3 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩ ⑾ ⑿ ①2Al+6HCl=2AlCl3+3H2↑ ②4Al+3O22Al2O3 2Al+6H+=2Al3++3H2↑ ※③2Al+2NaOH+2H2O=2NaAlO2+3H2↑ ④Al2O3+6HCl=2AlCl3+3H2O 2Al+2OH-+2H2O=2AlO2-+3H2↑ Al2O3+6H+=2Al3++3H2O ※⑤Al2O3+2NaOH=2NaAlO2+H2O ⑥AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl Al2O3+2OH-=2AlO2-+H2O Al3++3NH3·H2O = Al(OH)3↓+3NH4+ ⑦Al(OH)3+3HCl=AlCl3+3H2O ⑧2Al(OH)3 Al2O3+3H2O Al(OH)3+3H+=Al3++3H2O ☆⑨NaAlO2+HCl+H2O =Al(OH)3↓+NaCl或NaAlO2+2H2O+CO2=Al(OH)3↓+NaHCO3 AlO2-+H++H2O=Al(OH)3↓ AlO2-+2H2O+CO2=Al(OH)3↓+HCO3- ※⑩Al(OH)3+NaOH = NaAlO2+2H2O ☆⑾Al3++3H2OAl(OH)3胶体+3H+ Al(OH)3+OH-= AlO2-+2H2O 明矾净水 ⑿AlCl3+4NaOH = NaAlO2+3NaCl+2H2O Al3++4OH-= AlO2-+2H2O 3、铁及其化合物的转化关系 Fe3O4 Fe FeCl2 Fe(OH)2 Fe(SCN)3 FeCl3 Fe(OH)3 Fe2O3 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩ ⑾ ⑿ ⒁ ⒀ ①Fe3O4+4CO3Fe+4CO2 ※② 3Fe+4H2O(g)Fe3O4+4H2 ③ Fe+2HCl=FeCl2+H2↑ 或3Fe+2O2 Fe3O4 Fe+2H+=Fe2++H2↑ ④2Fe+3Cl22FeCl3 ※⑤2FeCl2+Cl2 = 2FeCl3 ※⑥Fe+2FeCl3 = 3FeCl2 2Fe2++Cl2 = 2Fe3++2Cl- Fe+2Fe3+= 3Fe2+ ⑦FeCl2+2NaOH = Fe(OH)2↓+2NaCl ⑧Fe(OH)2+2HCl = FeCl2+2H2O Fe2++2OH-= Fe(OH)2↓ Fe(OH)2+2H+= Fe2++2H2O ※⑨4Fe(OH)2+O2+2H2O = 4Fe(OH)3 ⑩FeCl3+3NaOH = Fe(OH)3↓+3NaCl 白色沉淀迅速变成灰绿色,最后变成红褐色 Fe3++3OH-= Fe(OH)3↓ ⑾Fe(OH)3+3HCl = FeCl3+3H2O Fe3++3H2OFe(OH)3胶体+3H+(净水) Fe(OH)3+3H+= Fe3++3H2O ⑿2Fe(OH)3 Fe2O3+3H2O ⒀Fe2O3+6HCl = 2FeCl3+3H2O ※⒁FeCl3+3KSCN = Fe(SCN)3+3KCl Fe2O3+6H+= 2Fe3++3H2O Fe3++3SCN-= Fe(SCN)3 4、硅及其化合物的转化关系 Na2SiO3 SiF4 Si SiO2 H2SiO3 CaSiO3 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ①Si+O2 SiO2 ②SiO2+2CSi+2CO↑ ※③SiO2+4HF = SiF4↑+2H2O(刻蚀玻璃) ④Si+4HF = SiF4↑+2H2↑ ⑤ SiO2+CaOCaSiO3 ※⑥ SiO2+2NaOH = Na2SiO3+H2O SiO2+CaCO3CaSiO3+CO2↑ SiO2+2OH-= SiO32-+H2O ※⑦ Na2SiO3+2HCl = H2SiO3↓+2NaCl SiO2+Na2CO3Na2SiO3+CO2↑ SiO32-+2H+= H2SiO3↓ ※⑦Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3或Na2SiO3+2H2O+2CO2=H2SiO3↓+2NaHCO3 SiO32-+H2O+CO2=H2SiO3↓+CO32-或SiO32-+2H2O+2CO2=H2SiO3↓+2HCO3- ⑧H2SiO3+2NaOH = Na2SiO3+2H2O ⑨H2SiO3H2O+SiO2 H2SiO3+2OH-= SiO32-+2H2O 5、氯及其化合物的转化关系 CuCl2 HClO HCl Cl2 FeCl3 NaClO Ca(ClO)2 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩ ①2Fe+3Cl2 2FeCl3 ②Cu+Cl2 CuCl2 ③2FeCl3+Cu = 2FeCl2+CuCl2 2Fe3++Cu = 2Fe2++Cu2+ 点燃 或光照 ④H2+Cl2 2HCl ※⑤MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O 光照 MnO2+4H++2Cl-Mn2++Cl2↑+2H2O 光照 ※⑥Cl2+H2O = HCl+HClO ※⑦2HClO 2HCl+O2↑ Cl2+H2O = H++Cl-+HClO 2HClO 2H++2Cl-+O2↑ ※⑧Cl2+2NaOH = NaCl+NaClO+H2O ※⑨2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O Cl2+2OH-= Cl-+ClO-+H2O 工业制漂白粉 ※⑩Ca(ClO)2+H2O+CO2 = CaCO3↓+2HClO或Ca(ClO)2+2HCl = CaCl2+2HClO Ca2++2ClO-+H2O+CO2= CaCO3↓+2HClO或ClO-+H+= HClO 漂白粉的漂白原理 向漂白粉溶液中通入过量的CO2:Ca(ClO)2+2H2O+2CO2 = Ca(HCO3)2+2HClO ClO-+H2O+CO2 = HCO3-+HClO 6、硫及其化合物的转化关系 ① ⑤ S SO2 SO3 H2SO4 CaSO3 CaSO4 ② ③ ④ ⑥ ⑦ ⑧氯水 ⑨Cu ⑩C ①S+O2 SO2 ②2H2S+SO2=3S+2H2O ※③SO2+O22SO3 ④SO3+H2O = H2SO4 ⑤SO2+CaOCaSO3 或 SO2+Ca(OH)2 = CaSO3↓+H2O ⑥ SO3+CaO = CaSO4 SO2+Ca2++2OH-=CaSO3↓+H2O SO3+Ca(OH)2 = CaSO4+H2O ⑦2CaSO3+O22CaSO4 ※⑧SO2+Cl2+2H2O = H2SO4+2HCl ※⑨Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O SO2+Cl2+2H2O = 4H++SO42-+2Cl- Cu+2H2SO4(浓)Cu2++SO42-+SO2↑+2H2O ※⑩C+2H2SO4(浓) CO2↑+2SO2↑+2H2O 高温或放电 7、氮及其化合物的转化关系 ① ⑨ ⑧ ⑦ ⑥ ④ ③ ⑤ N2 NH3 NH4Cl NO NO2 HNO3 ② ③ ※①N2+O2 2NO ※②2NO+O2 = 2NO2 ※③3NO2+H2O = 2HNO3+NO 3NO2+H2O =2H++2NO3-+NO 以上三个反应为“雷雨发庄稼”原理 扩展反应有:4NO2+O2+2H2O = 4HNO3 4NO+3O2+2H2O = 4HNO3 光照 ※④Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 上面两个反应主要用于气体溶于水时的计算 Cu+4H++2NO3-=Cu2++2NO2↑+2H2O 或4HNO3 4NO2↑+ O2↑+ 2H2O C+4HNO3(浓)CO2↑+2NO2↑+2H2O 浓硝酸见光易变黄的原因 ※⑤3Cu+8HNO3(稀) = 3Cu(NO3)2+2NO↑+4H2O ⑥N2+3H22NH3 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 合成氨反应是人工固氮的主要途径 ⑦NH3+HCl = NH4Cl ⑧NH4Cl NH3↑+HCl↑ NH3+H+ = NH4+(水溶液中) 补充:NH4HCO3 NH3↑+H2O+CO2↑ 氨气与酸均能反应生成铵盐,且与挥发性酸(如浓HCl、浓HNO3)相遇时空气中有白烟 铵盐受热都易分解,但并不是所有的铵盐 都分解出氨气,如NH4NO3、(NH4)2SO4 ※⑧NH4Cl+NaOH NaCl+NH3↑+H2O NH4++OH-NH3↑+H2O 所有的铵盐都能与碱作用放出氨气,可利用此反应鉴别铵离子。 ※⑧⑶2NH4Cl+2Ca(OH)2CaCl2+2NH3↑+2H2O 实验室制氨气,此反应为固体反应,不能写成离子方程式。 ☆⑨4NH3+5O24NO+6H2O 氨的催化氧化反应,工业制硝酸的第一步。 注:带“※”的反应为重要反应,必须熟记;带“☆”的反应只需了解。 必修二 第一章 物质结构 元素周期律 1、Li与O2反应(点燃): 4Li + O2 2Li2 O Na与O2反应(点燃): 2Na+O2Na2O2 Na与H2O反应: 2Na+2H2O===2NaOH+H2↑ K与H2O反应: 2K+2H2O===2KOH+H2↑ 2、卤素单质F2 、Cl2 、Br2 、I2与氢气反应: F2 + H2 === 2HF Cl2 + H2 === 2HCl Br2 + H2 === 2Br I2 + H2 === 2HI 3、卤素单质间的置换反应: (1)氯水与饱和溴化钠、氯水与饱和碘化钠溶液反应: ① Cl2+2NaBr===Br2+2NaCl ② Cl2+2NaI===I2+2NaCl (2)溴水与碘化钠溶液反应:Br2+2NaI===I2+2NaBr 4、Mg与H2O反应:Mg+2H2O === Mg(OH)2+H2↑ Al与HCl反应: 2Al+6HCl===2AlCl3+3H2↑ Mg与HCl反应: Mg+2 HCl === MgCl2+ H2↑ 5、Na与Cl2反应(点燃): 6、用电子式表示氯化氢的形成过程: 第二章 化学反应与能量 1、Ba(OH)2•8H2O与NH4Cl的反应 : Ba(OH)2·8H2O+2NH4Cl==BaCl2+2NH3↑+10H2O 2、原电池原理 典型的原电池(Zn-Cu原电池) 负极(锌):Zn-2e-===Zn2+(氧化反应) 正极(铜):2H++2e-===H2↑(还原反应) 电子流动方向:由锌经过外电路流向铜。 总反应离子方程式:Zn+2H+===Zn2++H2↑ 3、H2O2在催化剂作用下受热分解: 2H2O2 2H2O+O2↑ 4、Na2SO4与CaCl2反应:Na2SO4+CaCl2===CaSO4↓+Na2CO3 5、高炉炼铁:2C + O2 === 2CO Fe2O3 + 3CO ==2Fe + 3CO2 第三章 有机化合物 1、甲烷的主要化学性质 (1)氧化反应(与O2的反应):CH4(g)+2O2(g) CO2(g)+2H2O(l) (2)取代反应(与Cl2在光照条件下的反应,生成四种不同的取代物): 2、乙烯的主要化学性质 (1)氧化反应(与O2的反应):C2H4+3O2 2CO2+2H2O (2)加成反应((与Br2的反应): (3)乙烯还可以和氢气、氯化氢、水等发生加成反应: CH2=CH2 + H2CH3CH3 CH2=CH2+HClCH3CH2Cl(一氯乙烷) CH2=CH2+H2OCH3CH2OH(乙醇) (4)聚合反应: (乙烯制聚乙烯)① (氯乙烯制聚氯乙烯)② 3、苯的主要化学性质: (1)氧化反应(与O2的反应):2C6H6+15O2 12CO2+6H2O (2)取代反应: Br ① 与Br2的反应: + Br2 + HBr ② 苯与硝酸(用HONO2表示)发生取代反应,生成无色、不溶于水、有苦杏仁气味、密度大于水的油状液体——硝基苯。反应方程式: —NO2 + HONO2 + H2O (3)加成反应 用镍做催化剂,苯与氢发生加成反应: + 3H2 4、乙醇的重要化学性质 (1)乙醇与金属钠的反应:2CH3CH2OH+2Na2CH3CH2ONa+H2↑ (2)乙醇的氧化反应 ①乙醇的燃烧: CH3CH2OH+3O2 2CO2+3H2O ②乙醇的催化氧化反应: 2CH3CH2OH+O2 2CH3CHO+2H2O ③乙醇在常温下的氧化反应: CH3CH2OHCH3COOH 5、乙酸的重要化学性质 (1)乙酸的酸性 ①乙酸能使紫色石蕊试液变红 ②乙酸能与碳酸盐反应,生成二氧化碳气体 利用乙酸的酸性,可以用乙酸来除去水垢(主要成分是CaCO3): 2CH3COOH+CaCO3(CH3COO)2Ca+H2O+CO2↑ 乙酸还可以与碳酸钠反应,也能生成二氧化碳气体: 2CH3COOH+Na2CO32CH3COONa+H2O+CO2↑ 上述两个反应都可以证明乙酸的酸性比碳酸的酸性强。 (2)乙酸的酯化反应 ①反应原理(与乙醇的反应): 乙酸与乙醇反应的主要产物乙酸乙酯是一种无色、有香味、密度比水的小、不溶于水的油状液体。 6、①蔗糖水解反应:C12H22O11+H2O→C6H12O6+C6H12O6 ②淀粉(纤维素)水解反应: ③油脂的重要化学性质——水解反应: a)油脂在酸性条件下的水解: 油脂+H2O甘油+高级脂肪酸 b)油脂在碱性条件下的水解(又叫皂化反应): 油脂+H2O甘油+高级脂肪酸 蛋白质+H2O各种氨基酸 第四章 化学与可持续发展 1、HgO受热分解:2HgO 2Hg + O2↑ Ag2O受热分解:2Ag2O 4Ag + O2↑ 2、CO还原Fe2O3:Fe2O3 + 3CO 2Fe +3CO2 (高炉炼铁) ① C 还原ZnO :2 ZnO + C 2 Zn +CO2↑ ② C 还原MgO : MgO +C Mg + CO↑ ③ Al 还原Fe2O3(铝热反应): Fe2O3 + 2Al 2Fe + Al2O3 ④ Fe还原CuSO4: CuSO4 + Fe ==== FeSO4 +Cu (湿法炼铜) 3、电解 ①电解NaCl:2NaCl(熔融) 2Na +Cl2↑ ②电解MgCl2: MgCl2(熔融) Mg +Cl2↑ ③电解Al2O3: 2Al2O3(熔融) 4Al + 3O2↑ 4、石油的催化裂化 例如:C4H10 C2H4 + C2H6 C16H34 C8H18 +C8H16 C8H18 C4H10 +C4H8 C4H10 CH4 + C3H6 C4H10 C2H4 + C2H6查看更多