- 2021-05-10 发布 |
- 37.5 KB |
- 2页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
中考复习时溶液的浓度 溶液的配制复习教案无答案
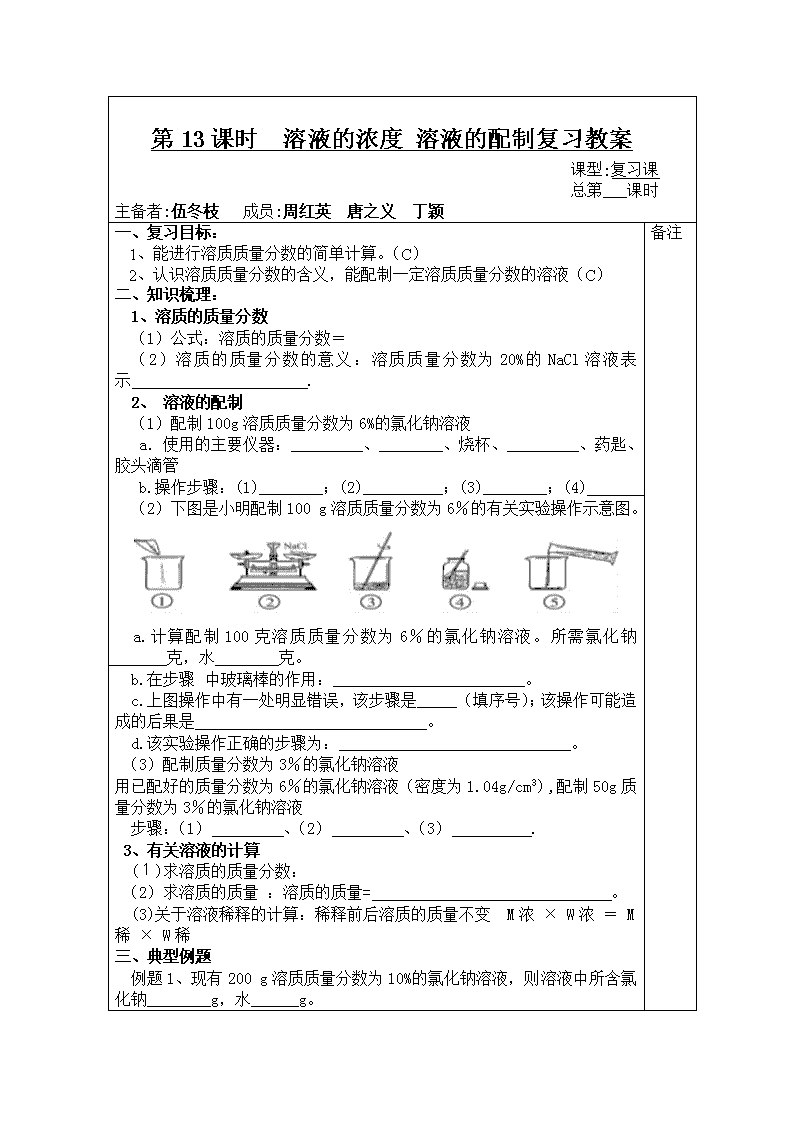
第13课时 溶液的浓度 溶液的配制复习教案 课型:复习课 总第___课时 主备者:伍冬枝 成员:周红英 唐之义 丁颖 一、复习目标: 1、 能进行溶质质量分数的简单计算。(C) 2、 认识溶质质量分数的含义,能配制一定溶质质量分数的溶液(C) 二、知识梳理: 1、溶质的质量分数 (1)公式:溶质的质量分数= (2)溶质的质量分数的意义:溶质质量分数为20%的NaCl溶液表示 . 2、 溶液的配制 (1)配制100g溶质质量分数为6%的氯化钠溶液 a.使用的主要仪器:_________、________、烧杯、_________、药匙、胶头滴管 b.操作步骤:(1)________;(2)__________;(3)________;(4) . (2)下图是小明配制100 g溶质质量分数为6%的有关实验操作示意图。 a.计算配制100克溶质质量分数为6%的氯化钠溶液。所需氯化钠________克,水________克。 b.在步骤中玻璃棒的作用:________________________。 c.上图操作中有一处明显错误,该步骤是_____(填序号);该操作可能造成的后果是_____________________________。 d.该实验操作正确的步骤为:_____________________________。 (3)配制质量分数为3%的氯化钠溶液 用已配好的质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制50g质量分数为3%的氯化钠溶液 步骤:(1) 、(2) 、(3) . 3、有关溶液的计算 (1)求溶质的质量分数: (2)求溶质的质量 :溶质的质量= 。 (3)关于溶液稀释的计算:稀释前后溶质的质量不变 M浓 × W浓 = M稀 × W稀 三、典型例题 例题1、现有200 g溶质质量分数为10%的氯化钠溶液,则溶液中所含氯化钠________g,水______g。 备注 例题2、向100g10%NaOH溶液中加入12.5gNaOH固体,完全溶解后,所得溶液中溶质质量分数为少? 例题3、现将100克20%的稀硫酸加水稀释为10%的稀硫酸,需加水的质量为多少? 例题4、32.5克锌粒与280克稀硫酸恰好完全反应。试求:(1)稀硫酸中溶质的质量分数。(2)生成物溶液中溶质的质量分数。 四、小结: 五、当堂训练: 教学反思:查看更多