- 2021-05-10 发布 |
- 37.5 KB |
- 4页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018中考化学模拟试题及答案
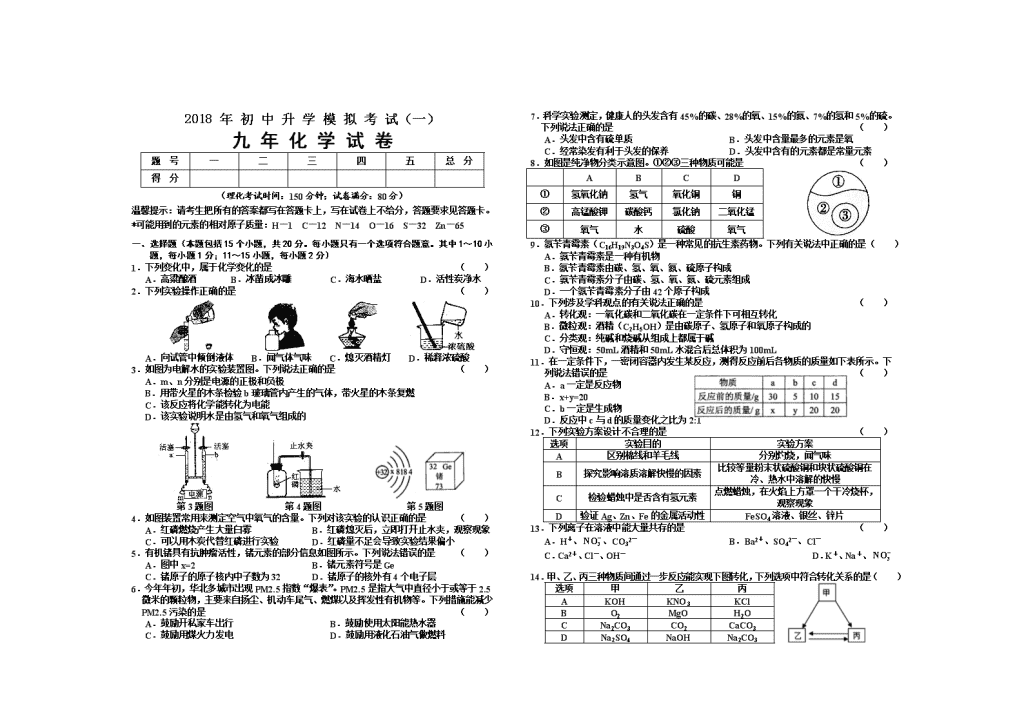
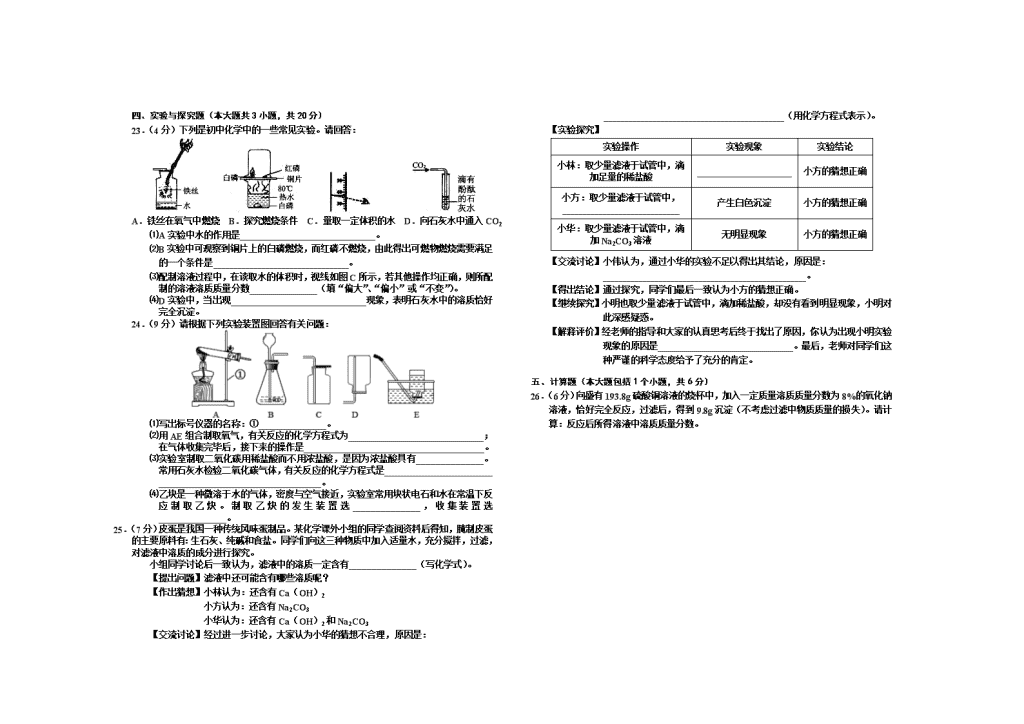
2018 年 初 中 升 学 模 拟 考 试(一) 九 年 化 学 试 卷 题 号 一 二 三 四 五 总 分 得 分 (理化考试时间:150分钟;试卷满分:80分) 温馨提示:请考生把所有的答案都写在答题卡上,写在试卷上不给分,答题要求见答题卡。 *可能用到的元素的相对原子质量:H—1 C—12 N—14 O—16 S—32 Zn—65 一、选择题(本题包括15个小题,共20分。每小题只有一个选项符合题意。其中1~10小题,每小题1分;11~15小题,每小题2分) 1.下列变化中,属于化学变化的是 ( ) A.高粱酿酒 B.冰凿成冰雕 C.海水晒盐 D.活性炭净水 2.下列实验操作正确的是 ( ) A.向试管中倾倒液体 B.闻气体气味 C.熄灭酒精灯 D.稀释浓硫酸 3.如图为电解水的实验装置图。下列说法正确的是 ( ) A.m、n分别是电源的正极和负极 B.用带火星的木条检验b玻璃管内产生的气体,带火星的木条复燃 C.该反应将化学能转化为电能 D.该实验说明水是由氢气和氧气组成的 第3题图 第4题图 第5题图 4.如图装置常用来测定空气中氧气的含量。下列对该实验的认识正确的是 ( ) A.红磷燃烧产生大量白雾 B.红磷熄灭后,立即打开止水夹,观察现象 C.可以用木炭代替红磷进行实验 D.红磷量不足会导致实验结果偏小 5.有机锗具有抗肿瘤活性,锗元素的部分信息如图所示。下列说法错误的是 ( ) A.图中x=2 B.锗元素符号是Ge C.锗原子的原子核内中子数为32 D.锗原子的核外有4个电子层 6.今年年初,华北多城市出现PM2.5指数“爆表”。PM2.5是指大气中直径小于或等于2.5微米的颗粒物,主要来自扬尘、机动车尾气、燃煤以及挥发性有机物等。下列措施能减少PM2.5污染的是 ( ) A.鼓励开私家车出行 B.鼓励使用太阳能热水器 C.鼓励用煤火力发电 D.鼓励用液化石油气做燃料 7.科学实验测定,健康人的头发含有45%的碳、28%的氧、15%的氮、7%的氢和5%的硫。下列说法正确的是 ( ) A.头发中含有硫单质 B.头发中含量最多的元素是氧 C.经常染发有利于头发的保养 D.头发中含有的元素都是常量元素 8.如图是纯净物分类示意图。①②③三种物质可能是 ( ) A B C D ① 氢氧化钠 氢气 氧化铜 铜 ② 高锰酸钾 碳酸钙 氯化钠 二氧化锰 ③ 氧气 水 硫酸 氧气 9.氨苄青霉素(C16H19N3O4S)是一种常见的抗生素药物。下列有关说法中正确的是( ) A.氨苄青霉素是一种有机物 B.氨苄青霉素由碳、氢、氧、氮、硫原子构成 C.氨苄青霉素分子由碳、氢、氧、氮、硫元素组成 D.一个氨苄青霉素分子由42个原子构成 10.下列涉及学科观点的有关说法正确的是 ( ) A.转化观:一氧化碳和二氧化碳在一定条件下可相互转化 B.微粒观:酒精(C2H5OH)是由碳原子、氢原子和氧原子构成的 C.分类观:纯碱和烧碱从组成上都属于碱 D.守恒观:50mL酒精和50mL水混合后总体积为100mL 11.在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列说法错误的是 ( ) A.a一定是反应物 B.x+y=20 C.b一定是生成物 D.反应中c与d的质量变化之比为2:1 12.下列实验方案设计不合理的是 ( ) 选项 实验目的 实验方案 A 区别棉线和羊毛线 分别灼烧,闻气味 B 探究影响溶质溶解快慢的因素 比较等量粉末状硫酸铜和块状硫酸铜在冷、热水中溶解的快慢 C 检验蜡烛中是否含有氢元素 点燃蜡烛,在火焰上方罩一个干冷烧杯,观察现象 D 验证Ag、Zn、Fe的金属活动性 FeSO4溶液、银丝、锌片 13.下列离子在溶液中能大量共存的是 ( ) A.H+、、CO32- B.Ba2+、SO42-、Cl- C.Ca2+、Cl-、OH- D.K+、Na+、 14.甲、乙、丙三种物质间通过一步反应能实现下图转化,下列选项中符合转化关系的是( ) 选项 甲 乙 丙 A KOH KNO3 KCl B O2 MgO H2O C Na2CO3 CO2 CaCO3 D Na2SO4 NaOH Na2CO3 15.现有一定质量含有少量泥沙等不溶性杂质和少量CaCl2、MgCl2、Na2SO4等可溶性杂质的粗盐样品。某实验小组利用实验室常用仪器对样品进行提纯,先将粗盐溶解于水,然后进行下列六项操作:①过滤;②加适量盐酸;③加过量Na2CO3溶液;④加过量NaOH溶液;⑤加过量BaCl2溶液;⑥蒸发,其中正确的操作顺序是 ( ) A.①④⑤③②⑥ B.④①③⑤②⑥ C.⑤④③②①⑥ D.⑤④③①②⑥ 二、填空题(本题包括4个小题。每空1分,共20分) 16.(5分)请用化学用语填空: ⑴2个铝离子_______________。 ⑵氩元素_______________。 ⑶标出硫酸铁中铁元素的化合价_______________。 ⑷硝酸铵:_______________。 ⑸自然界中最硬的物质_______________。 17.(5分)化学来源于生活,化学与生活密切相关。 ⑴硬水危害人体健康,生活中降低水硬度的方法是_______________。 ⑵合理膳食有益健康。蔬菜、水果中富含的营养素是_______________。 ⑶用洗洁精能除去餐具上的油污,这是利用了洗洁精的_______________作用。 ⑷食品包装中常充N2以防腐,这是由于N2_______________。 锤子常用铁制,而不用铝制,其原因是_______________。 18(5分)“共享单车”是指在公共场所提供共享服务的自行车,由于符合“低碳出行”的理念,颇受年轻人的喜爱。 ⑴“共享单车”车架的表面喷漆不仅美观,而且可有效阻止铁与_______________接触而锈蚀。 ⑵自行车的有些部件是由钢铁制成的,写出一氧化碳与氧化铁炼铁的化学方程式: _____________________________________________。 ⑶扫描二维码可以租用“共享单车”,二维码的制作材料一般是用PVC不干胶贴纸。PVC材料属于_______________(填“金属”、“有机合成”或“复合”)材料。PVC【其化学式为(C2H3Cl)n】中碳元素和氢元素的质量比为_______________。 19.(5分)t2℃时,将A、B两种物质各30g分别放入盛有50g水的烧杯中,充分溶解后,恢复到t2℃,现象如图一所示。A和B的溶觯度曲线如图二所示。请合图示答下列问题: ⑴P点的含义:____________________________________________________________。 ⑵固体A对应的溶解度曲线是_______________(填“甲”或“乙”)。 ⑶若要使烧杯②中的溶液恰好达到该温度下的饱和状态,还需要加入_______________g固体B。 ⑷若B中混有少量A,可采用_______________的方法提纯B。 ⑸将t2℃等质量的A、B饱和溶液分别降温到t1℃时,所得溶液的有关说法正确的是_______________(填字母序号)。 a.B溶液仍为饱和溶液 b.两种溶液中溶剂质量:A<B c.两种溶液中溶质质量分数:A=B d.两种溶液质量:A>B 三、简答题(本题包括3个小题,共14分) 20.(5分)能源、环境与人类的生活和社会发展密切相关。我国已在南海某领域试采可燃冰成功。可燃冰主要是由甲烷与水在高压低温条件下形成的,由于外观像冰且可燃烧,所以被称为“可燃冰”。可燃冰燃烧产生的能量比传统的化石燃料要多出数十倍,而且燃烧后不产生任何的残渣和废气,是公认的地球上尚未开发的最大新型能源。 ⑴目前,人类使用的化石燃料主要包括煤、_______________和天然气。 ⑵写出甲烷燃烧的化学方程式______________________________。 ⑶为方便贮存和运输,天然气通常被压缩到容积很小的钢瓶中,而可燃冰却很难被压缩。试从分子的角度分析,其中的原因是______________________________。 ⑷写出可燃冰作为新型能源的一条优点______________________________。 21.(4分)质量守恒定律的发现对化学的发展作出了巨大贡献。 ⑴为验证质量守恒定律,小华设计如上图l所示装置进行实验。 实验时,先将装有药品的装置放在天平上,添加砝码,移动游码至天平平衡,然后取下装置,用注射器向锥形瓶中注入少量稀盐酸,反应后再将装置放置于天平上,观察到______________________________,从而验证了质量守恒定律。若将锥形瓶改为烧杯,则不能验证质量守恒定律,原因是______________________________。 ⑵某反应的微观示意图如上图2所示。 ①x的化学式是_______________。 ②根据上述微观示意图,可得出化学反应遵循质量守恒定律的本质原因是: _____________________________________________。 22.(7分)A~H是初中化学常见物质,下图为这些物质的相互转化关系图。其中E为红色固体,H为红褐色沉淀,其中部分生成物与反应条件已省略。 ⑴F的化学式为:_______________; ⑵E→C化学方程式为:__________________________; ⑶上述反应中未涉及的基本反应类型为:__________________; ⑷举出E→C在工业生产中对应的一种用途:__________________。 四、实验与探究题(本大题共3小题,共20分) 23.(4分)下列是初中化学中的一些常见实验。请回答: A.铁丝在氧气中燃烧 B.探究燃烧条件 C.量取一定体积的水 D.向石灰水中通入CO2 ⑴A实验中水的作用是______________________________。 ⑵B实验中可观察到铜片上的白磷燃烧,而红磷不燃烧,由此得出可燃物燃烧需要满足的一个条件是______________________________。 ⑶配制溶液过程中,在读取水的体积时,视线如图C所示,若其他操作均正确,则所配制的溶液溶质质量分数_______________(填“偏大”、“偏小”或“不变”)。 ⑷D实验中,当出现______________________________现象,表明石灰水中的溶质恰好完全沉淀。 24.(9分)请根据下列实验装置图回答有关问题: ⑴写出标号仪器的名称:①_______________。 ⑵用AE组合制取氧气,有关反应的化学方程式为______________________________;在气体收集完毕后,接下来的操作是________________________________________。 ⑶实验室制取二氧化碳用稀盐酸而不用浓盐酸,是因为浓盐酸具有_______________。常用石灰水检验二氧化碳气体,有关反应的化学方程式是____________________________________________________________。 ⑷乙块是一种微溶于水的气体,密度与空气接近,实验室常用块状电石和水在常温下反应制取乙炔。制取乙炔的发生装置选_______________,收集装置选_______________。 25.(7分)皮蛋是我国一种传统风味蛋制品。某化学课外小组的同学查阅资料后得知,腌制皮蛋的主要原料有:生石灰、纯碱和食盐。同学们向这三种物质中加入适量水,充分搅拌,过滤,对滤液中溶质的成分进行探究。 小组同学讨论后一致认为,滤液中的溶质一定含有_______________(写化学式)。 【提出问题】滤液中还可能含有哪些溶质呢? 【作出猜想】小林认为:还含有Ca(OH)2 小方认为:还含有Na2CO3 小华认为:还含有Ca(OH)2和Na2CO3 【交流讨论】经过进一步讨论,大家认为小华的猜想不合理,原因是: ________________________________________(用化学方程式表示)。 【实验探究】 实验操作 实验现象 实验结论 小林:取少量滤液于试管中,滴加足量的稀盐酸 _____________________ 小方的猜想正确 小方:取少量滤液于试管中,__________________________ 产生白色沉淀 小方的猜想正确 小华:取少量滤液于试管中,滴加Na2CO3溶液 无明显现象 小方的猜想正确 【交流讨论】小伟认为,通过小华的实验不足以得出其结论,原因是: _____________________________________________。 【得出结论】通过探究,同学们最后一致认为小方的猜想正确。 【继续探究】小明也取少量滤液于试管中,滴加稀盐酸,却没有看到明显现象,小明对此深感疑惑。 【解释评价】经老师的指导和大家的认真思考后终于找出了原因,你认为出现小明实验现象的原因是______________________________。最后,老师对同学们这种严谨的科学态度给予了充分的肯定。 五、计算题(本大题包括1个小题,共6分) 26.(6分)向盛有193.8g硫酸铜溶液的烧杯中,加入一定质量溶质质量分数为8%的氧化钠溶液,恰好完全反应,过滤后,得到9.8g沉淀(不考虑过滤中物质质量的损失)。请计算:反应后所得溶液中溶质质量分数。 C九年化学(J营) 答案 +3 一、1.A 2. C 3. B 4.D 5.C 6.B 7.D 8.B 9.A 10.A 11.C 12.B 13.D 14.C 15.D 二、16. (1)2Al3+ (2)Ar (3)Fe2(SO4)3 (4)NH4NO3 (5)C 17.(1)煮沸 (2)维生素 (3)乳化 (4)常温下化学性质稳定 (5)铁的硬度较铝大 18.(1)氧气和水 (2)3CO+ Fe2O3 2 Fe +3CO2 (3)有机合成 8:1 19.(1)在t1℃时,甲、乙两物质的溶解度相等 (2)乙 (3)10 (4)降温结晶(或冷却热饱和溶液) (5)ad 三、20.(1)石油 (2)CH4+2O2CO2+2H2O (3)气态物质分子间的间隔较大,易被压缩,而固态物质分子间的间隔较小,不易被压缩等合理表述 (4)对环境污染小(或燃烧热值高等合理答案) 21.(1)天平平衡(或天平指针指在分度盘中央的位置等合理表述) 反应生成的气体逸散到空气中,使左盘质量减小(或装置不密闭等合理答案) (2)①SO2 ②原子种类、数目和质量都没有改变 22.(1) HaOH (2)300+Fe2O3 高温 2Fe+3CO2 (3)置换 (4)除锈 四、23.(1)防止高温熔化物溅落下来炸裂瓶底 (2)温度达到可燃物的着火点 (3)偏小 (4)溶液红色刚好消失(或溶液由红色刚好变为无色)等合理表述 24.(1)铁架台 (2)2KMnO4 △ K2MnO4+MnO2+O2↑;撤出导管,再熄灭酒精灯。 (3)挥发性; CO2+Ca(OH)2=Ca(OH)3↓+2H2O (4)B;E 25.NaCl、NaOH 【交流讨论】Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 【实验探究】实验现象:先无明显现象,后有气泡生成(答有气泡生成也给分) 实验操作:滴加CaCl2溶液[或Ca(NO3)2溶液、Ca(OH)2溶液、BaCl2溶液、Ba(NO3)2溶液、Ba(OH)2溶液等合理答案] 【交流讨论】无明显现象只能证明溶质中不含有氢氧化钙,不能证明是否含有碳酸钠等合理表述 【解释评价】滤液中含有NaOH,盐酸用量太少不会有气泡生成等合理表述 五、26.解: 设氢氧化钠溶液中氢氧化钠质量为x,生成硫酸钠质量为y。 CuSO4+ 2NaOH = Cu(OH)2↓+ Na2SO4 80 98 142 x 9.8g y x=8g y=14.2g 氢氧化钠溶液质量=8g÷8%=100g 反应后所得溶液质量=193.8g+100g-9.8g=284g 反应后所得溶液中溶质质量分数: 答:反应后所得溶液中溶质质量分数为5%。查看更多