- 2021-11-11 发布 |
- 37.5 KB |
- 7页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019年中考化学试题分类:3综合 7实验探究
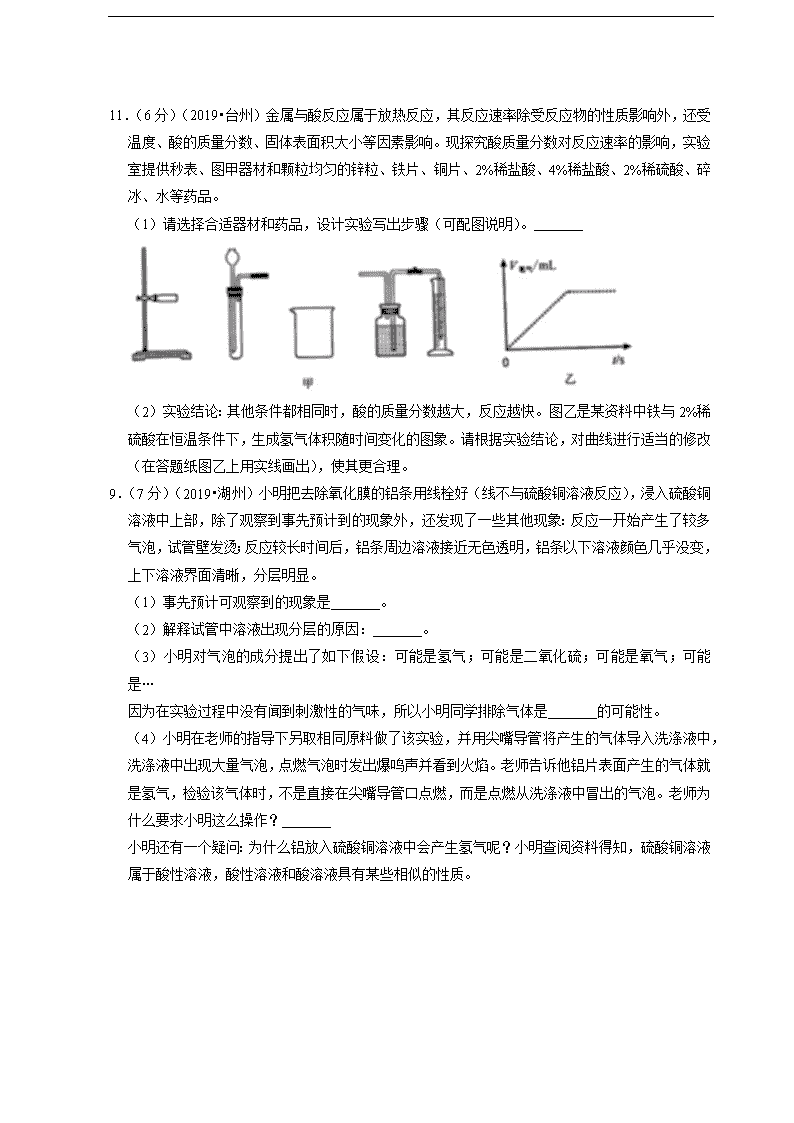
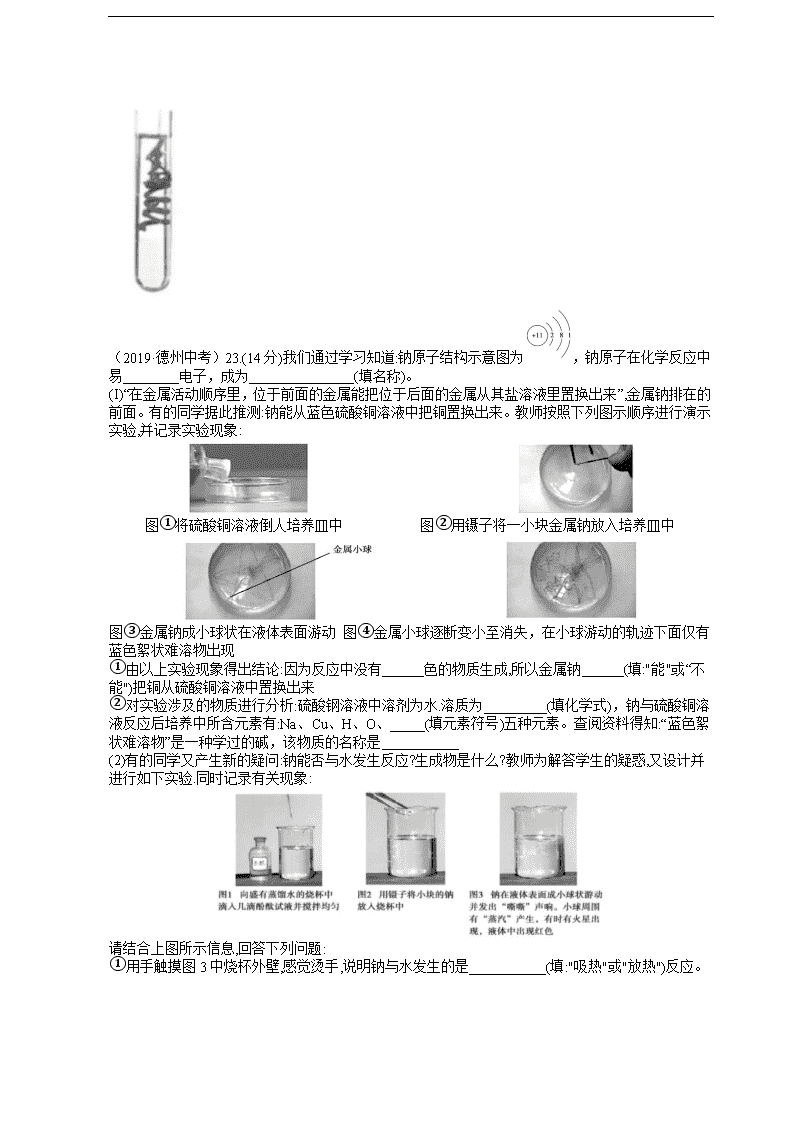
11.(6分)(2019•台州)金属与酸反应属于放热反应,其反应速率除受反应物的性质影响外,还受温度、酸的质量分数、固体表面积大小等因素影响。现探究酸质量分数对反应速率的影响,实验室提供秒表、图甲器材和颗粒均匀的锌粒、铁片、铜片、2%稀盐酸、4%稀盐酸、2%稀硫酸、碎冰、水等药品。 (1)请选择合适器材和药品,设计实验写出步骤(可配图说明)。 (2)实验结论:其他条件都相同时,酸的质量分数越大,反应越快。图乙是某资料中铁与2%稀硫酸在恒温条件下,生成氢气体积随时间变化的图象。请根据实验结论,对曲线进行适当的修改(在答题纸图乙上用实线画出),使其更合理。 9.(7分)(2019•湖州)小明把去除氧化膜的铝条用线栓好(线不与硫酸铜溶液反应),浸入硫酸铜溶液中上部,除了观察到事先预计到的现象外,还发现了一些其他现象:反应一开始产生了较多气泡,试管壁发烫;反应较长时间后,铝条周边溶液接近无色透明,铝条以下溶液颜色几乎没变,上下溶液界面清晰,分层明显。 (1)事先预计可观察到的现象是 。 (2)解释试管中溶液出现分层的原因: 。 (3)小明对气泡的成分提出了如下假设:可能是氢气;可能是二氧化硫;可能是氧气;可能是… 因为在实验过程中没有闻到刺激性的气味,所以小明同学排除气体是 的可能性。 (4)小明在老师的指导下另取相同原料做了该实验,并用尖嘴导管将产生的气体导入洗涤液中,洗涤液中出现大量气泡,点燃气泡时发出爆鸣声并看到火焰。老师告诉他铝片表面产生的气体就是氢气,检验该气体时,不是直接在尖嘴导管口点燃,而是点燃从洗涤液中冒出的气泡。老师为什么要求小明这么操作? 小明还有一个疑问:为什么铝放入硫酸铜溶液中会产生氢气呢?小明查阅资料得知,硫酸铜溶液属于酸性溶液,酸性溶液和酸溶液具有某些相似的性质。 (2019·德州中考)23.(14分)我们通过学习知道:钠原子结构示意图为,钠原子在化学反应中易________电子,成为_______________(填名称)。 (I)“在金属活动顺序里,位于前面的金属能把位于后面的金属从其盐溶液里置换出来”,金属钠排在的前面。有的同学据此推测:钠能从蓝色硫酸铜溶液中把铜置换出来。教师按照下列图示顺序进行演示实验,并记录实验现象: 图①将硫酸铜溶液倒人培养皿中 图②用镊子将一小块金属钠放入培养皿中 图③金属钠成小球状在液体表面游动 图④金属小球逐断变小至消失,在小球游动的轨迹下面仅有蓝色絮状难溶物出现 ①由以上实验现象得出结论:因为反应中没有______色的物质生成,所以金属钠______(填:"能"或“不能")把铜从硫酸铜溶液中置换出来 ②对实验涉及的物质进行分析:硫酸钢溶液中溶剂为水.溶质为_________(填化学式),钠与硫酸铜溶液反应后培养中所含元素有:Na、Cu、H、O、_____(填元素符号)五种元素。查阅资料得知:“蓝色絮状难溶物”是一种学过的碱,该物质的名称是___________ (2)有的同学又产生新的疑问:钠能否与水发生反应?生成物是什么?教师为解答学生的疑惑,又设计并进行如下实验.同时记录有关现象: 请结合上图所示信息,回答下列问题: ①用手触摸图3中烧杯外壁,感觉烫手,说明钠与水发生的是___________(填:"吸热"或"放热")反应。 ②从“图3”中可以断定:液体中出现红色说明反应后液体显_______性,结合液体中所含元素,继而推断有__________(填化学式)生成。另外,钠与水反应还生成一种可燃性气体单质。请写出钠与水反应的化学方程式:_________________________________________ (2019·安徽中考)15.(7分)某兴趣小组为探究金属活动性强弱,分别做了镁、铝、铜与稀盐酸反应的实验。 (1)比较金属活动性强弱:铝比铜______(填“强”或“弱”)。写出镁与稀盐酸反应的化学方程式:_____________________________________ (2)小芳同学做镁与稀盐酸反应的实验时,发现试管中出现灰白色沉淀,该小组同学对灰白色沉淀的成分进行如下探究: [提出假设]假设一:含有氯化镁 假设二:含有镁粉 假设三:含有氢氧化镁 …… [查阅资料]①氯化镁易溶于水: ②在一定条件下镁可与冷水缓慢反应。 [设计并进行实验]各取少量灰白色沉淀加入2支试管中进行如下实验: 编号 实验操作 实验现象 实验1 加入适量蒸馏水、搅拌 沉淀未见减少 实验2 加入适量稀盐酸 沉淀全部溶解,没有气泡产生 [得出结论]由实验1可知,假设___不成立;由实验2可知,沉淀中不含___。 假设三__________(填“成立”或“可能成立”或“不成立”)。 [实验反思]实验后同学们请教老师得知,灰白色沉淀的主要成分是碱式氯化镁,碱式氯化镁受热易分解产生氯化氢气体。于是小芳再取少量灰白色沉淀于试管中加热,并将蘸有紫色石蕊溶液的滤纸条悬于试管口,预期的实验现象是__________________________ 注意:若答对第(3)小题奖励4分.化学试卷总分不超过60分。 (3)为探究镁与稀盐酸反应生成碱式氯化镁的条件.该小组同学进行了如下实验:在小烧杯中加入一定量的盐酸和去除氧化膜的镁带,观察实验现象,并测量溶液pH的变化。结果见下表: 时间/min 0 2 4 8 12 16 20 24 溶液pH 2.0 5.3 7.0 8.6 9.3 9.8 10.0 10.0 实验现象 - 镁带溶解较快,产生大量气泡,无沉淀生成 镁带缓慢溶解,产生气泡速率减慢,溶液变浑浊,烧杯底部有灰白色沉淀 根据表中信息回答下列问题: ①请描述溶液pH变化的规律并解释原因:____________________ ②请对生成碱式氯化镁的条件提出猜想,并设计实验证明猜想:____________________ 9.(6分)(2019•衢州)某兴趣小组为探究锡纸中的金属成分(锡纸中以一种金属为主,其它成分对实验无干扰),开展了以下探究活动。 【提出问题】锡纸中的金属是什么? 【建立猜想】根据锡纸有银白色金属光泽,并结合金属活动性、价格等因素,猜想其中的金属可能是锌、铁、铝、锡中的一种。 【探究过程】 步骤 活动内容 收集证据 分析并得出结论 步骤一 ①查阅资料:金属锌在室温下很脆 锡纸未破损 锡纸中金属不是锌 ②取锡纸反复折叠 步骤二 用磁铁靠近锡纸 锡纸没有被磁铁吸引 锡纸中金属不是 步骤三 ①取锡纸条放入浓度为20%的盐酸中除去可能存在的氧化膜。当观察到 现象时,取出锡纸条并用蒸馏水清洗。 ②将处理过的锡纸条放入试管中,加入饱和硫酸锌溶液,静置观察。 ②中锡纸条表面无明显现象 说明锡纸中的金属活动性比锌弱,则锡纸中金属不是铝,而是锡。 【交流评价】 小科对实验结论提出质疑:“无明显现象”并不代表没有发生反应,因为铝与硫酸锌反应[2Al+3ZnSO4=3Zn+Al2(SO4)3]生成的金属锌为银白色,与铝颜色相同,因此无法得出结论。请在不改变反应原理的前提下运用定量方法完善实验方案,并根据预期结果得出相应结论: 。 【继续探究】运用完善后的方案进行实验,分析实验结果,得出初步结论:锡纸中金属是铝。 (2019·鄂州中考)43.小亮学完合金后,知道了不锈钢的主要成分是铁,白铜中含有铜和镍(Ni)。他决定探究Fe、Cu、Ni的金属活动性顺序。 (1)[查阅资料]镍能与稀硫酸反应生成能溶于水的NiSO4,并放出氢气。写出镍与稀硫酸反应的化学方程式: 。 (2)[猜想与假设]根据教材中常见金属的活动性顺序和查阅的资料,对以上三种金属 的活动性作出猜想: 猜想①Fe>Ni>Cu;猜想② 。 (3)[实验探究]把用砂纸打磨过的镍片浸入FeSO4溶液中,过一会儿取出,发现镍片 表面无明显变化。证明 (填“猜想①”或“猜想②”)成立。 (4)[拓展延伸]用铜片、NiSO4溶液和 ,通过实验探究也能判断Fe、Cu、Ni 的金属活动性顺序。 (2019·广州中考)29. (10分)已知金属钻(Co)的活动性与铁相似,请预测氯化钻(CoCl2)的化学性质,说明预测的依据,并设计实验验证。经查阅资料,钻的化合物相关性质如下: 物质 CoO Co(OH)2 CoCl2 CoSO4 Co(NO3)2 CoCO3 在水中溶的溶解性 难溶于水的灰绿色固体 难溶于水的粉红色固体 易溶于水形成粉红色溶液 易溶于水形成粉红色溶液 易溶于水形成粉红色溶液 难溶于水的粉红色固体 限选试剂:CoCl2溶液、(NH4)2CO3溶液、Na2SO4溶液、AgNO3溶液、NaOH溶液、稀硫酸、镁条、铜片。 预测 预测的依据 验证预测的实验操作与预期现象 ①能够与含Ag+的 可溶性盐反应 CoCl2 溶液中含Cl-, AgCl难溶于水。 取少量CoCl2溶液于试管中,__________,如果观察到_________________,则预测成立。 ②能够与________ (填物质类别)反应 ______________ 取少量CoCl2溶液于试管中,__________,如果观察到_________________,则预测成立。 ③能够与________ (填物质类别)反应 ______________ 取少量CoCl2溶液于试管中,__________,如果观察到_________________,则预测成立。 29.(8分)(2019•临沂)老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种。同学们对该粉末进行了定性与定量研究。 (1)定性实验: 实验方案 实验现象 实验结论 取少量红色粉末放入试管 中,滴加足量的稀盐酸振荡 红色粉末全部消失,溶液呈棕黄色 粉末为Fe2O3 粉末Cu 写出“红色粉末全部消失”发生反应的化学方程式 。 (2)定量实验: 取该粉末4g放入硬质玻璃管中,先通CO,然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却。实验装置如图: ①实验时,先通CO再加热的目的是 。 ②若该粉末全部是氧化铁,在硬质玻璃管中观察到的实验现象是 。B装置是用于吸收二氧化碳并收集CO,其中盛放的试剂最好是 。 A.NaOH溶液 B.稀盐酸 C.水 如果该实验没有装置B、C,实验造成的危害是 。 ③若该粉末为铜粉和氧化铁的混合物,待装置完全冷却至室温,称量硬质玻璃管内剩余固体的质量为mg。则m的取值范围是 。 (2019·毕节中考)22.(8 分)某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。 【查阅资料】 经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。该反应的化学方程式为 ▲ 。 【对比实验】 编号 操作 现象 甲 将表面未打磨的铝丝浸入CuSO4 溶液中 无明显现象 乙 将表面打磨后的铝丝浸入CuSO4 溶液中 铝丝表面析出红色固体 丙 将表面未打磨的铝丝浸入CuCl2 溶液中 铝丝表面析出红色固体 (1) 比较实验乙和实验 ▲ (填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。 (2) 实验乙中反应的化学方程式为 ▲ ,据此可知金属活动性 Al 比 Cu ▲ (填“强”或“弱”)。 (3) 小明同学对实验丙的现象进行分析,认为 H2O 对氧化铝薄膜有破坏作用。但此观点马上被其他同学否定,否定的依据是 ▲ 。 【猜测与探究】 小组同学针对实验丙的现象,经讨论后猜测:Cl- 破坏了氧化铝薄膜。 为检验此猜测是否正确,他们首先向两支试管中加入相同的 CuSO4 溶液,并均浸入表面未打磨的铝丝,然后进行了新的探究: 操作 现象 结论 推论 (1)向一支试管中再加入 NaCl 固体 铝丝表面析 出红色固体 氧化铝薄膜 被破坏 Na+或① ▲ 能 破坏氧化铝薄膜 (2)向另一支试管中再加入 Na2SO4 固体 ② ▲ 氧化铝薄膜 未被破坏 Na+和 SO2-都不能 4 破坏氧化铝薄膜 【结论与反思】 得出结论:前述猜测 ▲ (填“正确”或“不正确”)。总结反思:本次探究充分运用了比较法和控制变量法。查看更多