- 2021-11-11 发布 |
- 37.5 KB |
- 10页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2013年河南省中考原创仿真模拟试卷化学及详解
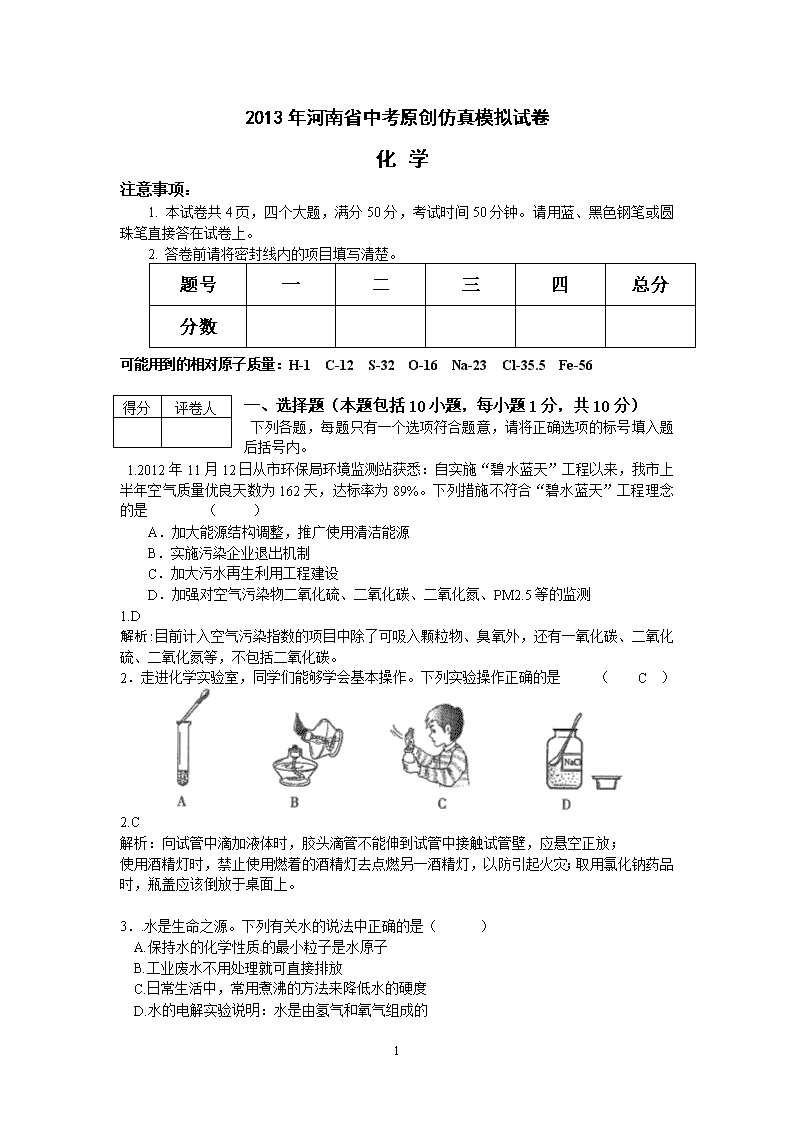
2013年河南省中考原创仿真模拟试卷 化 学 注意事项: 1. 本试卷共4页,四个大题,满分50分,考试时间50分钟。请用蓝、黑色钢笔或圆珠笔直接答在试卷上。 2. 答卷前请将密封线内的项目填写清楚。 题号 一 二 三 四 总分 分数 可能用到的相对原子质量:H-1 C-12 S-32 O-16 Na-23 Cl-35.5 Fe-56 得分 评卷人 一、选择题(本题包括10小题,每小题1分,共10分) 下列各题,每题只有一个选项符合题意,请将正确选项的标号填入题后括号内。 1.2012年11月12日从市环保局环境监测站获悉:自实施“碧水蓝天”工程以来,我市上半年空气质量优良天数为162天,达标率为89%。下列措施不符合“碧水蓝天”工程理念的是 ( ) A.加大能源结构调整,推广使用清洁能源 B.实施污染企业退出机制 C.加大污水再生利用工程建设 D.加强对空气污染物二氧化硫、二氧化碳、二氧化氮、PM2.5等的监测 1.D 解析:目前计入空气污染指数的项目中除了可吸入颗粒物、臭氧外,还有一氧化碳、二氧化硫、二氧化氮等,不包括二氧化碳。 2.走进化学实验室,同学们能够学会基本操作。下列实验操作正确的是 ( C ) 2.C 解析:向试管中滴加液体时,胶头滴管不能伸到试管中接触试管壁,应悬空正放; 使用酒精灯时,禁止使用燃着的酒精灯去点燃另一酒精灯,以防引起火灾;取用氯化钠药品时,瓶盖应该倒放于桌面上。 3..水是生命之源。下列有关水的说法中正确的是( ) A.保持水的化学性质的最小粒子是水原子 B.工业废水不用处理就可直接排放 C.日常生活中,常用煮沸的方法来降低水的硬度 D.水的电解实验说明:水是由氢气和氧气组成的 10 3.C 解析:分子是保持物质化学性质的最小粒子,因此,保持水的化学性质的最小粒子是水分子;水污染防治的关键是控制“污染源头”。为了保护水资源,我们要严禁工业废水的任意排放;水的电解实验生成氢气和氧气,说明水是由氢元素和氧元素组成的。 4.关于下图理解错误的是 ( ) A.在化学变化中原子重新结合成分子 B.在化学变化中分子可以化分成原子 C.物质都是由分子构成的 D.化学变化的实质是分子的破裂和原子的重新组合 4.C 解析:氢气是由分子构成的,但并不是所有物质都是由分子构成,金属、部分固态非金属、稀有气体是由原子构成,氯化钠、硫酸铜等是由离子构成的。 5.兴趣是最好的老师,化学实验深深地吸引了我们每一个同学。下列装置或操作能达到实验目的的是( ) A.稀释浓硫酸 B.探究燃烧的三个条件 C.测定空气中氧气的含量 D.探究C02的性质 5.D 解析:量筒不能用作反应容器,稀释浓硫酸,会受热不均,引起炸裂;B选项中,铜片上缺少红磷作对照,不能得出着火点的有关结论;C选项选取的反应物不合适,木炭燃烧生成气体二氧化碳,无气压差,不能准确测定空气中氧气的含量。 6.萝卜有很高的营养价值和药用价值,在民间有“小人参”之美称。俗语有“萝卜上 市、医生没事”之说。萝卜中含有丰富的碳水化合物和多种维生素,其中维生素C (化 学式为C6H8O6)的含量比梨高8-10倍。下列有关维生素C的说法正确的是 ( ) A.相对分子质量为176g B.由碳原子、氢分子和氧分子构成 C.氢元素的质量分数最小 D.碳、氢和氧三种元素的质量比为3:4:3 6.C 解析:相对分子质量是各原子相对原子质量的的加和,单位是1,A选项错误;B选项的错误在于宏观与微观的错配,应为维生素C由碳、氢、氧三种元素组成;由于不同元素的相对分子质量不同,因此任何物质中的元素质量比一定不等于原子个数比,D选项错误。 7.下列是检验氢氧化钠溶液是否变质的几种方法,其中不可行的是( ) A.滴加盐酸 B.滴加石灰水 10 C.滴加酚酞溶液 D.滴加氯化钙溶液 7.C 解析:氢氧化钠溶液易吸收空气中的二氧化碳生成碳酸钠而变质,碳酸钠溶液也显碱性,因此,滴加酚酞溶液均显红色,无法区别。 8.阳阳同学做了一个趣味实验,他把气球中的镁屑加入到盛有稀盐酸的锥形瓶中,整个实验过程如图所示(实验装置的气密性良好)。他关于本实验的下列说法中不正确的是( ) A.本实验能说明镁与稀盐酸反应时,有气体放出 B.本实验能说明与稀盐酸反应时,镁屑比镁条更快 C.本实验能说明镁与稀盐酸反应有热量放出 D.本实验能说明温度降低时,分子间间隔变小 8.B 解析:解:加入镁屑后气体出现膨胀而冷却后气球仍然膨胀,说明反应放出了气体;故A选项正确;本实验只涉及镁屑与盐酸的反应,并没有对比镁屑、镁条与盐酸的反应的情况,因此不能得到镁屑比镁条更快的结论;故B选项不正确;由于冷却后气球体积有所减小,说明反应放出热,放出的热量使氢气体积增大,冷却后体积又恢复到正常;故C选项正确;温度降低后,气体体积减小,可判断出分子间间隔减小;故D选项正确。 9.右图是不含结晶水的甲、乙两种固体物质的溶解度曲线,下列叙述错误的是( ) A.甲的溶解度大于乙的溶解度 B.t1℃时,配制等质量的甲乙两种物质的饱和溶液,需要相同体积的水 C.t2℃时,将甲、乙的饱和溶液降温至t1℃,肯定都有晶体析出 D.要从含有少量乙的甲溶液中得到较多的甲晶体,通常可采用降温结晶的方法 9.A 解析:从溶解度曲线图可知温度低于t1℃甲的溶解度小于乙的溶解度,温度高于t1℃时甲的溶解度大于乙的溶解度,故A选项说法不正确。t1℃时甲和乙的溶解度相等,饱和溶液中溶质质量分数相等,所以要配制相等质量的甲和乙的饱和溶液需要相同质量的溶质,溶液质量等于溶质质量加上溶剂质量,故所有用溶剂水质量相同,B选项说法正确;甲乙的溶解度都随温度的升高而降低,降低温度甲和乙的溶解度都减小,他们的饱和溶液都会结晶析出,C选项说法正确;甲是溶解度受温度影响较大的物质,可以采用冷却热饱和溶液的方法得到晶体;乙的溶解度受温度影响较小,降低温度几乎没有晶体析出或析出极少,所以D选项说法正确。 10.在一个密闭容器中放人甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表: 物质 甲 乙 丙 丁 10 反应前质量/g 18 1 2 32 反应后质量/g X(未知) 26 2 12 下列说法中,不正确的是 ( ) A.反应后物质甲的质量为13g B.乙是反应物 C.反应中乙、丁的质量比为5∶4 D.物质丙可能是该反应的催化剂 10.B 解析:反应前各物质的质量总和=反应后生成各物质的质量总和,则得:18g+1g+2g+32g=26g+2g+12g+x,解得x=13g;甲、丁的质量减少为反应物,乙的质量增加为生成物,丙的质量不变可能为催化剂;反应中乙、丁的质量比=(26g-1g):(32g-12g)=5∶4 故选项B不正确。 得分 评卷人 二、填空题(本题包括6个小题,每空1分,共16分) 11.2012年9月26日,在河南红茶评选活动中四大名旦“玫瑰红”、“玉兰红”、“牡丹红”、“菊花红”以“茶引花香,花增茶味”赢得好评。 (1)“闻香识茶”利用了分子 的性质。 (2)泡茶对水质的要求较高。通常可用 来鉴定软水和硬水。 11.不断运动 肥皂水 12.胡辣汤是河南人喜爱的汤类名吃之一,制作胡辣汤的主要原料有面粉、粉条、豆腐丝、胡椒粉、牛(羊)肉、食盐等,上述原料中富含糖类的是_______你认为还欠缺的营养素是__________。 12. 面粉(粉条) 维生素 13.右图为某反应的微观示意图,请回答: (1)反应后的物质是 (填 “纯净物”、“混合物”)。 (2)该反应的化学方程式为 。 13.(1)混合物 (2)2CO+ O2 2CO2 解析:从反应后的微观示意图推断,反应后图中有二氧化碳分子和氧分子,所以反应后的物质是混合物;通过对反应物和生成物的分子模型推断,反应物为一氧化碳和氧气,生成物为二氧化碳。 14.(10分)请结合图示实验装置,回答下列问题。 (1)某同学在实验室用B装置(多孔隔板用来放块状固体)制取二氧化碳,反应的化学方程式为 。B装置与A装置相比较,优点为 (答出一点即)。如用C装置收集CO2,则气体应从 10 端通入(填“c”或“d”)。 14. CaCO3+2HCl=CaCl2+CO2↑+H2O;可以随时控制反应的发生和停止(或随开随用、随关随停或减少酸的用量); C 解析: C装置是一个多用途装置,可用于洗气装置、干燥装置、气体收集装置。收集气体时,又可分为排水法与排空气法。排水法收集时,短进长出;排空气法收集气体时,若气体密度小于空气,则短进长出,若气体密度大于空气,则长进短出。 15.根据如图甲、乙、丙三种物质的转化关系,已知丙为一种常见金属,根据所学知识推断甲为__________,写出乙转化为丙的化学方程式:______________________________ 。 15. CuO Fe + CuSO4 == FeSO4 + Cu 解析:本题为框图式物质推断题,完成此题,关键是根据题干叙述,找准解题的突破口,直接得出有关物质的化学式,然后顺推或逆推或由两边向中间推,得出其他物质的化学式。丙是一种金属,能由铁(置换)反应生成,则丙在铁的后面,可能是铜,铜和氧气反应生成氧化铜,则甲可能是氧化铜,氧化铜与稀硫酸反应生成硫酸铜,硫酸铜能与铁反应生成硫酸亚铁和铜,代入框图,推断合理。 16.小明同学在家里做了如右图所示的小实验。 ① 图Ⅰ中观察到的主要现象是鸡蛋壳表面有气泡产生,蜡烛火焰熄灭。由此得出有关CO2性质的结论是 、 。并依此性质确定CO2的一个主要用途是 。 ② 当蜡烛熄灭后,在玻璃杯口迅速盖—块蘸有石灰水的玻璃片(见图Ⅱ)。观察到的现象是玻璃片上的石灰水 ,写出气体与石灰水反应的化学方程式 。 16. ①二氧化碳不支持燃烧、也不能燃烧;相同条件下密度比空气大。 二氧化碳气体能灭火。 ②变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O 得分 评卷人 三、简答题(本题包括4个小题,共14分) 17. 将铁粉在空气中洒向火盆,也有火星四射的现象产生。由此可知铁在空气中不能燃烧的结论是不够准确的。假设铁粉在空气中燃烧的产物和铁在纯氧气中燃烧的产物相同,请写出该反应的化学方程式: ,从铁丝在空气中不能燃烧,而铁粉在空气中却可以燃烧的事实中,你能得出的一个结论是 。 点燃 17. 3Fe + 2O2 Fe3O4 可燃物的表面积对能否燃烧有很大影响,或表面积越大越容易燃烧 18.几位同学理化生实验考试中做了氢氧化钠和稀盐酸的实验,考完后对两者反应后溶液中的溶质的组成进行了进一步的探究。甲同学猜想溶液中只含有氯化钠;乙同学猜想可能含有氯化钠、氢氧化钠和稀盐酸。 10 ①两位同学中有位同学的猜想是不正确的,请你帮他分析原因。 ②你再提出一个正确的猜想,并设计实验验证你的猜想。 18.(4分) ①乙同学猜想不合理; 因为NaOH和HCl会发生反应,不可能共存。 ②可能是NaCl和HCl(也可能是NaCl和NaOH);取少量反应后的溶液于试管中,向其中滴加石蕊试液,若试液变红,证明猜想成立(或即证明溶液呈酸性)。 19.(4分)物质的用途与其性质密切相关,研究金属的性质可以更好地利用金属。 (1) 铝的活动性比铁强,但是铝在空气中却表现出良好的抗蚀性,原因是什么? (2)为探究铝、铁、铜的活动性顺序,某同学设计了一组实验:①铝片浸入稀硫酸中; ②铜片浸入稀硫酸中;③铝片浸入硫酸亚铁溶液中。 这组实验还不能完全证明三种 金属的活动性顺序,请补充一个实验来达到目的(写出实验步骤、现象和化学方程式) 19.(1) 铝在常温下与空气中的氧气发生反应,使其表面生成一层致密的氧化铝薄膜, 阻止了内部的铝进一步被氧化。 (2分) (2) 将铁片浸入硫酸铜溶液中,铁片表面有红色固体析出。(1分) (或将铁片浸入稀硫酸中,有气泡产生等。) Fe + CuSO4==FeSO4 + Cu (或Fe + H2SO4== FeSO4 + H2↑等) (1分) 20.(3分)某同学用右图所示装置(集气瓶中事先装入少量的水)来测定空气中氧气的 含量。请回答下列问题: (1)该实验中燃烧物为什么用红磷? (2)实验完成后,若进入集气瓶中的水不足原空气体积的1/5, 你认为导致这一结果的原因可能是什么?(写一条即可) (3)如果实验室中没有红磷,该同学计划用木炭代替红磷进行实验,并对该实验稍作 修改即可,你认为他是如何修改的? 20.(1)只与氧气反应,产物是固体 (1分) (2)红磷的量不足或装置漏气等 (1分) (其他合理答案均可) (3)把集气瓶中的水改为氢氧化钠溶液 (1分) (其他合理答案均可) 解析:(1)测定空气中氧气的含量要保证反应物只与氧气反应,产物是固体。红磷燃烧只和空气中的氧气反应,且生成物是固体,符合条件;(2)若红磷的量不足,导致不能将装置内的氧气完全反应掉,因此测得氧气的体积分数小于1 /5 ;若装置漏气,导致空气进入集气瓶内,因此测得的氧气的体积分数小于1/5 ;若未等到装置冷却到室温,就打开止水夹,会使集气瓶内的气体处于膨胀状态,因此测得的氧气体积分数会小于1/5 ;(3)木炭燃烧生成气体二氧化碳,如果能够将二氧化碳气体吸收掉,照样可以使装置内气压减小,从而压迫外接液体进入装置内,所以就可以找吸收二氧化碳效果较好的氢氧化钠来进行实验。 得分 评卷人 四、 综合应用题(共10分) 21.天宫一号和神八对接成功,蛟龙号水下勘察作业突破7000米 10 ,是我国航天和航海史上国人引以为傲的大事件,在这其中,化学功不可没。例如用到了性能优越的合金材料。生活中也有很多地方用到合金,如生铁和钢是铁的合金。据所给内容回答问题: (1)从图1所示铁原子结构示意图可知,铁原子的核电荷数是 。 (2) 工业上,炼铁的原料是赤铁矿和焦炭,工业炼铁的反应原理是 (用化学方程式表示)。 (3)在化学实验室里,可以利用图2装置制得铁: ① 在装置B的反应中,实验开始前应先 (选填“通CO”或“加热”); 实验结束后应继续通入CO直至冷却至室温,其原因是 。 ②A、B处可观察到的实验现象是什么?C处酒精灯的作用是什么 (4)我国钢铁产量多年居世界第一位,每年要进口大量的铁矿石。1000t含氧化铁80%的赤 铁矿石,理论上可以炼出含杂质4%的生铁多少吨?(计算结果保留整数)。 四、综合应用题(共10分) 26.(1) 26, (2) Fe2O3+3CO2Fe+3CO2 (3) ① 通CO; 防止生成的铁被空气中的氧气氧化 ②A处红色粉末变成黑色;B处澄清石灰水变浑浊 除去尾气中的一氧化碳,防止污染空气 (4)解:设:1000t含氧化铁80%的赤铁矿石,理论上可以炼出含杂质4%的生铁的质量为х 10 Fe2O3+3CO2Fe+3CO2 160 112 1000t×80% (1-4%)х Х=583t 答:1000t含氧化铁80%的赤铁矿石,理论上可以炼出含杂质4%的生铁583t。 10 2013年河南省中考原创仿真模拟试卷化学答案 一、选择题(本题包括10小题,每小题1分,共10分) 1. D 2.C 3.C 4.C 5.D 6.C 7.C 8.B 9.A 10. B 二、填空题(本题包括6个小题,每空1分,共16分) 11.(1)在不断运动 (2)肥皂水 12.[ 面粉(粉条) 维生素 13.(1)混合物 (2)2CO+ O2 2CO2 14. CaCO3+2HCl=CaCl2+CO2↑+H2O;可以随时控制反应的发生和停止(或随开随用、随关随停或减少酸的用量); C 15. CuO Fe + CuSO4 == FeSO4 + Cu 16. ①二氧化碳不支持燃烧、也不能燃烧;相同条件下密度比空气大。 二氧化碳气体能灭火。 ②变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O。 三、简答题(本题包括4个小题,共14分) 点燃 17. 3Fe + 2O2 Fe3O4 可燃物的表面积对能否燃烧有很大影响,或表面积越大越容易燃烧 18.(4分) ①乙同学猜想不合理; 因为NaOH和HCl会发生反应,不可能共存。 ②可能是NaCl和HCl(也可能是NaCl和NaOH);取少量反应后的溶液于试管中,向其中滴加石蕊试液,若试液变红,证明猜想成立(或即证明溶液呈酸性)。 19.(1) 铝在常温下与空气中的氧气发生反应,使其表面生成一层致密的氧化铝薄膜, 阻止了内部的铝进一步被氧化。 (2分) (2) 将铁片浸入硫酸铜溶液中,铁片表面有红色固体析出。(1分) (或将铁片浸入稀硫酸中,有气泡产生等。) Fe + CuSO4==FeSO4 + Cu (或Fe + H2SO4== FeSO4 + H2↑等) (1分) 20.(1)只与氧气反应,产物是固体 (1分) (2)红磷的量不足或装置漏气等 (1分) (其他合理答案均可) (3)把集气瓶中的水改为氢氧化钠溶液 (1分) (其他合理答案均可) 四、综合应用题(共10分) 26.(1) 26, (2) Fe2O3+3CO2Fe+3CO2 (3) ① 通CO; 防止生成的铁被空气中的氧气氧化 ②A处红色粉末变成黑色;B处澄清石灰水变浑浊 除去尾气中的一氧化碳,防止污染空气 (4)解:设:1000t含氧化铁80%的赤铁矿石,理论上可以炼出含杂质4%的生铁的质量为х Fe2O3+3CO2Fe+3CO2 10 160 112 1000t×80% (1-4%)х Х=583t 答:1000t含氧化铁80%的赤铁矿石,理论上可以炼出含杂质4%的生铁583t。 10查看更多