- 2021-11-11 发布 |
- 37.5 KB |
- 10页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
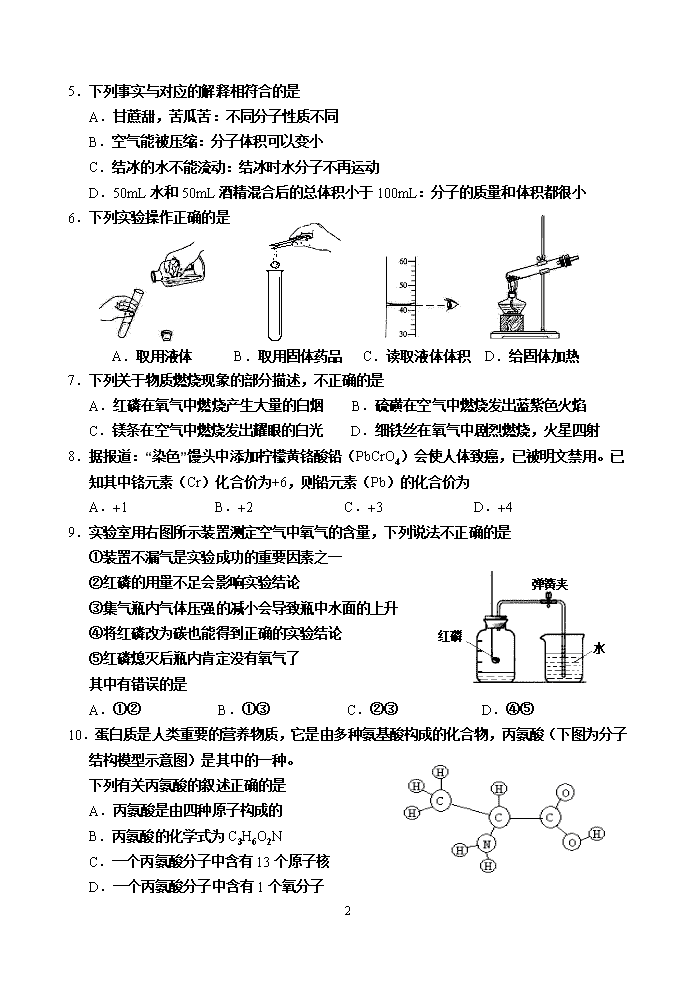
河西区2012-2013期中化学试卷
河西区2012—2013学年度第一学期九年级期中质量调查试卷 化 学 1.本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。第Ⅰ卷第1页至第3页,第Ⅱ卷第4页至第8页。试卷满分100分。考试时间70分钟。 2. 考生务必将答案写在“答题卡”上,答案答在试卷上无效。 祝各位考生考试顺利! 第Ⅰ卷 注意事项: 1.每题选出答案后,用2B铅笔把“答题卡”上对应题目的答案标号的信息点涂黑。 如需改动,用橡皮擦干净后,再选涂其他答案标号的信息点。 2.本卷共15题,共30分。 3.可能用到的相对原子质量:C 12 O 16 Ca 40 一、选择题(本大题共10题,每小题2分,共20分。每小题给出的四个选项中,只有一个最符合题意。) 1.2011年3月11日,日本发生了震惊世界的大地震。地震灾害过程中引发的下列变化中与其他三项有本质不同的是 A.山体滑坡 B.炸药爆炸 C.房屋倒塌 D.铁轨扭曲 2.汽车安全气囊必须在碰撞后10毫秒内释放出无毒、无味、对环境无污染、化学性质稳定的气体,气囊内充入的气体应该是 A.氮气 B.氧气 C.氢气 D.二氧化硫 3.美国发明了月球制氧机,它利用聚焦太阳光产生的高温使月球土壤发生化学反应放出氧 气。由此可推测月球土壤中一定含有 A.氧分子 B.水分子 C.氧元素 D.氯酸钾 4.下列符号中对“3”所表示的含义,说法不正确的是 Al—表示铝元素的化合价为+3 Al3+—表示一个铝离子带三个单位正电荷 3O2—表示三个氧分子 SO3—表示一个三氧化硫分子中含有三个氧元素 +3 A B C D 10 5.下列事实与对应的解释相符合的是 A.甘蔗甜,苦瓜苦:不同分子性质不同 B.空气能被压缩:分子体积可以变小 C.结冰的水不能流动:结冰时水分子不再运动 D.50mL水和50mL酒精混合后的总体积小于100mL:分子的质量和体积都很小 A.取用液体 B.取用固体药品 C.读取液体体积 D.给固体加热 6.下列实验操作正确的是 7.下列关于物质燃烧现象的部分描述,不正确的是 A.红磷在氧气中燃烧产生大量的白烟 B.硫磺在空气中燃烧发出蓝紫色火焰 C.镁条在空气中燃烧发出耀眼的白光 D.细铁丝在氧气中剧烈燃烧,火星四射 8.据报道:“染色”馒头中添加柠檬黄铬酸铅(PbCrO4)会使人体致癌,已被明文禁用。已知其中铬元素(Cr)化合价为+6,则铅元素(Pb)的化合价为 A.+1 B.+2 C.+3 D.+4 9.实验室用右图所示装置测定空气中氧气的含量,下列说法不正确的是 ①装置不漏气是实验成功的重要因素之一 弹簧夹 红磷 水 ②红磷的用量不足会影响实验结论 ③集气瓶内气体压强的减小会导致瓶中水面的上升 ④将红磷改为碳也能得到正确的实验结论 ⑤红磷熄灭后瓶内肯定没有氧气了 其中有错误的是 A.①② B.①③ C.②③ D.④⑤ 10.蛋白质是人类重要的营养物质,它是由多种氨基酸构成的化合物,丙氨酸(下图为分子 结构模型示意图)是其中的一种。 下列有关丙氨酸的叙述正确的是 A.丙氨酸是由四种原子构成的 B.丙氨酸的化学式为C3H6O2N C.一个丙氨酸分子中含有13个原子核 D.一个丙氨酸分子中含有1个氧分子 10 二、选择题(本大题共5题,每小题2分,共10分。每小题给出的四个选项中,有1~2个符合题意。) 11.逻辑推理是化学学习常用的思维方法,以下推理正确的是 A.在同一化合物中,金属元素显正价,所以非金属元素一定显负价 B. 氧化物只含有两种元素,所以氧化物中一定有一种元素不是氧元素 C.MnO2是加快H2O2分解的催化剂,所以催化剂是加快化学反应速率的物质 D.相同条件下,收集密度比空气小的气体(且该气体不与空气成分反应)一般可用向下排气法。能用向下排气法收集的气体的密度一定比空气小 12.下列四组物质中,均属于氧化物的是 A.一氧化碳、氧化镁、二氧化锰 B.水、二氧化硫、高锰酸钾 C.氧化亚铁、氧化铜、氧化汞 D.氧气、氧化钙、四氧化三铁 13.在“人吸入的空气和呼出的气体有什么不同”的探究中,下列说法不正确的是 A.证明呼出气体含水蒸气较多的证据是:呼出的气体在玻璃上结下水珠 B.证明呼出气体含有氮气的依据是:空气中含有氮气,而氮气不为人体吸收 C.证明呼出气体含氧气较少的证据是:呼出的气体使木条燃烧更旺 D.证明呼出气体含二氧化碳较多的证据是:呼出的气体使澄清石灰水更浑浊 14.密闭容器内有a、b、c、d四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示: 物质 a b c d 反应前质量/g 6.40 3.20 4.00 0.50 反应后质量/g x 2.56 7.20 0.50 下列说法不正确的是 A.表中x为0.64 B.X可能是该反应的催化剂 C.c中元素的种类等于a、b两种物质中元素的种类之和 高温 D.若a与b的相对分子质量之比为2:1,则反应中a与b的化学计量数之比为2:1 15.高温加热30g碳酸钙,一段时间后停止加热(已知:CaCO3 CaO + CO2↑),测得剩余固体中钙元素的质量分数为50%,反应生成的二氧化碳是 A.16.8g B.13.2g C.7.5g D.6g 10 第Ⅱ卷 注意事项: 1.用黑色墨水的钢笔或签字笔将答案写在“答题卡”上。 2.本卷共11题,共70分。 3.可能用到的相对原子质量:H 1 N 14 O 16 K 39 Mn 55 三、填空题(本大题共3小题 共20分) 16.(4分)请用数字和化学符号填空: (1)空气的成分按体积计算 约占空气体积的21%; (2)保持二氧化碳化学性质的最小粒子 ; (3)n个硫酸根离子 ; (4)相对分子质量最小的氧化物 。 17.(5分)用“ ” 和 “ ”分别代表两种不同的单质分子A2和B2,它们在一定 条件下能发生化学反应,其反应的微观示意图如下: 反应前 反应后 (1)该反应的基本反应类型是 ; (2)反应生成的物质是 (选填“单质”、“化合物”或“混合物”); (3)参加反应的B2与生成物分子的个数比为 ; (4)已知“ ”的相对原子质量是“ ”的m倍,则参加反应的A2与生成物的质量之比为 ; (5)生成物的化学式为 (用A、B表示)。 10 18.(11分)学习化学知识后,物质世界可用化学视角观察了。水是一种重要的物质, B.加热水 A.电解水 电源 a b 电源 a b - + 活塞 活塞 在日常生活和实验室中有着不可替代的作用。 请按要求回答下列问题(其中部分问题是据右图回答的): (1)从组成角度看:水是由 组成的。 a试管收集的是 。 (2)从微粒角度看:水是由 构成的。 用分子和原子的观点分析比较A装置和B装置在实验过程中 水的变化情况: 。 (3)从变化角度看:①写出A装置中发生反应的化学方 程式 。 ②水参加绿色植物光合作用可表示为: 叶绿素 光照 6CO2 + 6H2O 6O2 + X 则X的化学式为: 。 (4)①自来水生产过程中由吸附、沉淀和 的方法除去天然水中不溶性杂质,并吸附掉一些溶解的杂质,除去臭味。 ②地下水硬度过大会影响生产和生活,应先软化后使用。实验室区分硬水和软水常用的物质是 ,生活中常用 的方法降低水的硬度。 ③爱护水资源从我做起,下列做法可行的有 (选填序号)。 A.洗脸、刷牙时随时关闭水龙头 B.用洗菜、洗衣的水冲厕所、拖地 C.洗衣机洗衣服时尽量少放衣服 D.用残茶水浇灌某些花卉 四、简答题(本大题共3小题 共20分) 19.(8分)按要求完成下列化学方程式。 (1)白磷在空气中充分燃烧: ; (2)铁丝在氧气中燃烧: ; (3)氧化汞受强热分解: ; (4)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3): 。 10 20.(4分)对所学知识进行对比分析、归纳总结是学习化学的一种重要方法。 (1)在四种物质:SO2、C、Fe3O4、CuO中,有一种物质与众不同,该物质是 ,它与同组其他物质不同的原因是 。 高温 点燃 点燃 点燃 (2)在通风良好的煤炉中有许多化学反应,常见的有: ①2CO+O2 2CO2 ②S+O2 SO2 ③C+O2 CO2 ④CO2+C 2CO 通过比较,我们可以发现上述反应有许多相似之处(写出两点即可): 其一 ; 其二 。 21.(8分)下图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图。请回答下列问题: 17 Cl 氯 35.45 11 Na 钠 22.99 +11 2 8 1 +17 2 8 7 2 8 8 +17 +11 2 8 ① ② ③ ④ ⑤ +x 2 8 (1)氯元素原子的质子数是 ;钠元素与氯元素的最本质区别是 ;在元素周期表中,钠元素和氯元素位于 (选填序号)。 A.同一周期 B.不同周期 C.同一族 D.不同族 (2)上图①②③④四种粒子中,表示钠原子的是 (选填序号,下同);构成氯化钠的粒子是 。钠与氯气反应,每个 得到1个电子。 (3)若⑤表示Mg2+,则x = ,那么④和⑤相互作用形成的化合物的化学式是 。 五、实验题(本大题共3小题 共20分) 22.(4分)规范的实验操作是实验成功的前提,请回答: (1)用酒精灯给物质加热时,要使用酒精灯火焰的 。 (2)点燃可燃性气体时,都要先 ,再点燃。 (3)量取8mL5%的过氧化氢溶液,应选用 mL的量筒(选填“5mL”或“10mL”)。 10 (4)实验室用烧瓶制取蒸馏水时,烧瓶的底部应垫放 。 23.(13分)实验是学习化学的一个重要途径。根据给出的装置回答下列问题: A B C D E F a b ② ① ① (1)仪器①、②的名称是 、 。 (2)实验室用氯酸钾制取氧气时,若选用A和C分别作为发生装置和收集装置,停止加热时,必须先 ,反应的化学方程式是 ;实验室也可选用B作为制取氧气的发生装置,反应的化学方程式是 。 (3)以上两个反应所属基本反应类型都是 反应;以上两个反应都需使用二氧化锰,反应前后二氧化锰的质量和 都没有发生变化。 (4)若用排气法收集氧气,应选用 装置(填“D”或“E”),验满的方法是 。 (5)F装置的使用。若用F装置进行排水法收集氧气(瓶中已充满水),则气体应从 (填“a”或“b”,下同)口通入;若用F装置进行排空气法收集氢气,气体应从 口通入。 24.(3分)质量守恒定律的发现和发展对科学发展具有重大意义。 (1)用如下图所示的3个实验验证质量守恒定律,其中不能达到实验目的的是 (填序号),理由是 。 小气球 玻璃管 白磷 稀盐酸 碳酸钠固体 硫酸铜溶液 铁钉 A B C (2)在化学反应前后,一定变化的是 (填序号)。 a.原子种类 b.原子数目 c.分子种类 d.分子数目 e.元素种类 f.物质种类 10 六、计算题(本大题共2小题 共10分) 国内首创 优质硝酸铵NH4NO3 含氮量全球最高38% 25.(6分)林林在公共场所围墙上看到一则化肥广告(如下图),他通过计算判断出该广告是虚假广告,随后就向有关部门反映了。 (1)硝酸铵中各元素的质量比(最简)为: ; (2)已知该产品中的杂质不含氮元素,请你尝试写出林林 的计算过程和判断依据。(请写出详细的计算过程) (3)技术监督局对该产品进行取样分析,发现氮元素的质量分数仅为28%。请计算该产品中硝酸铵的质量分数。(请写出详细的计算过程) 26.(4分)某同学为测定一高锰酸钾样品的纯度进行了以下实验。取该高锰酸钾样品10g,放在试管中加热至完全反应,冷却后,称得剩余固体质量为9.04g。请计算: (1)反应中产生的氧气的质量; (2)该高锰酸钾样品的纯度。 10 河西区2012—2013学年度第一学期九年级期中质量调查 化学试题参考答案及评分标准 一、选择题(每题2分,共20分) 题号 1 2 3 4 5 6 7 8 9 10 答案 B A C D A C B B D C 二、选择题(每题2分,共10分) 题 号 11 12 13 14 15 答 案 BD AC C A D 三、填空题(3小题,共20分)(每空1分) 16.(4分) (1)O2 (2)CO2 (3)nSO42- (4)H2O 17.(5分) (1)化合反应 (2)化合物 (3)1:2 (4)3:( m +3) (5)BA3或A3B 18.(11分) (1)氢、氧两种元素 氢气 (2)水分子 A中的水分子发生了改变,构成水分子的氢原子和氧原子重新组合成 通电 氢气分子和氧气分子;B中的水分子本身没有改变,改变的是分子之间的间隔 (3)① 2H2O 2H2 ↑+ O2 ↑ ②C6H12O6(不考虑元素符号排序) (4)①过滤 ②肥皂水 煮沸 ③ABD 四、简答题(3小题,共20分)(化学方程式每个2分,其余每空1分) 点燃 点燃 19.(8分) (1)4P + 5O2 2P2O5 (2)3Fe + 2O2 Fe3O4 强热 (3)2HgO 2Hg + O2↑ (4)N2+3H2 2NH3 20.(4分) (1)SO2 只有它是气体 (或答“C ,只有它是单质”等) (2)都是化合反应 生成物都是氧化物 21.(8分) (1)17 原子核内质子数不同(或答“核电荷数不同”) AD (2)② ①④ ③ (3)12 MgCl2 五、实验题(3小题,共20分)(化学方程式每个2分,其余每空1分) 10 22.(4分) (1)外焰 (2)验纯 (3)10 (4)石棉网 23.(13分) △ MnO2 MnO2 (1)长颈漏斗 集气瓶 (2)把导管移出水面 2KClO3 2KCl+3O2↑ 2H2O2 O2↑+2H2O (3)分解 化学性质(写“性质”不给分) (4)E 用带火星木条靠近集气瓶口,如木条立即复燃,则氧气已经集满 (5)b b 24.(3分) (1)B 装置未密闭,生成的CO2气体逸出,导致左盘中容器内物质总质量减小 (2)cf 六、计算题(2小题,共10分) 25.(6分) (1)m(N):m(H):m(O) = 7:1:12 (1分) (2)NH4NO3的相对分子质量 = 80 NH4NO3中氮元素的质量分数= (1分) 因为纯硝酸铵中氮元素的质量分数小于38%,所以该广告是虚假的。 (1分) (3)设该产品为100g,其中氮元素的质量为:100g×28%=28g (1分) m(NH4NO3)= (1分) 产品中硝酸铵的质量分数为: (1分) 26.(4分) (1)生成O2的质量为:10g - 9.04g = 0.96g (1分) △ (2)设高锰酸钾样品中高锰酸钾的质量为x。 2KMnO4△ K2MnO4 + MnO2 + O2↑ 316 32 x 0.96g (1分) x=9.48g (1分) 高锰酸钾样品的纯度为: (1分) 答:生成O2的质量是0.96g,高锰酸钾样品的纯度是94.8%。 10查看更多