- 2021-11-06 发布 |
- 37.5 KB |
- 5页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
徐州专版2020中考化学复习方案第4章认识化学变化专项06质量守恒定律应用试题
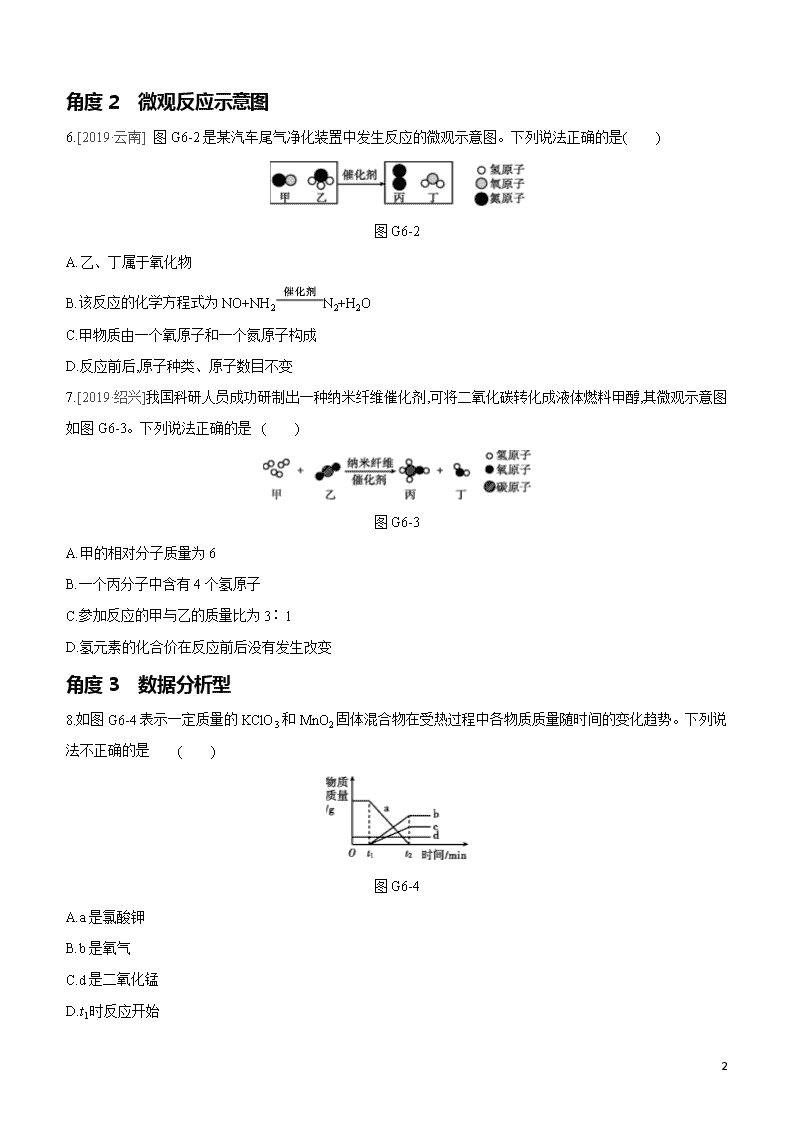
专项(六) 质量守恒定律应用 角度1 确定物质化学式及元素组成 1.过氧化钠(Na2O2)可作呼吸面具中氧气的来源,它与二氧化碳反应后的生成物为 ( ) A.Na2CO3和H2 B.Na2O和O2 C.NaOH和O2 D.Na2CO3和O2 2.[2019·广州]超氧化钾(KO2)常备于急救器和消防队员的背包中,能迅速与水反应放出氧气:2KO2+2H2O2KOH+X+O2↑。关于此反应的说法不正确的是 ( ) A.X的化学式为H2O2 B.反应前后元素种类发生变化 C.反应前后氧元素化合价发生变化 D.反应前后物质状态发生变化 3.[2019·天津]在化学反应A+2BC+2D中,已知16 g A与64 g B恰好完全反应,生成C和D的质量比为11∶9,又知B的相对分子质量为32,则D的相对分子质量为 ( ) A.9 B.12 C.18 D.36 4.某有机物在9.6 g氧气中恰好完全燃烧,生成8.8 g CO2和5.4 g H2O,下列说法正确的是 ( ) A.该有机物只含碳、氢两种元素 B.该有机物中一定含有碳、氢元素,可能含有氧元素 C.该有机物中一定含有碳、氢、氧三种元素 D.无法确定 5.物质X在5 g的氧气中充分燃烧,反应方程式为X+3O2RO2+2SO2,测得生成RO2和SO2的质量分别为2.2 g和6.4 g,下列判断中正确的是 ( ) A.X的相对分子质量为76 B.X中含有R、S、O三种元素 C.参加反应的X的质量为4.3 g D.X与氧气恰好完全反应 5 角度2 微观反应示意图 6.[2019·云南] 图G6-2是某汽车尾气净化装置中发生反应的微观示意图。下列说法正确的是( ) 图G6-2 A.乙、丁属于氧化物 B.该反应的化学方程式为NO+NH2N2+H2O C.甲物质由一个氧原子和一个氮原子构成 D.反应前后,原子种类、原子数目不变 7.[2019·绍兴]我国科研人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图G6-3。下列说法正确的是 ( ) 图G6-3 A.甲的相对分子质量为6 B.一个丙分子中含有4个氢原子 C.参加反应的甲与乙的质量比为3∶1 D.氢元素的化合价在反应前后没有发生改变 角度3 数据分析型 8.如图G6-4表示一定质量的KClO3和MnO2固体混合物在受热过程中各物质质量随时间的变化趋势。下列说法不正确的是 ( ) 图G6-4 A.a是氯酸钾 B.b是氧气 C.d是二氧化锰 D.t1时反应开始 5 9.[2019·滨州]在密闭容器内,有甲、乙、丙、丁四种物质。在一定条件下充分反应,测得反应前后各物质的质量分数如图G6-5所示,下列说法错误的是 ( ) 图G6-5 A.该反应符合质量守恒定律 B.生成的甲、丙两物质的质量比为8∶1 C.乙可能是该反应的催化剂 D.参加反应的丁的质量等于生成的甲和丙的质量之和 10.[2019·龙东]在密闭容器内有氧气、二氧化碳、水蒸气和一种未知物质W,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,则下列说法中正确的是 ( ) 物质 氧气 二氧化碳 水蒸气 W 反应前质量/g 50 1 1 23 反应后质量/g 2 45 28 x A.根据质量守恒定律,x的值应为2 B.该反应属于置换反应 C.该反应中的二氧化碳和水蒸气的质量比为44∶27 D.该反应中物质W含碳元素的质量为10 g 11.在一密闭容器中发生某反应,容器中各物质质量变化如表所示,其中未知数据错误的是 ( ) 物质 阶段 甲的质量/g 乙的质量/g 丙的质量/g 丁的质量/g 反应前 40 40 0 0 反应中 m1 m2 m3 10.8 反应后 23 m4 30 27 A.m1=33.2 B.m2=24 C.m3=10 D.m4=0 5 【参考答案】 典题训练 角度1 1.D 2.B [解析]由反应前后原子的种类和个数不变,可知X的化学式为H2O2;由质量守恒定律可知,反应前后元素的种类不变;化合物中氧元素的化合价为-2,单质中氧元素的化合价为0,反应前后氧元素化合价发生变化;反应前物质为固体和液体,反应后有气体生成,物质状态发生了变化。 3.C [解析]在化学反应A+2BC+2D中,已知16 g A与64 g B恰好完全反应,根据质量守恒定律,生成的C和D的质量之和为16 g+64 g=80 g,又因为生成C和D的质量之比为11∶9,所以D的质量是80 g×920=36 g,已知B的相对分子质量为32,设D的相对分子质量为x,则: A+2BC+2D 64 2x 64 g 36 g 642x=64 g36 g x=18 4.C [解析]由质量守恒定律,反应前后元素种类不变,该物质中一定含有碳元素和氢元素。8.8 g CO2中含有氧元素的质量为8.8 g×16×244×100%=6.4 g,5.4 g H2O中含有氧元素的质量为5.4 g×1618×100%=4.8 g,生成物8.8 g二氧化碳和5.4 g水中所含氧元素的质量和为6.4 g+4.8 g=11.2 g,该有机物中含氧元素的质量为11.2 g-9.6 g=1.6 g,则该有机物中一定含有碳、氢、氧三种元素。 5.A [解析]根据反应的化学方程式可得知,生成物的分子中共含有6个O原子,而反应物的3个O2中含有6个O原子,因此,X物质中不含O元素,B错误;根据X+3O2RO2+2SO2和质量守恒定律,参加反应的X的质量为(2.2 g+6.4 g)-4.8 g=3.8 g≠4.3 g,C错误;根据化学方程式计算可知,参加反应的氧气的质量为4.8 g,没有完全反应,D错误。 角度2 6.D [解析] 由反应的微观示意图可以看出,反应物是NH3和NO两种分子,生成物是N2和H2O两种分子,化学方程式为6NO+4NH35N2+6H2O。乙是NH3,不是氧化物;甲物质是由一氧化氮分子构成的;反应前后,原子种类、原子数目不变。 7.B [解析]由题目信息和质量守恒定律可知,该反应为二氧化碳和氢气在催化剂作用下反应生成甲醇和水,反应的化学方程式为3H2+CO2CH3OH+H2O。甲为氢气,甲的相对分子质量为2;由微粒的构成可知,一个 5 丙分子中含有4个氢原子;由上述反应可知,参加反应的甲、乙两物质的分子个数比为3:1,质量比是(2×3):44=3:22;该反应有氢气单质参加,有水生成,氢元素的化合价一定发生了变化。 8.B [解析]反应物是氯酸钾,质量从反应开始会不断减少,故a是氯酸钾,A正确;生成氧气和氯化钾的质量不断增加,根据化学方程式的计算可知,生成氯化钾的质量要比氧气的质量多,故b是氯化钾,B错误;二氧化锰在反应中为催化剂,反应前后质量不变,d是二氧化锰,C正确;t1时a的质量开始减少,说明反应开始发生,D正确。 9.B [解析]由图可知,18份质量的丁发生化学反应生成2份质量的甲和16份质量的丙,乙在该反应前后质量没有发生变化,可能是该反应的催化剂。一切化学反应都符合质量守恒定律,故A正确;通过分析计算可知生成甲、丙的质量比为1∶8,故B错误;乙在反应前后的质量没有发生变化,所以乙可能是该反应的催化剂,故C正确;该反应是分解反应,根据质量守恒定律,参加反应的丁的质量等于生成的甲和丙的质量和,故D正确。 10.C [解析]根据质量守恒定律,x=(50+1+1+23)-(2+45+28)=0;置换反应的生成物中有一种是单质,而二氧化碳和水都是化合物;生成物二氧化碳中的碳元素全部来自于W,生成的二氧化碳中碳元素的质量为44 g×1244=12 g。 11.C [解析]17∶27=(40-m1)∶10.8,m1=33.2;40∶27=(40-m2)∶10.8,m2=24;30∶27=m3∶10.8,m3=12;m4=40+40-30-27-23=0。 5查看更多