- 2021-11-06 发布 |
- 37.5 KB |
- 5页


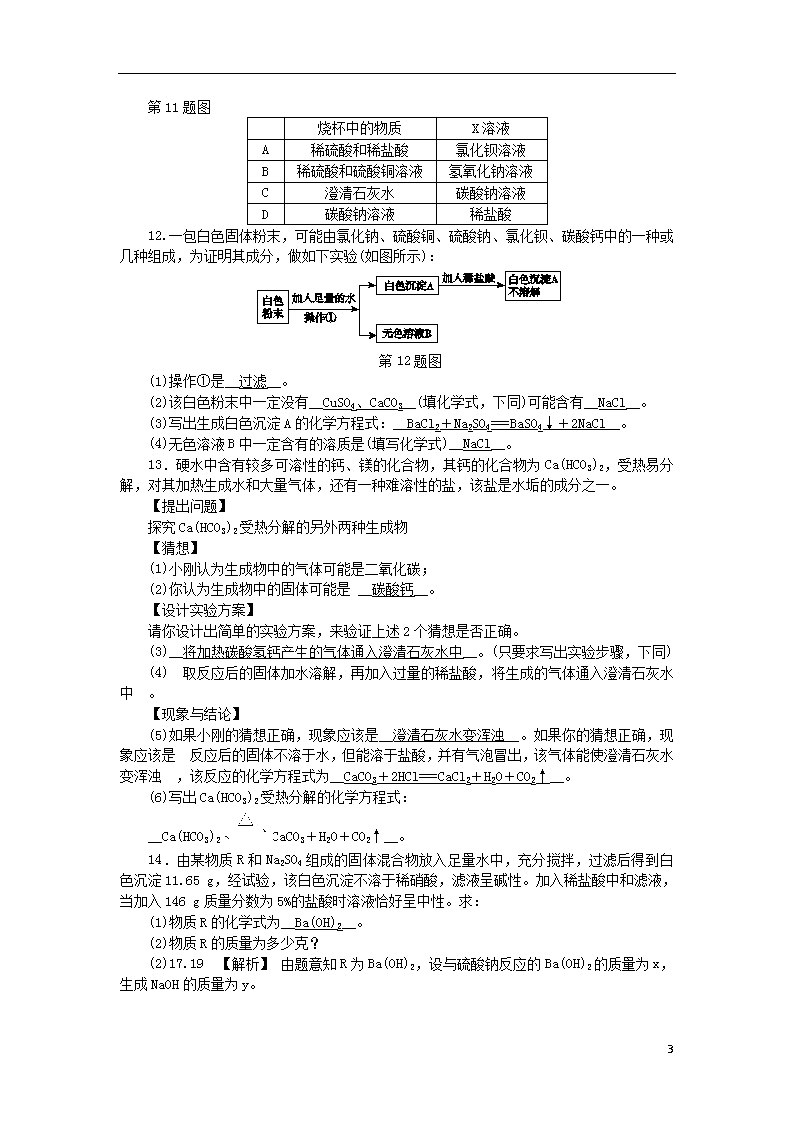
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020九年级科学上册第1章物质及其变化第6节几种重要的盐第1课时什么是盐练习
第6节 几种重要的盐 (见A本9页) 第1课时 什么是盐 1.盐:电离时能产生__金属离子__(或铵根离子)和__酸根离子__的化合物。 2.几种重要的盐 (1)碳酸钠(Na2CO3):俗称__纯碱、苏打__。晶体的化学式为Na2CO3·10H2O,在干燥的空气中容易失去结晶水而变成碳酸钠粉末。Na2CO3虽然是盐,但其水溶液却显__碱性__,因而俗称纯碱。 (2)碳酸钙(CaCO3):洁白纯净的碳酸钙岩石叫作__汉白玉__。可直接用来作装饰性的石柱或工艺品。因含杂质而有美丽花纹的碳酸钙叫作__大理石__,用来作建筑物外墙和内壁的贴面或铺设地面,但石灰石的主要用途是生产水泥和__石灰__。 (3)氯化钠(NaCl)是__食盐__的主要成分,是一种白色的晶体,易溶于水。摄入过多的食盐容易引起高血压等疾病,浓的食盐溶液具有__杀菌__作用。 A 练就好基础 基础达标 1.下列物质中,属于盐的是( C ) A. 硫酸(H2SO4) B.氢氧化钠(NaOH) C.碳酸钠(Na2CO3) D.四氧化三铁(Fe3O4) 2.下列每组物质(主要成分)的名称、俗称、化学式三者不能表示同一种物质的是( D ) A. 氯化钠、食盐、NaCl B.硫酸铜晶体、胆矾、CuSO4·5H2O C.碳酸钠晶体、纯碱晶体、Na2CO3·10H2O D.氧化钙、熟石灰、CaCO3 3.下列有关纯碱的说法正确的是( C ) A. 纯碱溶液呈中性 B.纯碱是碱而不是盐 C.纯碱晶体是含有结晶水的纯净物 D.纯碱难溶于水 4.将鸡蛋壳加入稀盐酸中有气泡产生, 5 生成的气体能使澄清的石灰水变浑浊。据此判断鸡蛋壳中含( C ) A. 氯离子 B.硫酸根离子 C.碳酸根离子 D.氢氧根离子 5.下列各组物质,只需用水就可鉴别出来的是( C ) A. 氯化钠和蔗糖 B.氯化铜和硫酸铜 C.硫酸钡和硫酸钠 D.氯化钠和硝酸钾 6.新鲜鱼肉用食盐腌渍不容易变质,其主要原因是( C ) A. NaCl溶液中的Cl-有杀菌作用 B.浓NaCl溶液O2少,细菌无法生存 C.由于渗透作用使细菌失水死亡 D.由于渗透作用使鱼肉细胞失水所致 第7题图 7.如图是实验室里一瓶标签破损的白色粉末状固体。王丽同学取出少量该固体放入一洁净试管中,加水振荡后固体溶解,形成无色透明溶液,继续加入少量盐酸,有无色无味的气体产生,则该固体可能是( C ) A. Na2SO4 B.NaCl C.Na2CO3 D.NaOH 8.将下列试剂分别加入KOH溶液、饱和石灰水和稀H2SO4中,能出现三种不同现象的是( B ) A. 紫色石蕊试液 B.Na2CO3溶液 C.CuCl2溶液 D.NaCl溶液 B 更上一层楼 能力提升 9.分离MgCl2、NaCl、AgCl可选用的一组试剂是( D ) A. 水、KOH溶液、稀硫酸 B.水、NaOH溶液、稀硫酸 C.水、KOH溶液、稀盐酸 D.水、NaOH溶液、稀盐酸 10. 对于某些离子的检验及结论一定正确的是( C ) A. 加入稀盐酸产生无色气体,一定有CO B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO C.加入硝酸银溶液有白色沉淀,不一定有Cl- D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ 11.向烧杯中逐滴加入X溶液至过量(如图甲),生成沉淀或气体的质量与加入X溶液的质量关系符合图乙的是( B ) 5 第11题图 烧杯中的物质 X溶液 A 稀硫酸和稀盐酸 氯化钡溶液 B 稀硫酸和硫酸铜溶液 氢氧化钠溶液 C 澄清石灰水 碳酸钠溶液 D 碳酸钠溶液 稀盐酸 12.一包白色固体粉末,可能由氯化钠、硫酸铜、硫酸钠、氯化钡、碳酸钙中的一种或几种组成,为证明其成分,做如下实验(如图所示): 第12题图 (1)操作①是__过滤__。 (2)该白色粉末中一定没有__CuSO4、CaCO3__(填化学式,下同)可能含有__NaCl__。 (3)写出生成白色沉淀A的化学方程式:__BaCl2+Na2SO4===BaSO4↓+2NaCl__。 (4)无色溶液B中一定含有的溶质是(填写化学式)__NaCl__。 13.硬水中含有较多可溶性的钙、镁的化合物,其钙的化合物为Ca(HCO3)2,受热易分解,对其加热生成水和大量气体,还有一种难溶性的盐,该盐是水垢的成分之一。 【提出问题】 探究Ca(HCO3)2受热分解的另外两种生成物 【猜想】 (1)小刚认为生成物中的气体可能是二氧化碳; (2)你认为生成物中的固体可能是 __碳酸钙__。 【设计实验方案】 请你设计出简单的实验方案,来验证上述2个猜想是否正确。 (3)__将加热碳酸氢钙产生的气体通入澄清石灰水中__。(只要求写出实验步骤,下同) (4) 取反应后的固体加水溶解,再加入过量的稀盐酸,将生成的气体通入澄清石灰水中 。 【现象与结论】 (5)如果小刚的猜想正确,现象应该是__澄清石灰水变浑浊__。如果你的猜想正确,现象应该是 反应后的固体不溶于水,但能溶于盐酸,并有气泡冒出,该气体能使澄清石灰水变浑浊 ,该反应的化学方程式为__CaCO3+2HCl===CaCl2+H2O+CO2↑__。 (6)写出Ca(HCO3)2受热分解的化学方程式: __Ca(HCO3)2CaCO3+H2O+CO2↑__。 14.由某物质R和Na2SO4组成的固体混合物放入足量水中,充分搅拌,过滤后得到白色沉淀11.65 g,经试验,该白色沉淀不溶于稀硝酸,滤液呈碱性。加入稀盐酸中和滤液,当加入146 g质量分数为5%的盐酸时溶液恰好呈中性。求: (1)物质R的化学式为__Ba(OH)2__。 (2)物质R的质量为多少克? (2)17.19 【解析】 由题意知R为Ba(OH)2,设与硫酸钠反应的Ba(OH)2的质量为x,生成NaOH的质量为y。 5 Ba(OH)2+Na2SO4===BaSO4↓+2NaOH 171 233 80 x 11.65 g y 171/x=233/ 11.65 g 233 /11.65 g=80/y 解得x=8.55 g y=4.00 g 设4.00 g NaOH消耗HCl的质量为z。 HCl+NaOH===NaCl+H2O 36.5 40 z 4.00 g 36.5/z=40 /4.00 g 解得z=3.65 g 向滤液中共加入盐酸的质量为146 g×5%=7.3 g,而与氢氧化钠反应的盐酸的质量为3.65 g,所以HCl还与剩余的Ba(OH)2反应。设剩余的Ba(OH)2的质量为w。 Ba(OH)2+2HCl===BaCl2+2H2O 171 73 w 7.3 g-3.65 g 171/w=73 /(7.3 g-3.65 g) 解得w=8.55 g 所以共有氢氧化钡的质量为8.55 g+8.55 g=17.1 g。 C 开拓新思路 拓展创新 15.某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红。碱溶液可以使酚酞溶液变红,是因为碱在水溶液中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞溶液变红呢?他们设计了下图3个实验,请你和他们一起探究。 第15题图 (1)实验Ⅰ可以探究__Na+是否能使酚酞试液变红__。 (2)实验Ⅱ加入蒸馏水的目的是__探究水分子是否能使酚酞试液变红__小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是__酚酞试液中就有水分子(或氯化钠溶液中含有水分子)__。 (3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞溶液变红,向变红后的溶液中再逐渐滴入过量的CaCl2溶液,红色逐渐消失,同时还观察到__白色沉淀__现象。由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO可以使酚酞溶液变红。 (4)小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞溶液变红也是由于溶液中存在OH-。”你认为Na2CO3溶液存在OH-的原因是__ CO与H2O发生反应产生OH-(合理即可)__。 5 5查看更多