- 2022-04-01 发布 |
- 37.5 KB |
- 33页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
呼和浩特专版2020中考化学复习方案实验突破04空气中氧气含量的测定课件 13225
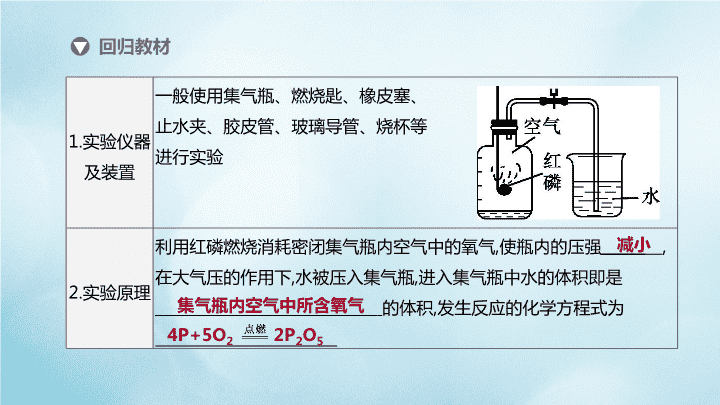
实验突破(四)空气中氧气含量的测定 回归教材1.实验仪器及装置一般使用集气瓶、燃烧匙、橡皮塞、止水夹、胶皮管、玻璃导管、烧杯等进行实验2.实验原理利用红磷燃烧消耗密闭集气瓶内空气中的氧气,使瓶内的压强,在大气压的作用下,水被压入集气瓶,进入集气瓶中水的体积即是的体积,发生反应的化学方程式为减小4P+5O22P2O5集气瓶内空气中所含氧气 3.实验步骤(1)检查装置的(2)在集气瓶中加入少量水,再把水面以上的部分分成五等份并做上记号(3)点燃的红磷,立即伸入瓶中,把塞子塞紧(4)红磷燃烧停止后,冷却到,打开止水夹,观察现象4.实验现象(1)红磷燃烧,产生,放出热量(2)烧杯中的水进入集气瓶内,进入集气瓶内水的体积约占集气瓶中原空气体积的________(续表)气密性燃烧匙内过量(或足量)室温大量白烟 5.实验结论氧气约占空气体积的推论:氮气难溶于水、不能燃烧也不支持燃烧补充:氮气的化学性质(氮气可用于医疗手术,作食品保护气等)不活泼(续表) 6.误差分析(1)结果偏小:①装置漏气②③等(2)结果偏大:①红磷点燃后,燃烧匙伸入瓶中速度过慢,未及时塞紧瓶塞②未夹(或未夹紧)止水夹红磷量不足装置未冷却至室温就打开止水夹(续表) 7.装置改进装置优点:装置密闭,无污染,测量结果更准确(续表) 1.某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究。(1)用如图S4-1甲所示装置和药品进行实验,冷却至室温后打开止水夹,可观察到的现象是。若观察到结果小于预期值,则可能是因为。拓展训练图S4-1水进入集气瓶至第一刻度处红磷量不足(或装置漏气或没有冷却至室温就打开止水夹等,合理即可) (2)小组内同学还对该实验进行了如图乙所示的改进。(已知试管容积为45mL)请结合实验目的,在以下的操作中排出正确的实验操作顺序(填序号)。①点燃酒精灯。②撤去酒精灯,待试管冷却后松开弹簧夹。③将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图中所示的连接方式固定好,再用弹簧夹夹紧胶皮管。④读取注射器活塞的数据。最终注射器活塞将从10mL刻度处慢慢前移到约为mL刻度处才停止。③①②④图S4-11 2.[2019·安徽模拟]某实验小组对教材内测量空气中氧气体积分数的实验进行改进,并取得成功(装置如图S4-2所示)。实验准备具支试管和小气球内空气总体积为50mL,注射器中留下的空气体积为50mL,该装置气密性良好。实验探究装入药品,按图所示连接好仪器。用酒精灯在红磷部位加热,加热时不断推拉注射器活塞,气球忽大忽小,并不断将气球中的气体全部挤入试管中。现象分析图S4-2 (1)实验开始时应先检查装置气密性。连接装置后且其气密性良好,若将注射器向内推,可观察到气球变(填“大”或“小”)。(2)加热试管底部,红磷被引燃,说明燃烧不能缺少的一个条件是,足量的红磷在试管中未能全部燃烧,说明试管内剩余气体具有的化学性质为。写出红磷燃烧的化学方程式:。大温度达到着火点不燃烧也不支持燃烧(或不与红磷反应) 2.[2019·安徽模拟]某实验小组对教材内测量空气中氧气体积分数的实验进行改进,并取得成功(装置如图S4-2所示)。实验准备具支试管和小气球内空气总体积为50mL,注射器中留下的空气体积为50mL,该装置气密性良好。实验探究装入药品,按图所示连接好仪器。用酒精灯在红磷部位加热,加热时不断推拉注射器活塞,气球忽大忽小,并不断将气球中的气体全部挤入试管中。现象分析图S4-2 (3)实验结束后,停止加热,待试管冷却至室温,将气球内的气体全部挤入注射器内,待注射器活塞稳定后,读取注射器内剩余气体的体积为mL。得出结论氧气约占空气总体积的。反思评价实验中,加热时不断推拉注射器的目的为____________________________;此实验与课本实验比较的优点为。30充分耗尽空气中的氧气,使实误差小(或无污染,合理即可)验结果更准确 3.[2019·兰州节选]利用如图S4-3甲所示装置测定空气中氧气的含量并结合现代传感器技术,测得过程中容器内气体压强、温度、氧气浓度的变化趋势如图乙所示。(1)t2时打开止水夹,最终集气瓶中水平面大约上升至刻度处。图S4-3 [答案](1)1[解析](1)空气中氧气的体积大约占总体积的,红磷燃烧消耗集气瓶中的氧气生成固体五氧化二磷,燃烧结束,冷却至室温后,打开止水夹,烧杯中的水进入集气瓶,进入瓶中水的体积等于燃烧消耗氧气的体积,图中t2时温度恢复至室温,最终集气瓶中液面大约上升至刻度1处。 3.[2019·兰州节选]利用如图S4-3甲所示装置测定空气中氧气的含量并结合现代传感器技术,测得过程中容器内气体压强、温度、氧气浓度的变化趋势如图乙所示。(2)结合曲线,AB段气体压强变化的原因是。图S4-3 [答案](2)红磷燃烧放热,集气瓶中温度升高,气体体积增大,导致压强增大[解析](2)图中AB段气体压强增大,原因是红磷燃烧放热,集气瓶中温度升高,气体体积增大,压强增大。 4.[2019·安徽模拟]兴趣小组借助如图S4-4所示装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积分数。(1)实验前用砂纸打磨铁钉至光亮的目的是。(2)已知试管剩余空间和导管的体积为20mL,导管截面积约为1cm2,充分反应后,形成稳定液柱时,读取读数为4.1cm,则空气中氧气的体积分数为%(保留至小数点后一位)。去除铁钉表面的铁锈图S4-420.5 4.[2019·安徽模拟]兴趣小组借助如图S4-4所示装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积分数。(3)实验时发现上述测量过程因反应较慢耗时较长,现对影响铁生锈速率的因素作如下分析:提出假设假设一:溶液的酸碱度;假设二:NaCl溶液的浓度;请你再提出一种影响铁生锈快慢的因素。假设三:。实验探究借助上述实验装置,通过控制铁钉用量等其他条件均相同时,调节溶液的pH获得了下表所示实验数据:图S4-4温度(或铁的形状等,合理即可) 实验结论根据实验数据分析,为缩短实验测定时间,pH的最佳范围是;还可以采取何种方法进一步缩短实验时间:(答一条即可)。实验反思当pH=2时,没有观察到稳定液柱形成的原因是______________________。pH2.05.56.06.57.08.0液柱高度/cm00.64.14.14.14.1形成稳定液柱时间/min3.03.05.15.315.617.56.0~6.5用铁粉代替铁钉(合理即可)pH等于2时酸性较强,铁与酸反应产生H2,导致装置内压强增大 5.[2019·福建]某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。实验1按图S4-5甲所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。实验2按图乙所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。(1)实验1中,红磷燃烧的主要现象是。红磷熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因是。图S4-5 [答案](1)产生大量白烟,放出热量 氧气被消耗,集气瓶内气体压强小于外界大气压[解析](1)实验1中红磷燃烧产生大量白烟,待集气瓶冷却后,打开K,由于氧气被消耗,集气瓶内气体压强小于外界大气压,导致水倒吸入集气瓶。 5.[2019·福建]某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。实验1按图S4-5甲所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。实验2按图乙所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。(2)为提高实验的准确性,以上两个实验都需要注意的事项是(写一点)。图S4-5 [答案](2)装置的气密性良好(或红磷和铁粉除氧剂足量,合理即可)[解析](2)实验1和实验2都应注意装置的气密性良好,反应物应足量等事项,从而提高实验的准确性。 5.[2019·福建]某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。实验1按图S4-5甲所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。实验2按图乙所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。图S4-5 (3)实验过程中,连接数字传感器,测得实验1、实验2中氧气的体积分数随时间变化的关系分别如图S4-6丙、丁所示。依据图丙、丁所示信息,(填“实验1”或“实验2”)的测定方法更准确,判断依据是。图S4-6 [答案](3)实验2反应后,实验1集气瓶中剩余氧气的体积分数为8.6%,而实验2集气瓶中氧气几乎耗尽[解析](3)分析图丙和图丁信息可知,实验2的测定方法更准确,因为实验1中集气瓶剩余氧气的体积分数约为8.6%,而实验2集气瓶中氧气几乎耗尽。 5.[2019·福建]某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。实验1按图S4-5甲所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。实验2按图乙所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。(4)结合你的学习经验,若要寻找红磷或铁粉除氧剂的替代物,用图甲或图乙装置测定空气中氧气的体积分数,该替代物应满足的条件是(写两点)。实验3测定用排空气法收集到的集气瓶中二氧化碳的体积分数。图S4-5 [答案](4)能够和氧气反应;生成物不影响测定结果(合理即可)[解析](4)通过上述实验可知,若要寻找红磷或铁粉除氧剂的替代物,该物质应能和氧气反应,且生成物不能为气体,不影响测定结果。 5.[2019·福建]某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。实验1按图S4-5甲所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。实验2按图乙所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。图S4-5 (5)甲同学设计图S4-7戊所示装置进行测定。浓NaOH溶液的作用是(用化学方程式表示)。图S4-7 [答案](5)2NaOH+CO2Na2CO3+H2O[解析](5)实验3测定排空气法收集到的集气瓶中二氧化碳的体积分数,用浓氢氧化钠溶液吸收二氧化碳,即2NaOH+CO2Na2CO3+H2O,从而导致集气瓶内气体压强减小,烧杯内水倒吸入集气瓶,进入集气瓶中水的体积即为二氧化碳的体积。 5.[2019·福建]某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。实验1按图S4-5甲所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。实验2按图乙所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。(6)乙同学提出,仅利用图己所示装置,在不添加其他试剂的前提下,也能测得集气瓶中二氧化碳的体积分数。为达到实验目的,操作方法是。图S4-5 [答案](6)用冰水冷却集气瓶,打开K(合理即可)[解析](6)为了使烧杯内的氢氧化钠溶液被倒吸,必须使集气瓶内压强减小,可用冰水冷却集气瓶,使瓶内压强减小,再打开K。查看更多