2020届高考化学一轮复习物质结构元素周期律高考真题作业
1.(2018·江苏高考)用化学用语表示NH3+HCl===NH4Cl中的相关微粒,其中正确的是( )
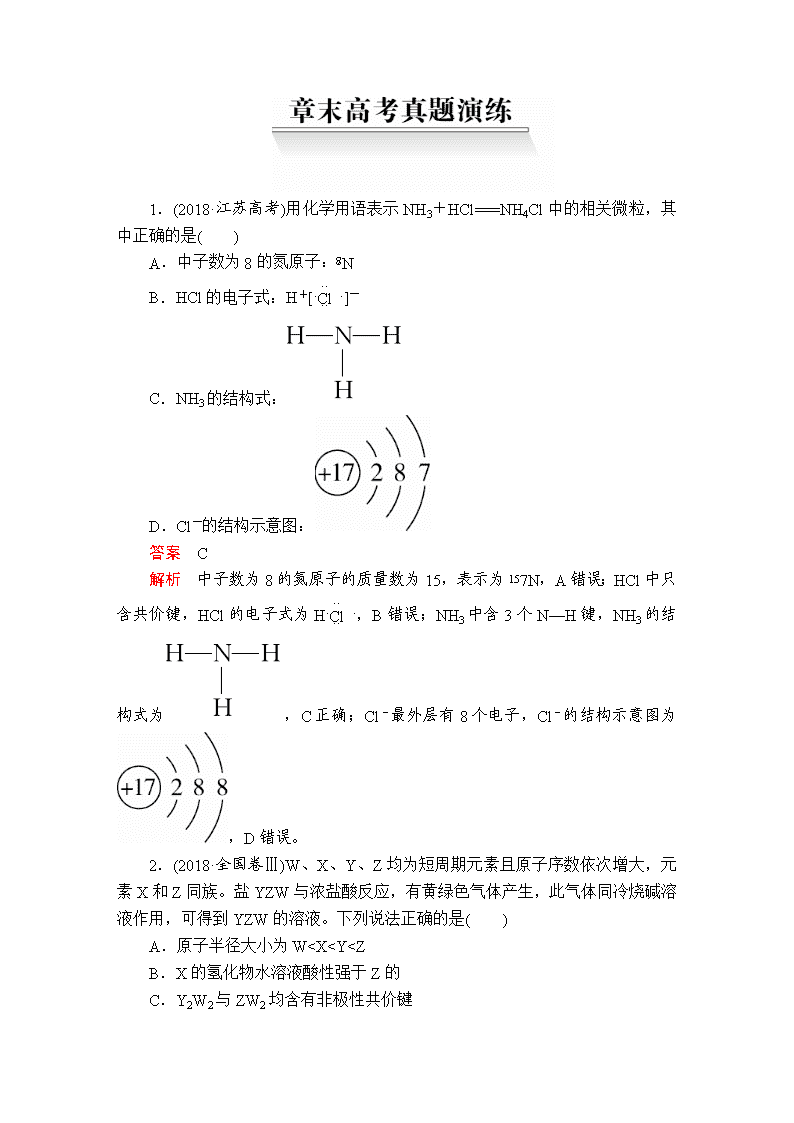
A.中子数为8的氮原子:N
B.HCl的电子式:H+[ ]-
C.NH3的结构式:
D.Cl-的结构示意图:
答案 C
解析 中子数为8的氮原子的质量数为15,表示为7N,A错误;HCl中只含共价键,HCl的电子式为H ,B错误;NH3中含3个N—H键,NH3的结构式为,C正确;Cl-最外层有8个电子,Cl-的结构示意图为,D错误。
2.(2018·全国卷Ⅲ)W、X、Y、Z均为短周期元素且原子序数依次增大,元素X和Z同族。盐YZW与浓盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作用,可得到YZW的溶液。下列说法正确的是( )
A.原子半径大小为W
c>b>a
B.4种元素中b的金属性最强
C.c的氧化物的水化物是强碱
D.d单质的氧化性比a单质的氧化性强
答案 B
解析 a原子核外电子总数与b原子次外层的电子数相同,b原子次外层的电子数为2或8,若b原子次外层的电子数为2,则a为He,不是主族元素,不符合题意;则b原子次外层的电子数为8,则b为第三周期元素,a为O;d与a同族,则d为S;c所在周期数与族数相同,则c为Al,b为Na或Mg。A错:原子半径:aNH3>SiH4
B.氢元素与其他元素可形成共价化合物或离子化合物
C.图中所示实验可证明元素的非金属性:Cl>C>Si
D.用中文“”(ào)命名的第118号元素在周期表中位于第七周期0族
答案 C
解析 A对:元素的非金属性越强,其对应的气态氢化物的稳定性越强。B对:氢元素可与O、S等形成共价化合物,又可与Na、Ca等形成离子化合物。C错:该实验只能证明酸性:HCl>H2CO3>H2SiO3,HCl酸性的强弱与元素非金属性强弱无关。D对:根据元素周期表可知,118号元素位于第七周期0族。
8.(2017·江苏高考)短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强的元素。下列说法正确的是( )
A.原子半径:r(X)X>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
答案 C
解析 根据题意,不难推出n为Cl2,m为H2O,q为HClO,r为HCl,p为烷烃,s为一氯代烷、二氯代烷等的混合物,从而推出W、X、Y、Z四种元素分别为H、C、O、Cl。A项,原子半径大小为HCl>C(即Y>Z>X),错误;C项,Y的氢化物有H2O2、H2O,二者在常温常压下均为液态,正确;D项,X的最高价氧化物的水化物为H2CO3,属于弱酸,错误。
10.(2016·全国卷Ⅱ)a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和c+离子的电子层结构相同,d与b同族。下列叙述错误的是( )
A.a与其他三种元素形成的二元化合物中其化合价均为+1
B.b与其他三种元素均可形成至少两种二元化合物
C.c的原子半径是这些元素中最大的
D.d与a形成的化合物的溶液呈弱酸性
答案 A
解析
由题中信息可知,a、b、c、d分别是H、O、Na、S。H与Na形成的二元化合物NaH中,H元素的化合价为-1,A项错误;O与其他三种元素可分别形成H2O、H2O2,Na2O、Na2O2,SO2、SO3等,B项正确;Na元素位于第三周期ⅠA族,在四种元素中原子半径最大,C项正确;氢硫酸是一种弱酸,D项正确。
11.(2018·天津高考)下图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:
(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H-除外):______,Mg在元素周期表中的位置:____________,Mg(OH)2的电子式:____________。
(2)A2B的化学式为________。反应②的必备条件是____________。上图中可以循环使用的物质有____________。
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料________(写化学式)。
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:_______________。
答案 (1)r(H+)
查看更多