- 2021-08-24 发布 |
- 37.5 KB |
- 21页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018届二轮复习三年全国II卷选择题分析课件(21张)(全国通用)
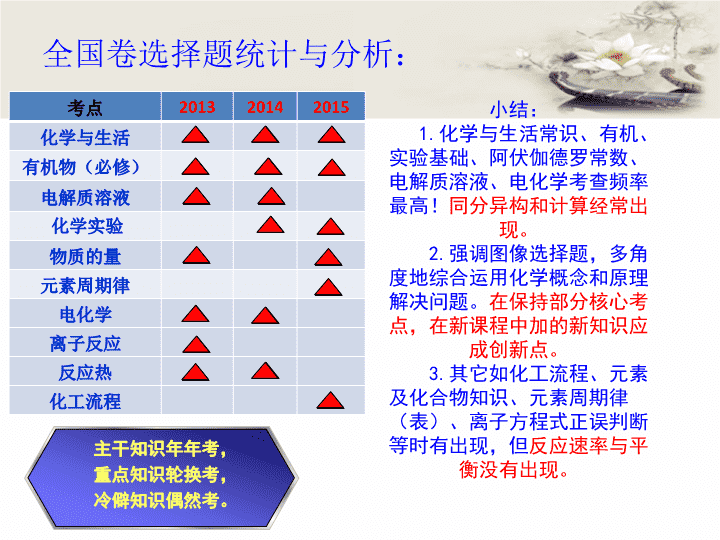
三年全国 II 卷 选择题 分析及复习策略 近三年新课标全国卷 II 选择题研究 2013 年 2014 年 2015 年 7 有机基础知识 (化学与生活) 化学素养 ( 化学与生活 ) 化学与生活 8 有机物基础知识 有机同分异构 有机基础知识 9 N A 元素化合物知识 N A 10 离子方程式 实验操作 元素周期律 11 电化学(原电池) 电解质溶液 有机同分异构 12 反应热 电化学 化学工艺流程 13 电解质溶液 反应热 实验操作 全国卷选择题统计与分析: 考点 2013 2014 2015 化学与生活 有机物(必修) 电解质溶液 化学实验 物质的量 元素周期律 电化学 离子反应 反应热 化工流程 主干知识年年考, 重点知识轮换考, 冷僻知识偶然考。 小结: 1. 化学与生活常识、有机、实验基础、阿伏伽德罗常数、电解质溶液、电化学考查频率最高! 同分异构和计算经常出现。 2. 强调图像选择题,多角度地综合运用化学概念和原理解决问题。 在保持部分核心考点,在新课程中加的新知识应成创新点。 3. 其它如化工流程、元素及化合物知识、元素周期律(表)、离子方程式正误判断等时有出现,但 反应速率与平衡没有出现。 考点 命题特点 高频考点 生活 与 化学 取材极灵活,能反映考生的学科素养,涉及元素化合物知识 化学实验 (无机化工流程) 元素化合物知识 为载体 , 考查 实验原理和操作 元素周期律 基于微粒结构进行推理的能力 ,考查必修二内容 有机化学 考 性质 考 结构 考同分异构体 ,考 查 必修 二内容 电解质溶液 强调离子平衡问题中定性与定量分析相结合 反应热 考查反应中能量转化形式、热化学方程式与盖斯定律相结合 重点 考点 物质的 量 难点常落在混合物的组成或纯净物的结构 电化学 前沿性的电化学应用为情境,但考的是基本概念 元素及化合物 考查化学用语及定量计算能力 非常“ 6+1 ” 6 白马(高频、重点)考点 1 黑马(较冷)考点 形式上强调图表等多种呈现方式,实质上考查多综合 运用化学概念和原理解决问题的能力 , 选题上 不强调覆盖面, 侧重基础与能力并行 ,但在选项设置时却对相关知识点考查较系统 。 近三年新课标全国卷 II 选择题知识点分布 2013 2014 2015 必修 1 6+6 6+6 6+6 必修 2 6 6 选修 4 6+6+6 6+6+6 选修 5 6 6 6+6 化学 实验 6 6+6 近三年选择题考点在各本教材中的分值分配 注:STSE纳入必修1 1. 保持平稳,适度创新。 2. 重视基础、突出主干,但 边缘化 知识点也经常出其意。 3 .部分试题直接取材于课本,充分体现了“源于教材,高于教材,理在书内,题在书外”的高考命题原则。 4. 试题与生产、生活实际密切联系。要求利用化学知识对社会、生活现象进行解释;对于考生正确认识化学学科的价值起到了良好的导向作用。 5 .涉及到计算能力的考查。但纯技巧性的计算几乎没有,主要突出化学计算的实用 价值。 6. 由于 《 选修四 》 为必考,与 《 选修四 》 相关的选择题,难度较大,所占比重也较大。 7. 虽然 《 选修五 》 为选考,但由于有机知识的连贯性,所以在必考部分出现的有机题往往需要涉及 《 选修五 》 知识。 命题思想: “保持平稳,适度创新” 命题观: “重视基础”、 “突出主干”、 “知识为载体” 、“能力为主导” 考查指向 : “联系实际” “探究意识” ( 201 5 -7) 食品干燥剂应无毒、无味、无腐蚀性及环境友好 。下列说法错误的是 A .硅胶可用作食品干燥剂 B . P 2 O 5 不可用作食品干燥剂 C .六水合氯化钙可用作食品干燥剂 D .加工后具有吸水性的植物纤维可用作食品干燥剂 近五年高频考点命题特点 1.STSE: 取材极其灵活,能反应考生的学科素养,常涉及元素化合物知识,还有一些是被“边缘”的概念的和常识。 C (201 4 -7) 下列过程没有发生化学反应的是 A .用活性炭去除冰箱中的异味 B .用热碱水清除炊具上残留的油污 C .用浸泡过高锰酸钾溶液的硅藻土保鲜水果 D .用含硅胶、铁粉的透气小袋与食品一起密封包装 A (201 4 -7) 在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下 : 下列叙述错误的是 A .生物柴油由可由再生资源制得 B . 生物柴油是不同酯组成的混合物 C .动植物油脂是高分子化合物 D . “地沟油”可用于制备生物柴油 C 1.STSE: 取材极其灵活,能反应考生的学科素养,常涉及元素化合物知识,还有一些是被“边缘”的概念的和常识。 (201 5 -1 2 ) 海水开发利用的部分过程如图所示。下列说法错误的是 A .向苦卤中通入 Cl 2 是为了提取溴 B .粗盐可采用除杂和重结晶等过程提纯 C .工业生产中常选用 NaOH 作为沉淀剂 D .富集溴一般先用空气和水蒸气吹出单质溴,再用 SO 2 将其还原吸收 教材 《 必修二 》93 页 4 题、 107 页 9 题均与此题相关。 2.化学实验: ①常与元素化合物等知识结合考察;②要求准确掌握实验原理和基本操作;③关注实验中药品用量问题;④重视对课本实验的考察 C 选项 ① 中 物质 ② 中物质 预测 ② 中的现象 A . 稀盐酸 碳酸钠与氢氧化钠的混合溶液 立即产生气泡 B . 浓硝酸 用砂纸打磨过的铝条 产生红棕色气体 C . 氯化铝溶液 浓氢氧化钠溶液 产生大量白色沉淀 D . 草酸溶液 高锰酸钾酸性溶液 溶液逐渐褪色 ( 2015-13 ) 用右图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是 D 2.化学实验: ①常与元素化合物等知识结合考察;②要求准确掌握实验原理和基本操作;③关注实验中药品用量问题;④重视对课本实验的考察 ( 2014-10 ) 下列图示实验正确的是 [ 来源 D 2.化学实验: ①常与元素化合物等知识结合考察;②要求准确掌握实验原理和基本操作;③关注实验中药品用量问题;④重视对课本实验的考察 ( 2015-11 ) 分子式为 C 5 H 10 O 2 并能与饱和 NaHCO 3 溶液反应放出气体的有机物有 ( 不含立体异构 ) A . 3 种 B . 4 种 C . 5 种 D . 6 种 B 3.有机化学: ①考察思维有序性,重视同分异构体的考察,记忆某些常见化学式的异构体种数利于快速解题; ②结构、性质、反应类型等的考察均有体现;③难度向必修范畴靠拢。 ( 2014-8 ) 四联苯 的一氯代物有 A . 3 种 B . 4 种 C . 5 种 D . 6 种 C ( 201 5 - 8 ) 某羧酸酯的分子式为 C 18 H 26 O 5 , 1mol 该酯完全水解可得到 1mol 羧酸和 2mol 乙醇,该羧酸的分子式为 A . C 14 H 18 O 5 B . C 14 H 16 O 4 C . C 14 H 22 O 5 D . C 14 H 10 O 5 A ( 201 4 - 3 ) 下列叙述中,错误的是 A .苯与浓硝酸、浓硫酸共热并保持 55-60℃ 反应生成硝 基苯 B .苯乙烯在合适条件下催化加氢可生成乙基环己烷 C .乙烯与溴的四氯化碳溶液反应生成 1,2- 二溴乙烷 D .甲苯与氯气在光照下反应主要生成 2,4- 二氯甲苯 D 3.有机化学: ①考察思维有序性,重视同分异构体的考察,记忆某些常见化学式的异构体种数利于快速解题; ②结构、性质、反应类型等的考察均有体现;③难度向必修范畴靠拢。 (2014-11 ) 一定温度下,下列溶液的离子浓度关系式正确的是( ) A . pH=5 的 H 2 S 溶液中, c (H + )= c (HS - )=1×10 —5 mol·L —1 B . pH= a 的氨水溶液,稀释 10 倍后,其 pH= b ,则 a = b +1 C . pH=2 的 H 2 C 2 O 4 溶液与 pH=12 的 NaOH 溶液任意比例混合: c (Na + )+ c (H + )= c (OH - )+ c ( HC 2 O 4 - ) D . pH 相同的① CH 3 COONa ② NaHCO 3 ③ NaClO 三种溶液的 c (Na + ) :①>②>③ 4. 电解质: ①定性与定量结合;②图像图表结合;③要求原理清楚、思维严密、计算准确。 D (2013-13 ) 室温时, M(OH) 2 (S) M 2+ (aq)+2OH - (aq) Ksp=a , c(M 2+ )=b mol·L -1 时,溶液的 pH 等于 4. 电解质: ①定性与定量结合;②图像图表结合;③要求原理清楚、思维严密、计算准确。 C (2014-13 ) 室温下,将 1mol 的 CuSO 4 ·5H 2 O(s) 溶于水会使溶液温度降低,热效应为△ H 1 ,将 1mol 的 CuSO 4 (s) 溶于水会使溶液温度升高,热效应为△ H 2 ; CuSO 4 ·5H 2 O 受热分解的化学方程式为: CuSO 4 ·5H 2 O(s)====CuSO 4 (s)+5H 2 O(l) , 热效应为△ H 3 。则下列判断正确的是 A .△ H 2 >△ H 3 B .△ H 1 <△ H 3 C .△ H 1 + △ H 3 = △ H 2 D .△ H 1 + △ H 2 >△ H 3 6. 反应热: ① 综合运用所学化学知识解决相关 化学问题的能力 ;②图像图表结合;③ 灵活运用盖斯定律 。 B (2013-12 ) 在 1200℃ 时,天然气脱硫工艺中会发生下列反应 ①H 2 S(g)+ 3/2 O 2 (g)=SO 2 (g)+H 2 O(g) △H 1 ②2H 2 S(g)+SO 2 (g)= 3/2 S 2 (g)+2H 2 O(g) △H 2 ③H 2 S(g)+ 1 /2O 2 (g)=S(g)+H 2 O(g) △H 3 ④2S(g) =S 2 (g) △H 4 则 △H 4 的正确表达式为( ) A . △H 4 =2/ 3 ( △H 1 +△H 2 -3△H 3 ) B . △H 4 =2/3 ( 3△H 3 -△H 1 -△H 2 ) C . △H 4 =3/2 ( △H 1 +△H 2 -3△H 3 ) D . △H 4 =3/2 ( △H 1 -△H 2 -3△H 3 ) 6. 反应热: ① 综合运用所学化学知识解决相关 化学问题的能力 ;②图像图表结合;③ 灵活运用盖斯定律 。 B (201 5 - 9 ) N A 代表阿伏加德罗常数的值。下列叙述正确的是 A . 60g 丙醇中存在的共价键总数为 10 N A B . 1L 0.1mol·L - 1 的 NaHCO 3 溶液中 HCO 3 - 和 CO 3 2 - 离子数之和 为 0.1 N A C .钠在空气中燃烧可生成多种氧化物。 23g 钠充分燃烧时转移 电子数为 1 N A D . 235g 核互 U 发生裂变反应: U+ n S r+ U+10 n ,净产生的中子 ( n) 数为 10 N A C 7N A : ①考察学生 物质的量在物质及其所含构成微粒关系式计算中的应用 ;②体现化学学科 从定性到定量、从宏观到微观的特点 ;③ 能反应考生的 知识是否全面 。 (201 3 - 9 ) N A 为阿伏伽德罗常数的值,下列叙述正确的是 A . 1.0L1.0mo1·L -1 的 NaAlO 2 水溶液中含有的氧原子数为 2N A B . 12g 石墨烯 ( 单层石墨 ) 中含有六元环的个数为 0.5N A C . 25℃ 时 pH =13 的 NaOH 溶液中含有 OH - 的数目为 0.1 N A D . 1 mol 的羟基与 1 moL 的氢氧根离子所含电子数均为 9 N A B 7N A : ①考察学生 物质的量在物质及其所含构成微粒关系式计算中的应用 ;②体现化学学科 从定性到定量、从宏观到微观的特点 ;③ 能反应考生的 知识是否全面 。 (201 5 - 10 ) 原子序数依次增大的元素 a 、 b 、 c 、 d ,它们的最外层电子数分别 为 1 、 6 、 7 、 1 。 a - 的电子层结构与氦相同, b 和 c 的次外层有 8 个电子, c - 和 d + 的电子层结构相同。下列叙述错误的是 A .元素的非金属性次序为 c > b > a B . a 和其他 3 种元素均能形成共价化合物 C . d 和其他 3 种元素均能形成离子化合物 D .元素 a 、 b 、 c 各自最高和最低化合价的代数和分别为 0 、 4 、 6 B 8. 元素周期律和周期表: ①考察 短周期 元素原子结构、元素性质及其递变规律;②可能需要 较“边缘”的知识辅助 推断,能反应考生的 知识是否全面 。 选择题复习策略 1. 安排时间让学生将几本化学教材通读,尤其是平时容易忽视的一些地方更应着重理解。 2. 加强元素化合物、有机化学方程式及其实验相关知识的反复记忆,以便高考时能快速、准确的提取基础知识进行应用。 3. 重视图像、图表类选择题的训练。 4. 复习完元素化合物后,可增加选择题的定时训练、提 高做选择题的速度、技巧、增强应考自信心。查看更多