卓越联盟2021届高三化学9月联考试题(Word版带答案)
绝密★启用前
卓越联盟新高考省份高三年级9月份检测试题
化 学 试 卷
(本试卷满分100分,考试时间:90分钟)
注意事项:
1.答卷前:先将自己的姓名、准考证号填写在试卷和答题卡上,并将准考证条码粘贴在答题卡上指定位置。
2.选择题,每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
3.非选择题,用0.5mm黑色签字笔写在答题卡上对应的答题区域,写在非答题区域无效。
相对原子质量:O-16 Cl-35.5 Cu-64 P-31 Sn-119
一、选择题:本题共10小题,每小题2分,共20分.每小题只有一个选项符合题目要求.
1.从石油原料到口罩的生产过程中涉及的下列变化不属于化学变化的是
A
B
C
D
石油催化裂解得到丙烯
丙烯催化聚合生成聚丙烯
聚丙烯熔融后喷丝压成熔喷布
利用环氧乙烷与微生物蛋白质发生烷基化反应消毒
2.化学与生产和生活密切相关,下列说法错误的是
A.高纯硅可用于制作光感电池
B.活性炭具有除异味和杀菌作用
C.氢氧化铝、碳酸氢钠都是常见的胃酸中和剂
D.碘酒可用于皮肤外用消毒
3.下列反应的离子方程式正确的是
A.用醋酸除去水垢:CaCO3 +2H+ = Ca2+ + CO2↑+ H2O
B.向AlCl3溶液中加入过量的浓氨水:Al3++4NH3∙H2O=AlO2−+4NH4++2H2O
C.向苯酚钠溶液中通入少量CO2:2+CO2+H2O→2+CO32−
D.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2++2OH−+NH4++HCO3−=BaCO3↓+NH3∙H2O+H2O
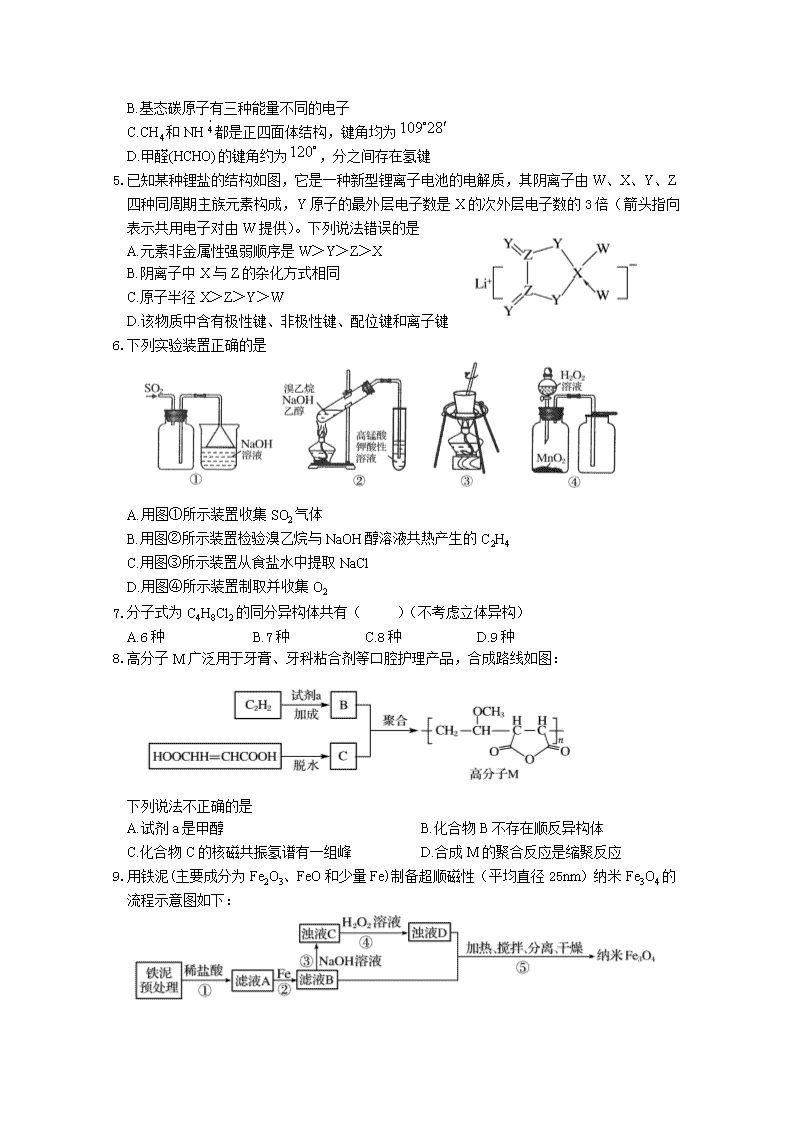
4.下列关于物质结构的说法错误的是
A.晶格能:NaF>NaCl>NaBr
B.基态碳原子有三种能量不同的电子
C.CH4和NH都是正四面体结构,键角均为
D.甲醛(HCHO)的键角约为,分之间存在氢键
5.已知某种锂盐的结构如图,它是一种新型锂离子电池的电解质,其阴离子由W、X、Y、Z四种同周期主族元素构成,Y原子的最外层电子数是X的次外层电子数的3倍(箭头指向表示共用电子对由W提供)。下列说法错误的是
A.元素非金属性强弱顺序是W>Y>Z>X
B.阴离子中X与Z的杂化方式相同
C.原子半径X>Z>Y>W
D.该物质中含有极性键、非极性键、配位键和离子键
6.下列实验装置正确的是
A.用图①所示装置收集SO2气体
B.用图②所示装置检验溴乙烷与NaOH醇溶液共热产生的C2H4
C.用图③所示装置从食盐水中提取NaCl
D.用图④所示装置制取并收集O2
7.分子式为C4H8Cl2的同分异构体共有( )(不考虑立体异构)
A.6种 B.7种 C.8种 D.9种
8.高分子M广泛用于牙膏、牙科粘合剂等口腔护理产品,合成路线如图:
下列说法不正确的是
A.试剂a是甲醇 B.化合物B不存在顺反异构体
C.化合物C的核磁共振氢谱有一组峰 D.合成M的聚合反应是缩聚反应
9.用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备超顺磁性(平均直径25nm)纳米Fe3O4的流程示意图如下:
下列叙述不正确的是
A.常用热的Na2CO3溶液除去钢铁表面的油污
B.步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+
C.步骤④中,反应完成后剩余的H2O2无需除去
D.步骤⑤中,为了验证得到的固体是超顺磁性的Fe3O4粒子,可将其均匀分散在水中,做丁达尔效应实验
10.2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。磷酸铁锂锂离子电池充电时阳极反应式为,,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内。放电工作示意图如图。下列叙述不正确的是
A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,
C、Fe、P元素化合价均不发生变化
二、选择题:本题共5小题,每小题4分,共20分.每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错得0分.
11.下列实验操作、现象与结论对应关系正确的是
选项
实验操作
实验现象
结论
A
向盛有2mL0.l mol/L的AgNO3溶液中加入10滴0.1mol/L的NaCl溶液,振荡,再加入10滴0.1 mol/L的NaI溶液,再振荡
先生成白色沉淀,后产生黄色沉淀
Ksp(AgI)
”, “<”, “=”)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因 。
④c点时该反应的平衡常数K= 。
(3)中国科学家首次用CO2高效合成乙酸,其反应路径如图所示:
①原料中的CH3OH可通过电解法由CO2制取,用稀硫酸作电解质溶液,写出生成CH3OH的电极反应式 。
②根据图示,写出总反应的化学方程式: 。
19.(12分)丁苯酞(J)是治疗轻、中度急性脑缺血的药物,合成J的一种路线如下:
已知:
(1)G中官能团的名称为_________、_________。
(2)D的系统命名是_______,化合物J的结构简式为 。
(3)C与银氨溶液反应的化学方程式为______________________________________。
(4)根据 ,X的分子式为__________。X有多种同分异构体,其中满足下列条件的同分异构体共有_______种(已知:碳碳三键或碳碳双键不能与羟基直接相连)。
①除苯环外无其他环,且无—O—O—键
②能与FeCl3溶液发生显色反应
③苯环上的一氯代物只有两种
(5)参照题中信息写出以甲烷和甲苯为原料,合成的 路线流程图(其他试剂自选)。
20.(11分)2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效灭活新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(C1O2)就是其中一种高效消毒灭菌剂。氯酸钠还原法是目前使用较为广泛的ClO2制备方法,其中一种是用NaClO3与CH3OH在催化剂、60℃时,发生反应得到ClO2,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
已知:
①ClO2的浓度较大时易分解爆炸,一般用CO2或空气稀释到10%以下;
实验室也常用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I−+8H+2Cl−+5I2+4H2O。
③
请回答:
(1)仪器b在装置中的作用是 ;比较仪器c和d,实验中c的优点是 。
(2)根据反应条件判断制备装置甲中需改进的一项措施是 。
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式: ;该制备法可选用不同的还原性物质作为还原剂,例如草酸(草酸的氧化产物为CO2),相比甲醇法,草酸法的优点是 。
(4)下列有关说法正确的是________。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置e主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5ClO2−=Cl−+4ClO2↑+2H2O
D.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,Cl2的氧化能力是ClO2的2.5倍
(5)自来水厂用碘量法检测水中ClO2的浓度,其实验操作如下:取100.0 mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用0.1000 mol·L−1 Na2S2O3标准溶液滴定碘单质(I2+2S2O32−=2I−+S4O62−),达到滴定终点时用去15.00 mL Na2S2O3标准溶液,测得该水样中ClO2的含量为________mg·L−1。
新高考省份高三年级9月份检测试题
化学试卷答案
第Ⅰ卷(共40分)
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1-5 CBDDB 6-10 DDDCD
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错得0分。
11.C 12.BD 13.AB 14.BD 15.C
第Ⅱ卷(共60分)
16.(11分)
Ⅰ.(1) ZnO(s) + C(s) = Zn(g) + CO(g)(2分)
Ⅱ.(2) ZnS+2Fe3+ = Zn2++2Fe2++S(2分)
取a中红色溶液,向其中加入ZnS,振荡,红色褪去(2分)
(3)通入空气将二价铁氧化,加入的ZnO可控制溶液pH(2分)
(4)Mn2+ - 2e-+2H2O = MnO2+4H+(2分))
(5)硫酸(1分)
17.(11分)
(1)不稳定(1分)
Cu+的价电子排布为3d10,全满,比Cu2+的价电子排布为3d9稳定(1分)
(2)sp3(1分) 1(1分) F>N>O>C>B(1分)
(3)Cu2+诱导胺的氧化脱氢反应形成的Cu+配合物后,体系的共轭程度增大,荧光信发生改变,从而对Cu2+进行检测。(2分)
(4)SnCu3P(1分) (1分) (2分)
△
18.(15分)
(1)Ea-1366.8 (2分) CH3CH2Cl+OH−C2H5OH +Cl− (2分)
v=kc(CH3CH2Cl) (1分)
(2)①反应 I (1分) ② > (1分)
③该反应为放热反应,温度升高,平衡逆向移动(2分) ④ (2分)
(3)CO2+6e- +6H+ = CH3OH+H2O (2分)
CH3OH+ CO2+H2 CH3COOH+H2O (2分)
19.(12分)
(1)羟基(1分) 溴原子(或碳溴键)(1分)
(2)2-甲基-1-丙烯(或2-甲基丙烯)(1分) (2分)
(3)(2分)
(4)C8H6O3 (1分) 9(2分)
(5)
(2分)
20.(11分)
(1)冷凝回流甲醇兼导气(1分) 有利于液体顺利流下,防止甲醇挥发 (1分)
(2)水浴加热(1分)
(3)4NaClO3+CH3OH+2H2SO42Na2SO4+4ClO2↑+HCOOH+3H2O
或4NaClO3+CH3OH+4H2SO44ClO2↑+HCOOH+4NaHSO4+3H2O(2分)
产生的CO2可稀释ClO2,防止ClO2浓度较大时分解 (2分)
(4)AC (2分)
(5)202.5(2分)