- 2021-08-24 发布 |
- 37.5 KB |
- 9页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
【化学】安徽省定远县育才学校2020-2021学年高二上学期开学考试
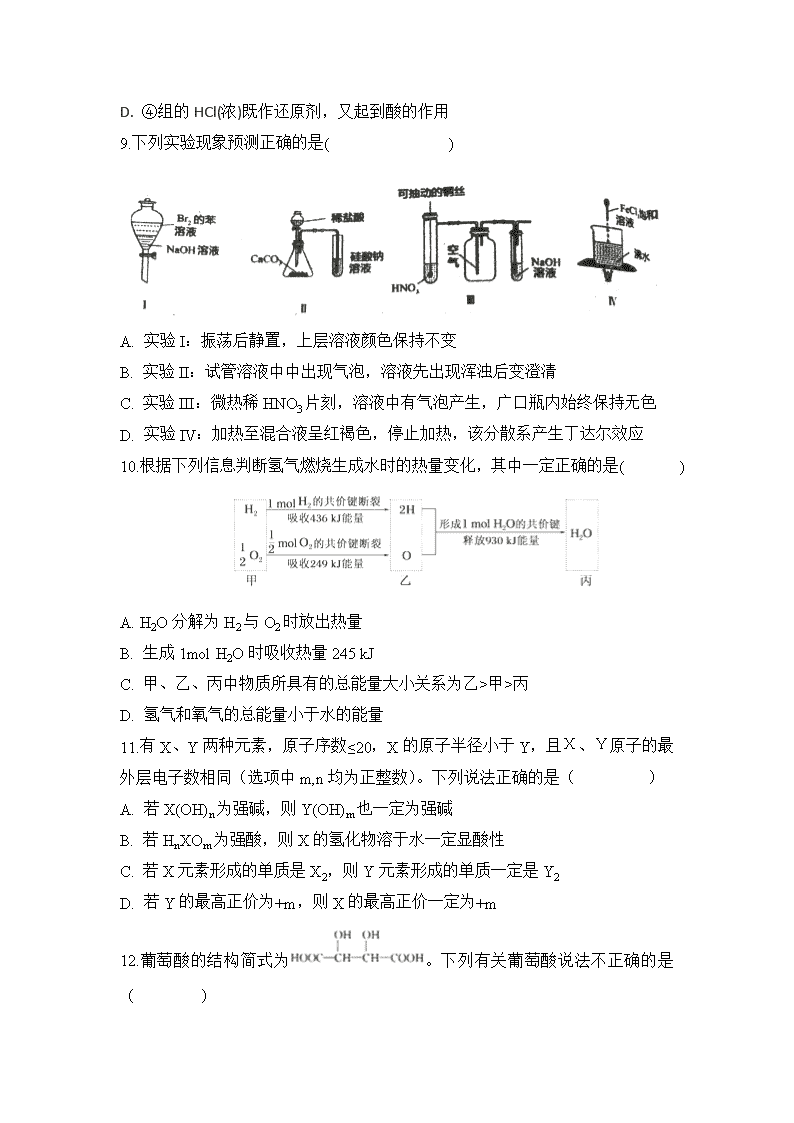
安徽省定远县育才学校 2020-2021 学年高二上学期开学考试 一、选择题(每小题 3 分,18 小题,共 54 分。) 1.胶体区别于其它分散系的本质是( ) A. 胶体粒子不能穿过半透膜,能通过滤纸空隙 B. 胶体粒子带电荷并且在一定条件下能稳定存在 C. 胶体的分散质粒子直径在 1 nm~100nm 之间 D. 胶体粒子能够发生布朗运动而且能产生丁达尔现象 2.在 2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O 反应中( ) A. 氧化剂与还原剂的物质的量之比为 1∶8 B. 氧化剂与还原剂的物质的量之比为 5∶1 C. 氧化产物与还原产物的物质的量之比为 5∶2 D. 氧化产物与还原产物的物质的量之比为 2∶5 3.草酸(分子式为 H2C2O4,沸点:150℃)是生物体的一种代谢产物,广泛分布 于植物、动物和真菌体中.下列有关判断不正确的是( ) A. 45g 草酸中含有 1.204×1024 个氧原子 B. 1mol 草酸中含有 6.02×1023 个分子 C. 草酸的摩尔质量是 90g/mol D. 1mol 草酸在标准状况下的体积约为 22.4L 4.常温下,发生下列几种反应: ①16H++10Z-+2XO4-===2X2++5Z2+8H2O ②2A2++B2===2A3++2B- ③2B-+Z2===B2+2Z- 根据上述反应,判断下列结论错误的是( ) A. 溶液中可发生:Z2+2A2+===2A3++2Z- B. 氧化性强弱的顺序为 XO4->Z2>B2>A3+ C. Z2 在①③反应中为氧化剂 D. 反应③中 B2 是 2B-的氧化产物 5.在 K2SO4 和 Al2(SO4)3 的混合溶液中,测得 Al3+浓度为 0.2mol/L,加入等体 积 0.6mol/L 的 BaCl2 溶液恰好使 SO42﹣完全沉淀,则混合溶液中 K+的浓度为 ( ) A. 0.3 mol/L B. 0.45 mol/L C. 0.6 mol/L D. 0.15 mol/L 6.下列化学用语的书写,正确的是( ) A. 氯原子的结构示意图: B. 6 个质子 8 个中子的碳元素的核素符号:12C C. 氯化镁的电子式:[ ]-Mg2+[ ]- D. 用电子式表示氯化氢的形成过程:H·+· ―→H +[ ]- 7.X、Y、Z、W 是原子序数依次增大的四种短周期元素,X 的最高价氧化物对应 的水化物的化学式为 H2XO3,Y 的最外层电子数是电子层数的 3 倍,Z 是地壳中 含量最高的金属元素,W 的一种核素的质量数为 28,中子数为 14。下列说法正 确的是( ) A. 原子半径由大到小的顺序是 Z>W>Y>X B. 元素的非金属性 W>Y>X C. Z2Y3、WX 分别是离子化合物、共价化合物 D. X、Z、W 的最高价氧化物都是酸性氧化物 8.下列叙述中正确的是( ) 序号 氧化剂 还原剂 其他 反应物 氧化 产物 还原产物 ① Cl2 FeCl2 FeCl3 ② KMnO4 H2O2 H2SO4 O2 MnSO4 ③ KClO3 HCl(浓) Cl2 Cl2 ④ KMnO4 HCl(浓) Cl2 MnCl2 A. 表中第①组反应 FeCl3 只作为还原产物 B. 氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+ C. 还原性比较:H2O2>Mn2+>Cl- D. ④组的 HCl(浓)既作还原剂,又起到酸的作用 9.下列实验现象预测正确的是( ) A. 实验 I:振荡后静置,上层溶液颜色保持不变 B. 实验 II:试管溶液中中出现气泡,溶液先出现浑浊后变澄清 C. 实验 III:微热稀 HNO3 片刻,溶液中有气泡产生,广口瓶内始终保持无色 D. 实验 IV:加热至混合液呈红褐色,停止加热,该分散系产生丁达尔效应 10.根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( ) A. H2O 分解为 H2 与 O2 时放出热量 B. 生成 1mol H2O 时吸收热量 245 kJ C. 甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙 D. 氢气和氧气的总能量小于水的能量 11.有 X、Y 两种元素,原子序数≤20,X 的原子半径小于 Y,且X、Y原子的最 外层电子数相同(选项中 m,n 均为正整数)。下列说法正确的是( ) A. 若 X(OH)n 为强碱,则 Y(OH)m 也一定为强碱 B. 若 HnXOm 为强酸,则 X 的氢化物溶于水一定显酸性 C. 若 X 元素形成的单质是 X2,则 Y 元素形成的单质一定是 Y2 D. 若 Y 的最高正价为+m,则 X 的最高正价一定为+m 12.葡萄酸的结构简式为 。下列有关葡萄酸说法不正确的是 ( ) A. 葡萄酸能发生取代反应 B. 葡萄酸既能与乙醇发生酯化反应,也能与乙酸发生酯化反应 C. 葡萄酸能与 Na 和 NaOH 反应 D. 葡萄酸能使溴的四氯化碳溶液褪色 13.下列相关实验设计不能达到预期目的的是( ) 选 项 实验设计 预期目的 A 相同温度下,等质量的大理石块、大 理石粉分别与等体积、等浓度的盐酸反 应 探究接触面积对化学反应速率 的影响 B 把装有颜色相同的 NO2 和 N2O4 混合 气体的两支试管(密封)分别浸入冷水 和热水中 探究温度对化学平衡的影响 C 用 MgCl2 和 AlCl3 分别与过量氨水反 应 探究 Mg、Al 的金属性强弱 D 往盛有葡萄糖溶液的试管中滴入新制 氢氧化铜悬浊液,加热 探究葡萄糖的化学性质 14.有关电化学知识的描述正确的是 A. CaO+H2O=Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中 的化学能转化为电能 B. 原电池的两极一定是由活动性不同的两种金属组成 C. 从理论上讲,任何能自发进行的氧化还原反应都可设计成原电池 D. 原电池工作时,正极表面一定有气泡产生 15.已知某化学反应 A2(g)+2B2(g)=2AB2(g) (A2、B2、AB2 的结构式分别为 A=A、 B-B、B-A-B),能量变化如图所示,下列有关叙述中正确的是( ) A. 该反应若生成 2molAB2(g)则吸收的热量为(El-E2)kJ B. 该反应的进行一定需要加热或点燃条件 C. 该反应断开化学键消耗的总能量小于形成化学键释放的总能量 D. 生成 2molB-B 键放出 E2kJ 能量 16.化学与生活密切相关,下列说法错误的是( ) A. 含有重金属的电器废品不能随意丢弃,要分类回收并利用 B. 食品中都必须添加大量的化学防腐剂,使食品保质期更长久 C. 采用加热消毒的目的是使蛋白质变性而杀灭细菌消毒 D. 使用乙醇作为汽油的代用品,可以减少汽车尾气中有害气体排放 17.为比较 Fe3+和 Cu2+对 H2O2 分解反应的催化效果,甲、乙两位同学分别设计 了如图甲、乙所示的实验。下列叙述中不正确的是( ) A. 图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 B. 若图甲所示实验中反应速率为①>②,则一定说明 Fe3+比 Cu2+对 H2O2 分解 催化效果好 C. 用图乙所示装置测定反应速率,可测定反应产生的气体体积及反应时间 D. 为检查图乙所示装置的气密性,可关闭 A 处活塞,将注射器活塞拉出一定距 离,一段时间后松开活塞,观察活塞是否回到原位 18.如图为实验室制取少量乙酸乙酯的装置图,下列关于该实验的叙述中,不正 确的是( ) A. 向 a 试管中先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸 B. 可将饱和碳酸钠溶液换成氢氧化钠溶液 C. 试管 b 中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现 象 D. 实验时加热试管 a 的目的是及时将乙酸乙酯蒸出并加快反应速率 二、非选择题(共 3 小题 ,共 46 分) 19.在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又 可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性, 在空气中受撞击或受热时会燃烧,所以俗称"引火铁"。请分别用下图中示意的两 套仪器装置,制取上述铁的氧化物和"引火铁",实验中必须使用普通铁粉和 6 摩 /升盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设 备等在图中均已略去)。 按要求填写下列空白: (1)实验进行时试管 A 中应加入的试剂是__________;烧瓶 B 的作用是___ ; 烧 瓶 C 的 作 用 是 ___________________ ; 在 试 管 D 中 收 集 得 到 的 是 ____________。 (2)实验时,U 型管 G 中应加入的试剂是____________;长颈漏斗 H 中应加入 ____。 (3)两套装置中,在实验时需要加热的仪器是(填该仪器对应的字母) ____________。 (4)试管 E 中发生反应的化学方程式是______________________________。 (5)为了安全,在 E 管中的反应发生前,在 F 出口处必须_____;E 管中的反应开 始后,在 F 出口处应____________。 20.X、Y、Z 三种短周期元素,它们的原子序数之和为 16。X、Y、Z 三种元素 常见单质在常温下都是无色气体,在适当条件下可发生如下图所示变化: 已知一个 B 分子中含有的 Z 元素的原子个数比 C 分子中的少一个。 请回答下列问题: (1)Y 元素在周期表中的位置是______;X、Y 原子半径的大小:X______Y(填 “>”、“<”或“=”) (2)X 的单质与 Z 的单质可制成新型的化学电源(KOH 溶液作电解质溶液),两 个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正 极通入______(填物质名称);负极电极反应式为______。 (3)C 在一定条件下反应生成 A 的化学方程式是___________________。 (4)已知 Y 的单质与 Z 的单质生成 C 的反应是可逆反应,△H<0.将等物质的量 的 Y、Z 的单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下 列说法中,正确的是______(填写下列各项的序号)。 a.达到化学平衡的过程中,混合气体平均相对分子质量减小 b.反应过程中,Y 的单质的体积分数始终为 50% c.达到化学平衡时,Y、Z 的两种单质在混合气体中的物质的量之比为 1:1 d. 达到化学平衡时,正反应速率与逆反应速率相等 21.已知铝土矿的主要成分是 Al2O3,含有杂质 SiO2(不溶于盐酸和水)、Fe2O3、 MgO。工业上从铝土矿中提取铝可采用如下工艺流程: 请回答下列问题: (1)溶液 A 转化为溶液 D 发生的离子方程式为____________________; (2)由物质 M 制取铝的化学方程式为____________________; ( 3 ) 溶 液 D 中 通 入 过 量 CO2 生 成 沉 淀 F 的 离 子 方 程 式 为 ____________________; (4)沉淀 C 的成份是________________ ,逐滴向少量沉淀 C 中加入过量 HI 至 沉淀全部溶解,所得溶液的颜色为______________。 参考答案 1.C 2.C 3.D 4.C 5.C 6.C 7.C 8.D 9.D 10.C 11.A 12.D 13.C 14.C 15.A 16.B 17.B 18.B 19. (1)普通铁粉(或铁粉) 作为水蒸气发生器(或用来产生水蒸气) 防止水倒吸 (或用作安全瓶) 氢气 (2)固体 NaOH(或碱石灰、CaO 等碱性固体干燥剂) 6 摩/升 HCl (3)A、B、E (4)Fe3O4+4H2 3Fe+4H2O; (5)检验氢气的纯度;点燃氢气。 20. (1)第 2 周期,VA 族 < (2)氧气 H2+2OH-=2H2O+2e- (3)4NH3+5O2= 4NO+6H2O (4) b d 21. (1) Al3++4OH-=AlO2-+2H2O (2) 2Al2O3 4Al + 3O2↑ (3) AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- (4)Fe(OH)3 Mg(OH)2 浅绿色查看更多