- 2021-08-24 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019-2020学年江苏省扬州中学高二上学期10月月考试题 化学 word版
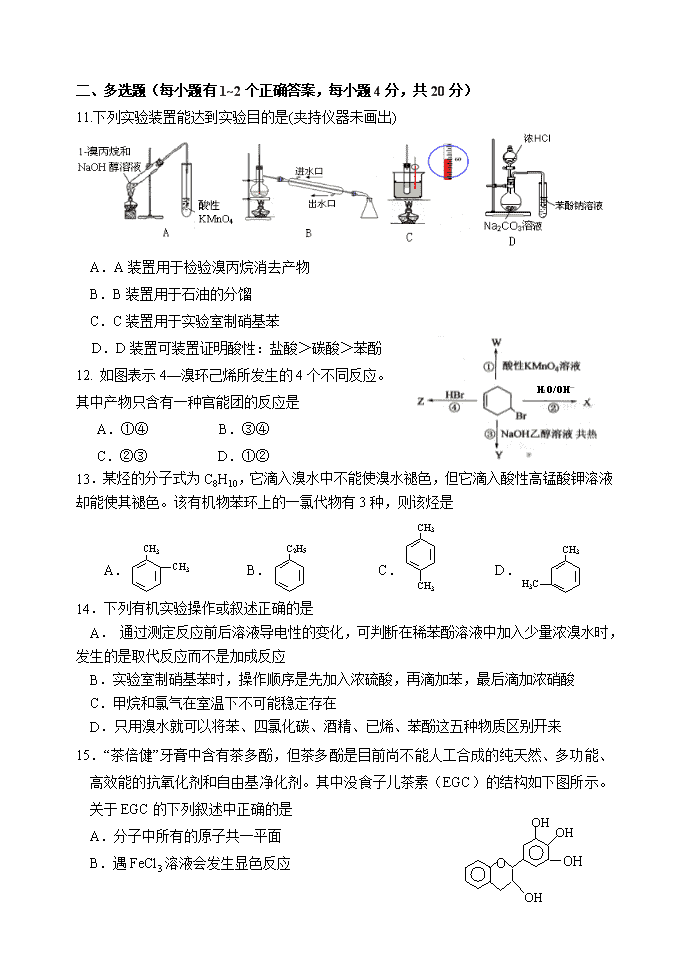
扬州中学2019-2020年度上学期高二年级阶段测试 选 修 化 学 2019-10 (可能用到的相对原子质量:C-12 H-1 O-16) Ⅰ卷 共40分 一、选择题(每小题只有一个正确答案,每小题2分,共20分) 1.下列说法中不正确的是 A.1828年,德国化学家维勒在实验室制得了尿素,突破了无机物与有机物的界限 B.开发核能、太阳能等新能源,推广基础甲醇汽油,使用无磷洗涤剂都可直接降低碳排放 C.在有机化学发展的进程中,德国化学家李比希的“基团理论”对有机化学的发展起到了巨大的推动作用 D.红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 2.下列表述或说法正确的是 A.乙烯分子球棍模型: B.乙醚的结构式: C.-OH与都表示羟基 D.乙烯的结构简式:CH2CH2 3.下列有机化合物中,其核磁共振氢谱图中不可能只出现一个峰的是 A.C2H6 B.C2H6O C.C4H8 D.C6H12 4.下列说法中正确的是 A.煤油可由石油分馏获得,可用作燃料和保存少量金属钠 B.煤经加工所得的产物中存在大量的多环芳烃和稠环芳烃,如二甲联苯()、萘()、蒽()等,这些芳烃均属于苯的同系物 C.两种化合物组成元素相同,各元素质量分数也相同,则二者互为同分异构体 D.石油经过分馏、裂化工序后得到大量乙烯、苯等不饱和烃 5.用NA表示阿伏加德罗常数的值。下列叙述正确的是 A.1 mol的碳烯(︰CH2)含电子数为6 NA B.标准状况下,2.24 L CHCl3的原子总数为0.1 NA C.4.2 g C3H6中含有的碳碳双键数一定为0.1 NA D.常温常压下,28 g丙烯和丁烯的混合气体中含有的碳原子数为2 NA 6. 下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是 A.异戊二烯( )与等物质的量的Br2发生加成反应 B.甲苯在一定条件下发生硝化生成一硝基甲苯的反应 C.1丁烯(CH3CH2CH===CH2)与HCl分子发生的加成反应 D.苯甲酸()与NaHCO3溶液反应 7.某有机物的结构简式为。下列关于该物质的说法中正确的是 A.该物质分子中至多有4个碳原子共面 B.该物质能和AgNO3溶液反应产生AgBr沉淀 C.该物质可以发生消去反应 D.该物质可以发生水解反应 8.有机物A的键线式结构为 ,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是 A.有机物A的一氯取代物只有4种 B.用系统命名法命名有机物A,名称为2,2,3﹣三甲基戊烷 C.有机物A的分子式为C8H18 D.B的结构可能有3种,其中一种名称为3,4,4﹣三甲基﹣2﹣戊烯 9.现有相同碳原子数的烷烃、烯烃、炔烃,分别取等质量的三种烃在空气中完全燃烧生成二氧化碳和水,需要空气量的比较中正确是 A.烷烃最多 B.烯烃最多 C.炔烃最多 D.三者一样多 10.下列事实不能说明有机物分子中原子或原子团直接相连时而产生相互影响的是 A.苯酚能与NaOH溶液反应而乙醇不能 B.等物质的量的乙醇和甘油与足量的金属钠反应,后者产生的氢气比前者多 C.苯与液溴在铁作催化剂下发生反应,而苯酚与浓溴水混合就能发生反应 D.甲苯能使酸性高锰酸钾溶液褪色而甲烷不能 二、多选题(每小题有1~2个正确答案,每小题4分,共20分) 11.下列实验装置能达到实验目的是(夹持仪器未画出) A.A装置用于检验溴丙烷消去产物 B.B装置用于石油的分馏 C.C装置用于实验室制硝基苯 H2O/OH— D.D装置可装置证明酸性:盐酸>碳酸>苯酚 12. 如图表示4—溴环己烯所发生的4个不同反应。 其中产物只含有一种官能团的反应是 A.①④ B.③④ C.②③ D.①② 13.某烃的分子式为C8H10,它滴入溴水中不能使溴水褪色,但它滴入酸性高锰酸钾溶液却能使其褪色。该有机物苯环上的一氯代物有3种,则该烃是 A. B. C. D. 14.下列有机实验操作或叙述正确的是 A. 通过测定反应前后溶液导电性的变化,可判断在稀苯酚溶液中加入少量浓溴水时,发生的是取代反应而不是加成反应 B.实验室制硝基苯时,操作顺序是先加入浓硫酸,再滴加苯,最后滴加浓硝酸 C.甲烷和氯气在室温下不可能稳定存在 D.只用溴水就可以将苯、四氯化碳、酒精、已烯、苯酚这五种物质区别开来 O —OH OH OH OH 15.“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中正确的是 A.分子中所有的原子共一平面 B.遇FeCl3溶液会发生显色反应 C.可发生氧化反应、取代反应、消去反应、加成反应 D.1molEGC与4molNaOH恰好完全反应 Ⅱ卷 共60分 16.(14分)按要求回答问题: (1)乙炔的电子式 ; (2)的分子式 (3)CH3CH2CH2CH2Cl的键线式 (4)CH3CH(C2H5)CH(CH3)2的系统命名为 ; (5)遇FeCl3溶液显紫色且苯环上有两个取代基的的同分异构体有________种。 (6)C4H10O的同分异构体中,属于醇类且含有“手性碳原子”的结构简式为 ; (7)CH2=CH-CH3加聚反应的方程式 17.(13分)下图为苯和溴取代反应的改进实验装置。其中A为带支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑。 填写下列空白: (1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式): _____________________该反应的类型为_______________反应。 (2)试管C中苯的作用是 ;反应开始后,观察D试管,看到的现象为 ;能说明苯与溴发生的是取代反应而不是加成反应的现象为_________________________。 (3)在上述整套装置中,具有防倒吸作用的仪器有 (填字母)。 (4)相对于原装置(右图)改进后的实验除①步骤简单,操作方便,成功率高;② 各步现象明显;③对产品便于观察这三个优点外,还有一个优点是 。 18.(12分)咖啡酸具有止血、镇咳、祛痰等疗效,其结构为 (1)咖啡酸分子中的含氧官能团的名称为 、 ; (2)已知咖啡酸能与碳酸氢钠溶液发生反应,请写出此反应的化学方程式: (3)1mol 咖啡酸在一定条件下,最多消耗 mol溴水中的Br2。 (4)有机物A(分子式为C11H12O4)在一定条件下能发生如下转化: ①D、E的结构简式分别为 、 ; ②B→C反应的化学方程式为 ; 19.(9分)有机物A只含有C、H、O三种元素,常用作有机合成的中间体。16.8 g该有机物经燃烧生成44.0 g CO2和14.4 g H2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的—C≡C—键,核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1。 (1) 16.8gA中C、H、O物质的量分别为:C_______mol,H________mol,O________mol, (2) A的结构简式是_____________________________。 (3) 下列物质中,一定条件下能与A发生反应的是________。 A.H2 B.Na C.酸性KMnO4溶液 D.Br2 (4)有机物B是A的同分异构体,1 mol B可与1 mol Br2加成。该有机物中所有碳原子在同一个平面,没有顺反异构现象,则B的结构简式是______________。 20.(12分)化合物A(分子式为C6H6O)是一种有机化工原料,在空气中易被氧化。A的有关转化反应如下(部分反应条件略去): 已知: ①已知K2Cr2O7是一种常用强氧化剂 ② ③(R表示烃基,R′和R″表示烃基或氢) (1)写出A的结构简式: 。 (2)某化合物是E的同分异构体,且分子中只有两种不同化学环境的氢。写出该化合物的结构简式: (任写一种)。 (3)F和D互为同分异构体。写出反应E→F的化学方程式: ,此反应类型是 。 (4)根据已有知识并结合相关信息,写出以A和HCHO为原料制备的合成路线流程图。无机试剂任用,合成路线流程图示例: 【答案】 1.B 2.C 3.C 4.A 5.D 6.D 7.D 8.A 9.A 10.B 11.C 12.B 13.BD 14.AD 15.BC 16.(14分);C7H12, ,2,3 二甲基戊烷;3种; 17.(13分) 取代 (2)除去HBr中混有的溴蒸气 石蕊试液变红,导管口有白雾产生 E中有淡黄色沉淀生成或石蕊试液变红(任写一个) (3)DEF (4)对尾气进行处理,防止对空气造成污染 18. (12分)(1) 羟基 羧基 (各1分) (2) A (3)4 (4)①D:CH3COOH E: ② 19.(9分)答案 (1)1mol, 1.6mol,0.2mol (2)ABCD (3) (4) 20. (12分)(1) (2)或 (3),消去反应 (4) 查看更多