- 2021-08-23 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
【化学】黑龙江省七台河市第一中学2019-2020学年高一下学期期中考试试题
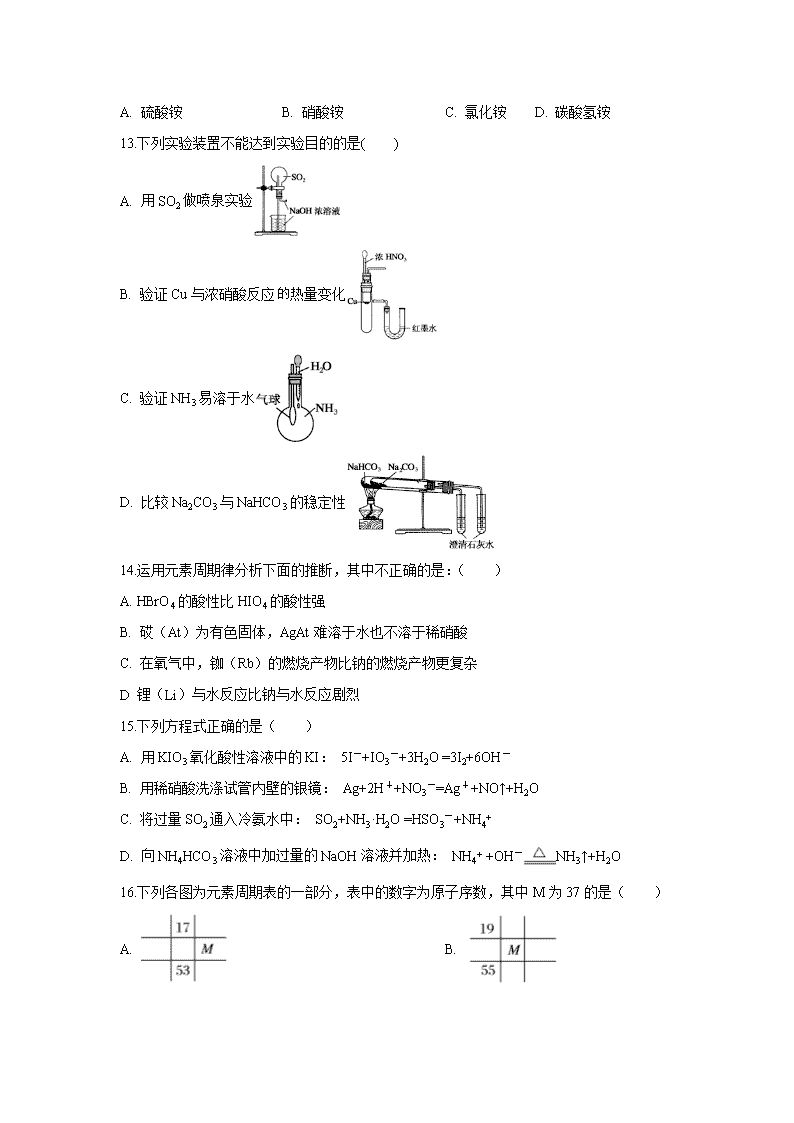
黑龙江省七台河市第一中学2019-2020学年高一下学期期中考试试题 可能用到的相对原子质量:H:1 C:12 N:14 O:16 Mg:24 Cu:64 一、选择题(单项选择,每小题3分,共25小题,计75分) 1. 化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是( ) ①加快化石燃料的开采与使用;②研发易降解的生物农药;③应用高效洁净的能源转换技术;④田间焚烧秸秆;⑤推广使用节能环保材料。 A. ①③⑤ B. ②③⑤ C. ①②④ D. ②④⑤ 2.关于SO2与NO2的下列说法正确的是( ) A. 都能引起光化学烟雾 B. 都能使石蕊试液先变红后褪色 C. 都是酸性氧化物 D. 都能与氢氧化钠溶液反应 3.下列表达式不正确的是( ) A. 四氯化碳分子的电子式: B. S2-的结构示意图: C. 氮气分子结构式: D. 氚的原子符号: 4.是重要的核工业原料。下列有关、说法正确的是( ) A 原子核中含有92个中子 B. 原子核外有143个电子 C. 与互为同位素 D. 与互为同素异形体 5.下列关于物质用途的说法正确的是( ) ①水玻璃是制备硅胶和木材防火剂的原料;②氨用做制冷剂;③氢氟酸可以用来刻蚀玻璃; ④晶体硅是制备光导纤维的原料;⑤利用氯气的毒性可以消灭田鼠;⑥二氧化硫既可做漂白毛、丝、纸张的漂白剂,又可做食物的增白剂;⑦晶体硅是良好的半导体材料,可以制成光电池 A. ①②③④⑤ B. ①③④⑤⑥ C. ①②③⑤⑦ D. ③④⑤⑥⑦ 6.下列各组物质的性质比较正确的是( ) A. 稳定性:AsH3<PH3<NH3<CH4 B. 沸点: H2S<H2Se<H2Te<H2O C. 密度:Li<Na<K<Rb D. 酸性:H3BO3<H2CO3<HNO3<H3PO4 7.已知某元素的原子序数,则不能推出该元素原子的( ) A. 质子数 B. 中子数 C. 电子数 D. 核电荷数 8.对下列事实解释错误的是( ) A. 向蔗糖中加入浓H2SO4后出现发黑现象,说明浓H2SO4具有脱水性 B. 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 C. 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 D. 反应CuSO4+H2S=CuS↓+H2SO4能进行,说明硫化铜既不溶于水,也不溶于稀硫酸 9. 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列叙述错误的是( ) A. T的氧化物能与碱反应 B. 元素的非金属性:Q强于W C. W的单质共热时,能与其最高价氧化物的水化物浓溶液反应 D. 原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物 10. 下列叙述中能说明金属A肯定比金属B的活泼性强的是 ( ) A. A原子的最外层电子数比B原子的最外层电子数少 B. A原子电子层数比B原子电子层数多 C. 1mol A从酸中置换出的H2比1molB从酸中置换的H2多 D. 常温时,A能从稀盐酸中置换出氢,而B不能 11. 天然存在的Fr(钫)极微量,它的 21种同位素都有放射性,它是碱金属中最重的元素,根据它在周期表中的位置预言其性质,其中不正确的是( ) A. 在已知碱金属中它具有最多的电子层 B. 在空气中燃烧的时候,生成氧化物Fr2O C. 氧化物对应的水化物是极强的碱 D. 单质的熔点不如Na的高 12.一种盐X与烧碱混合共热,可放出无色气体Y,Y经一系列氧化后再溶于水可得Z溶液,Y和Z反应又生成X,则X是( ) A. 硫酸铵 B. 硝酸铵 C. 氯化铵 D. 碳酸氢铵 13.下列实验装置不能达到实验目的的是( ) A. 用SO2做喷泉实验 B. 验证Cu与浓硝酸反应热量变化 C. 验证NH3易溶于水 D. 比较Na2CO3与NaHCO3的稳定性 14.运用元素周期律分析下面的推断,其中不正确的是:( ) A. HBrO4的酸性比HIO4的酸性强 B. 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 C. 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 D 锂(Li)与水反应比钠与水反应剧烈 15.下列方程式正确的是( ) A. 用KIO3氧化酸性溶液中的KI: 5I-+IO3-+3H2O =3I2+6OH- B. 用稀硝酸洗涤试管内壁的银镜: Ag+2H++NO3-=Ag++NO↑+H2O C. 将过量SO2通入冷氨水中: SO2+NH3·H2O =HSO3-+NH4+ D. 向NH4HCO3溶液中加过量的NaOH溶液并加热: NH4+ +OH-NH3↑+H2O 16.下列各图为元素周期表的一部分,表中的数字为原子序数,其中M为37的是( ) A. B. C. D. 17.含有相同质子数和电子数的两种微粒之间的关系不正确的是( ) A. 它们可能是同一元素的不同核素 B. 可能是不同分子 C. 可能是不同的离子 D. 可能是一种分子和一种离子 18. 下列每组物质中含有的化学键类型相同的是( ) A. NaCl、HCl、NaOH B. Cl2、Na2S、SO2 C. HBr、CO2、SiO2 D. NH4Cl、H2O2、H2O 19.下列说法正确的是( ) ①离子化合物中一定含有离子键;②含有共价键的化合物一定是共价化合物;③非金属单质分子中一定含有非极性共价键;④分子间作用力比化学键弱得多;⑤含有离子键的化合物中一定含有金属元素;⑥氢键不是化学键;⑦不同元素组成的多原子分子中的化学键一定都是极性键 A. ①④⑥ B. ①②⑤⑦ C. ①③④⑥ D. ③⑥⑦ 20. 几种短周期元素的原子半径及主要化合价如下表 元素代号 X Y Z M R Q 原子半径 1.86 0.99 1.43 1.60 0.75 0.74 最高正价 +1 +7 +3 +2 +5 最低负价 -1 -3 -2 下列说法不正确的是( ) A. 由元素X和Q组成的化合物可能含有共价键 B. X、Z、R的最高价氧化物对应水化物可彼此反应 C. 离子半径:r(M2+)查看更多
相关文章
- 当前文档收益归属上传用户