2020届高三化学11月月考试题新版 新人教版
2019届高三化学11月月考试题
7.有些古文或谚语包含了丰富的化学知识,下列解释不正确的是
选项
古文或谚语
化学解释
A
以曾青涂铁,铁赤色如铜
置换反应
B
日照香炉生紫烟
碘的升华
C
煮豆燃豆萁
化学能转化为热能
D
雷雨肥庄稼
自然固氮
8.分子式为C4H8O的有机物,能与新制氢氧化铜共热反应生成砖红色沉淀的同分异构体有
A.2种 B.3种 C.4种 D.5种
9.设NA为阿伏伽德罗常数的值,下列说法正确的是
A.pH=2的NaHSO4溶液中的SO42-的数目为0.01Na
B.0.lmolNa2O2与足量的潮湿的CO2反应转移的电子数为0.1Na
C.标准状况下,6.0gNO和2.24LO2混合,所得气休的分子数目为0.2Na
D.室温下,lLpH=3的NH4Cl溶液中,由水电离的H+数目为10-11 Na
10.下列装置合理且能达到实验目的的是
A.实验室用装置①制取氨气
B.装置②将化学能转化为电能
C.装置③可用于分离沸点相差较大的互溶液体混合物
D.装置④可用于Fe(OH)2的制取,并能防止Fe(OH)2被氧化
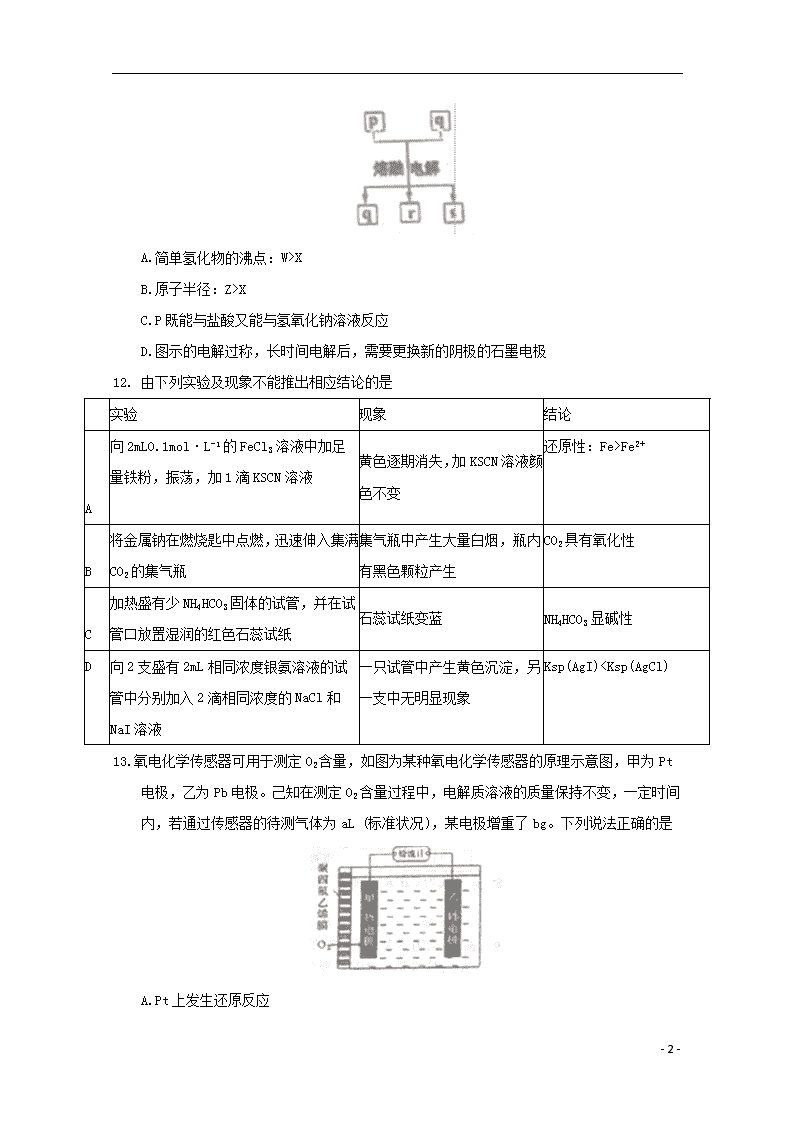
11.短周期元素W、X、Y、Z的原子序数依次增加,其简单离子电子层结构相同,其中Y与Z为金属元素,Z离子的半径在同周期中的最小。 p、q是它们中的部分元素组成的化合物,r是W的单质,s是Z的单质,这些物质的转化关系如图,下列说法不正确的是
- 8 -
A.简单氢化物的沸点:W>X
B.原子半径:Z>X
C.P既能与盐酸又能与氢氧化钠溶液反应
D.图示的电解过称,长时间电解后,需要更换新的阴极的石墨电极
12. 由下列实验及现象不能推出相应结论的是
实验
现象
结论
A
向2mL0.1mol·L-1的FeCl3溶液中加足量铁粉,振荡,加1滴KSCN溶液
黄色逐期消失,加KSCN溶液颜色不变
还原性:Fe>Fe2+
B
将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶
集气瓶中产生大量白烟,瓶内有黑色颗粒产生
CO2具有氧化性
C
加热盛有少NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸
石蕊试纸变蓝
NH4HCO3显碱性
D
向2支盛有2mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液
一只试管中产生黄色沉淀,另一支中无明显现象
Ksp(AgI)
”“<”或“=”,下同),平衡常数Ka Kb Kc。
②若B点时X=3,则平衡常数Kb= (代入数据列出算式即可)。
- 8 -
③下列措施能同时满足增大反应速率和提髙CO2转化率的是 。
a.升高温度 b.加入催化剂 c.增大投料比X d.增加压强
e.将产物从反应体系中分离出来
(3)乙烯也可作为制备甲酸的基础工业原料,常温时,HCOOH的电离平衡常数
Ka=1.8×l0-4mol·L-1,pH=12的HCOONa和含少量NaOH混合溶液中。
①书写HCOONa的水解离子反应方程式 。
②该溶液中离子浓度关系:= mol·L-1
③若0. lmol/L的HCOONa溶液中加入等体积的0.09mol/LHCOOH,配制了pH=6.8的溶液,则该溶液中微粒浓度由小到大的顺序为 。(不考虑水分子)
35.[化学-选修3:物质结构与性质](15分)
硫是一种重要的非金属元素,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是 。
(2)①硫单质的一种结构为,杂化方式为 ,该物质 (填“可溶”或“难溶”)于水。
②SO42-、CS2、CO32-键角由大到小的顺序是 。
(3)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
①NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点
FeO NiO(填“<”或“>”)
②铁有δ、Υ、ɑ三种同素异形体,各晶胞如下图,则δ、ɑ两种晶胞中铁原子的配位数之比为 。
(4)某钙钛型复合氧化物如图1所示,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、
Cr、Mn、Fe等时,这种化合物具有CMR效应。
- 8 -
①用A、B、O 表示这类特殊晶体的化学式: 。
②已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛化合物La1-xAxMnO3(x<0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁—铁磁、铁磁—顺磁及金属—半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为 。(用x表示)
③下列有关说法正确的是 。
A.镧、锰、氧分别位于周期表f、d、P区
B.氧的第一电离能比氮的第一电离能大
C.锰的电负性为1.59,Cr的电负性为1.66,说明锰的金属性比铬强
D.铬的堆积方式与钾相同,则其堆积方式如图2所示
36.[化学-选修5:有机化学基础](15分)
树脂交联程度决定了树脂的成膜性。下面是—种成膜性良好的醇酸型树脂的合成路线,如下图所示:
(1)合成A的化学方程式是 。
(2) B的分子式为C4H7Br,且B不存在顺反异构,B的结构简式为 ,A到B步骤的反应类型是 。
(3)E中含氧官能团的名称是 ,D的系统命名为 。
(4)下列说法正确的是 。
A.1mol化合物C最多消耗3molNaOH
B.1mol化合物E与足量银氨溶液反应产生2molAg
C.F不会与Cu(OH)2悬浊液反应
D.丁烷、1-丁醇、化合物D中沸点最高的是丁烷
- 8 -
(5)写出D、F在一定条件下生成醇酸型树脂的化学方程式 。
(6) 的符合下列条件的同分异构体有 种。
①苯的二取代衍生物:②遇FeCl3溶液显紫色③可发生消去反应
7.B 8.A 9.B 10.D 11.D 12.C 13.C
26. (14分,各2分)
(1)浓氨水与碱石灰(或CaO、NaOH固体)
(2)降低温度,提高反应物的转化率;通过观察气泡,调节NH3与CO2通入比例;三颈烧瓶;c
(3)稀硫酸(其他合理答案也给分)
(4) 80%
27.(14分,各2分)
(1)铁粉
(2) c
(3) 4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S
(4)蒸发浓缩、冷却结晶、过滤、洗涤、干燥(未写过滤洗涤干燥扣一分)
(5)促进Fe3+的水解生成聚铁胶体
(6)4SO2+4NO2+12NH3+3O2+6H2O=4(NH3)2SO4+4NH4NO3
(7)31.11%
28. (15分)
- 8 -
(1) -2(b-a)或2(a-b) (2分)
(2)①< (1分);=(1分); > (1分)
②等合理答案(2分)
③c d(2分)
(3) HCOO- +H2O=HCOOH+OH-(2分) 1.8×106(2分)
c(OH-) CO32- >SO42-
(3)①< ②4:3
(4)①ABO3 ②(1-x):x ③A、C
36.[化学——选修5:有机化学基础](15分,除标注外,每空1分)
(1)
(2)CH3CHBrCH=CH2 取代反应( 1分)
(3)醛基 1, 2, 3-丁三醇
(4) A
(5)
(6)6
- 8 -