2019-2020学年吉林省白城市通榆县第一中学高二上学期第二次月考化学试题 word版
白城市通榆县第一中学2019-2020学年高二上学期第二次月考
化学试卷
可能用到的相对原子质量: C-12 H-1 O-16
一.选择题(每小题只有一项符合题意,每小题3分,共66分)
1.未来人类最理想的燃料是( )
A.无烟煤 B.石油 C.天然气 D.氢气
2..将A与B的混合物15mol放人容积为2L的密闭容器里,在一定条件下发生反应:2A(气)+3B(气) C(气)+2D(气),经过15min达到平衡,达平衡时容器内的压强是反应前的。则以B气体的浓度变化表示的反应速率是( )
A.0.15mol·L-1·min-1 B.0.3mol·L-1·min-1
C.0.45mol·L-1·min-1 D.0.6mol·L-1·min-1
3.在一定温度下的定容容器中,当下列各量不再发生变化时,表明反应A(g)+2B(g)C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体的总质量 ⑧混合气体的总体积 ⑨C、D的分子数之比为1:1.
A.①②③④⑤⑥⑦⑧ B.①③④⑤ C.①②③④⑤⑦ D.①③④⑤⑧⑨
4.对于可逆反应:2SO2+O22SO3,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A.增大压强 B.升高温度 C.使用催化剂 D.多充O2
5.某反应的△H=+100kJ·mol﹣1,下列有关该反应的叙述正确的是( )
A.正反应活化能小于100 kJ·mol﹣1 B.逆反应活化能一定小于100 kJ·mol﹣1
C.正反应活化能不小于100 kJ·mol﹣1 D.正反应活化能比逆反应活化能小100 kJ·mol﹣1
6.已知:a.C2H2(g)+H2(g)=C2H4(g) △H<0; b.2CH4(g)=C2H4(g)+2H2(g) △H>0
判断以下三个热化学方程式中△H1、△H2、△H3的大小顺序是( )
①C(s)+2H2(g)=CH4(g) △H1 ②C(s)+H2(g)=1/2C2H4(g) △H2
③C(s)+1/2H2(g)=1/2C2H2(g) △H3
A. △H2>△H3>△H1 B. △H3>△H2>△H1
C. △H3>△H1>△H2 D. △H1>△H2>△H3
7.相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)2NH3(g)△H=﹣92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
容器
编号
起始时各物质的物质的量/mol
达平衡时体系能量的变化
N2
H2
NH3
①
1
3
0
放出热量:23.15 kJ
②
0.9
2.7
0.2
放出热量:Q
下列叙述不正确的是( )
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15kJ
D.若容器①体积为0.5L,则平衡时放出的热量小于23.15kJ
8.判断一个化学反应的自发性常用焓判据和熵判据,则在下列情况下,可以判定反应一定自发进行的是( )
A.ΔH>0,ΔS>0 B.ΔH<0,ΔS>0 C.ΔH>0,ΔS<0 D.ΔH<0,ΔS<0
9.已知某可逆反应:mA(g)+nB(g)pC(g) 在密闭容器中进行,下图表示在不同时刻时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是 ( )
A、T2>T1 P1
P2 m+nT2 P2>P1 m+n>P △H<0 D、T1>T2 P1P △H>0
10.在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )。
A. 图Ⅰ表示温度对化学平衡的影响,且
甲的温度较高
B. 图Ⅱ表示t0时刻使用催化剂对反应速
率的影响
C. 图Ⅲ表示t0时刻增大O2的浓度对反应
速率的影响
D. 图Ⅳ表示t0时升温对反应速率的影响
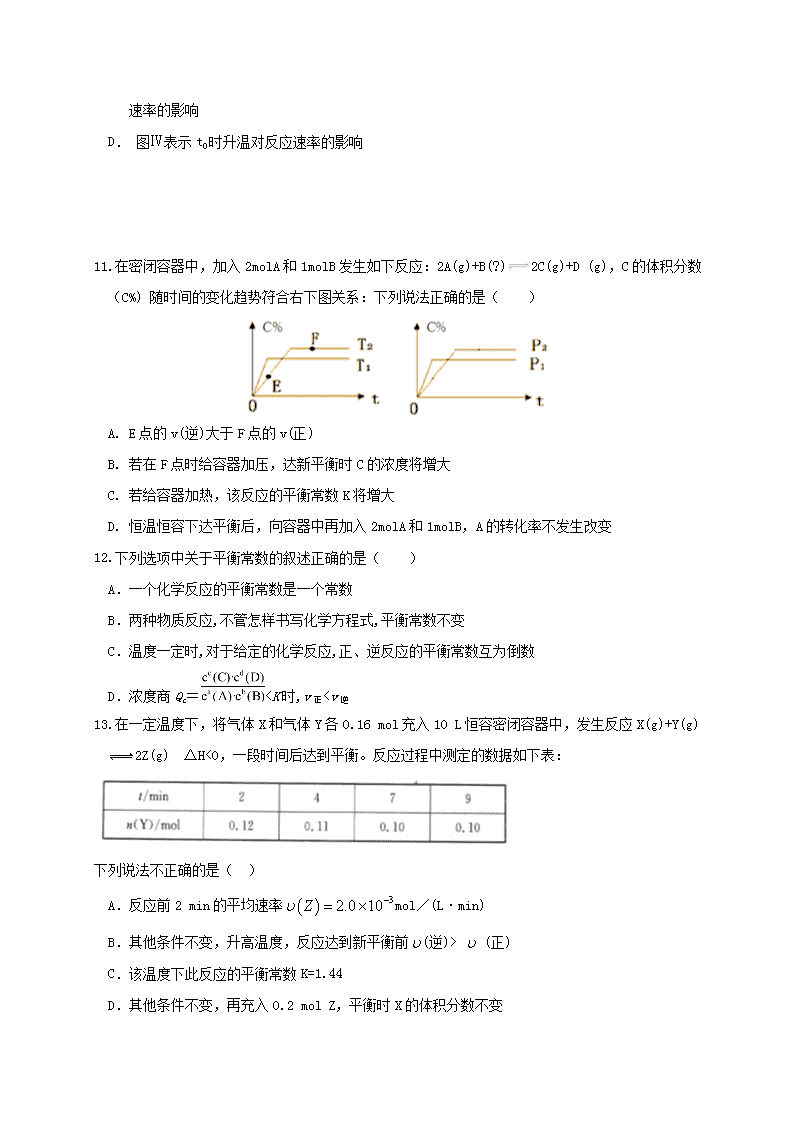
11.在密闭容器中,加入2molA和1molB发生如下反应:2A(g)+B(?)2C(g)+D (g),C的体积分数(C%) 随时间的变化趋势符合右下图关系:下列说法正确的是( )
A. E点的v(逆)大于F点的v(正)
B. 若在F点时给容器加压,达新平衡时C的浓度将增大
C. 若给容器加热,该反应的平衡常数K将增大
D. 恒温恒容下达平衡后,向容器中再加入2molA和1molB,A的转化率不发生改变
12.下列选项中关于平衡常数的叙述正确的是( )
A.一个化学反应的平衡常数是一个常数
B.两种物质反应,不管怎样书写化学方程式,平衡常数不变
C.温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数
D.浓度商Qc= (正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变
14.在一定温度下,一定体积的密闭容器中有如下平衡:H2(g)+I2(g)2HI(g)。已知H2和I2的起始浓度均为0.10 mol·L-1时,达平衡时HI的浓度为0.16 mol·L-1。若H2和I2的起始浓度均变为0.20 mol·L-1,则平衡时H2的浓度(mol·L-1)是
A. 0.16 B. 0.08 C. 0.04 D. 0.02
15.在容积为2 L的密闭容器中充入2 mol SO2和一定量O2,发生反应2SO2+O22SO3,当反应进行到4 min时,测得n(SO2)=0.4 mol。若反应进行到2 min时,容器中SO2的物质的量是( )
A.等于1.6 mol B.等于1.2 mol C.大于1.6 mol D.小于1.2 mol
16.反应速率V和反应物浓度的关系是用实验的方法测定的,化学反应:H2+Cl2=2HCl的反应速率V可以表示为:v=k·Cm(H2)·Cn(Cl2),式中的k为常数,m和n的值以可用下列表中数据确定之。
H2(mol/L)
Cl2(mol/L)
V(mol/L·S)
1.0
1.0
1.0k
2.0
1.0
2.0k
2.0
4.0
4.0k
由此可以推得,m和n的值正确的是( )
A.m=1,n=2 B. m=、n= C.m=1,n= D.m=,n=1
17.某温度下,在2L密闭容器中投入一定量的A、B发生反应:3A(g) + bB (g) cC(g) ΔH=-Q kJ·mol-1(Q>0)。12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如右图所示。下列说法正确的是( )
A.前12s内,A的平均反应速率为0.025mol·L-1·s-1
B.12s后,A的消耗速率等于B的生成速率
C.化学计量数之比b :c=1 :2
D.12s内,A和B反应放出的热量为0.2Q kJ
18.对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时,4v正(NH3)=5v逆(H2O)
B. 若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率减小
D. 达到平衡时,若减小容器体积,则NH3的转化率会增大
19.一定条件下,将3 mol A和1 mol B两种气体混合于容积为2
L的密闭容器中,发生反应:3A(g)+B(g) xC(g)+2D(s)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol/L。下列判断正确的是( )
A. 该条件下此反应的平衡常数约为0.91
B. 2 min内A的平均反应速率为0.3 mol/(L·s)
C. B的转化率为60%
D. 混合气体的密度不再改变时,该反应不一定达到平衡状态
20.在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:
3A(g)+ B(g) xC(g) + D(s),向甲中通入6molA和2 molB,向乙中通入
1.5molA、0.5molB、3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为20%,下列叙述中不正确的是( )
A.若平衡时,甲、乙两容器中A的物质的量不相等,则X=4
B.平衡时,甲、乙两容器中A、B的物质的量之比相等
C.平衡时甲中A的体积分数为40%
D.若平衡时两容器中的压强不相等,则两容器中压强之比为8:5
21.将2 mol SO2和2 mol SO3气体混合于某固定体积的密闭容器中,在一定条件下反应:2SO2(g)+O2(g) 2SO3(g),平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3的物质的量大于W mol的是()
A.2 mol SO2+1 mol O2 B.4 mol SO2+1 mol O2
C.3 mol SO2+1 mol SO3 D.2 mol SO2+1 mol O2+2 mol SO3
22.将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,发生反应NH2COONH4 (s)2NH3 (g)+ CO2 (g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是( )
A. C点对应状态的平衡常数K(C)=10-3.638
B. 该反应的△H>0
C. 30 ℃时,B点对应状态的v(正)<v(逆)
D. NH3的体积分数不变时,该反应一定达到平衡状态
填空题
23.在一定条件下,可逆反应2NO2(g) N2O4(g) ΔH<0达到平衡,当分别改变下列条件时,请填空:
(1)保持容器容积不变,通入一定量NO2,则达到新平衡时NO2的百分含量________(填“增大”“减小”或“不变”,下同),保持容器容积不变,通入一定量N2O4,则达到新平衡时NO2的百分含量________。
(2)保持压强不变,通入一定量N2O4,则达到平衡时NO2的百分含量________;保持压强不变,通入一定量N1O2,则达到平衡时NO2的百分含量________。
(3)保持容器容积不变,通入一定量氖气,则达到平衡时NO2的转化率_______;保持压强不变,通入氖气使体系的容积增大一倍,则达到平衡时NO2的转化率________。
24.在一定条件下,可逆反应A+BmC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
(1)温度T1________T2(填“大于”“等于”或“小于”)。
(2)正反应是________反应(填“吸热”或“放热”)。
(3)如果A、B、C均为气体,则m________2(填“大于”“等
于”或“小于”)。
(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀
有气体,则体系的压强________(填“增大”“减小”或
“不变”),平衡________移动(填“向正反应方向”“向逆反应方向”或“不”)。
25.甲醇是重要的化工基础原料和清洁液体燃料,工业上可利用CO或CO2来生产甲醇。已知制备甲醇的有关化学反应以及在不同温度下的化学平衡常数如下表所示:
化学反应
平衡常数
温度/℃
500
800
①2H2(g)+CO(g) CH3OH(g)
K1
2.5
0.15
②H2(g) +CO2 (g) H2O(g)+CO(g)
K2
1.0
2.50
③3H2(g)+CO2(g) CH3OH(g)+H2O(g)
K3
(1)在恒容密闭容器中发生反应②,达到平衡后升高温度,下列说法正确的是_______。
a.平衡正向移动
b.混合气体的平均相对分子质量增大
c.CO2的转化率增大
(2)K1、K2、K3的关系是:K3=_______。
(3)500℃时测得反应在某时刻,H2(g)、CO2(g)、CH3OH(g)H2O(g)的浓度(mol/L)分别为0.2、0.1、0.01、0.2,则此时V正____V逆(填“>”“=”“<”)。
(4)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图所示,若开始加入2mol/LH2和1mol./LCO,则B点时化学平衡常数为___________。
(5)相同温度下,在甲、乙两个容积相等的恒容密闭容器中,投入
H2和CO2,发生反应②,起始浓度如下表所示。其中甲经2min
达平衡,平衡时c(H2O)=0.05mol/L,甲中CO2的转化率为_____,
乙中CO2的转化率___甲。(填“大 于”、“等 于”或“小于”)
起始浓度
甲
乙
c(H2)/mol/L
0.10
0.20
c(CO2 )/ mol/L
0.10
0.20
26. 1,2-二氯丙烷(CH2ClCHClCH3)是重要的化工原料,工业上可用丙烯加成法生产,主要副产物为3-氯丙烯(CH2=CHCH2C1) ,反应原理为
i.CH2=CHCH,3(g)+Cl2(g)CH2ClCHClCH3(g) ΔH1= -134 kJ mol-1
ii.CH2=CHCH,3(g)+Cl2(g)CH2=CHCH2Cl (g)+HCl(g) ΔH2= -l02 kJ mol-1
已知:相关化学键的键能数据如下表所示:
化学键
C=C
C—C
C—Cl
Cl—Cl
E/( kJ mol-1)
611
x
328
243
请回答下列问题:
(1)由反应i计算出表中x=_____________。
(2)一定温度下,密闭容器中发生反应i和反应ii,达到平衡后增大压强,CH2C1CHC1CH3的产率
____________(填“增大”“减小”或“不变”),理由是__________________。
(3)T1℃时,向10L恒容的密闭容器中充入1 mol CH2=CHCH2C1和2 mol HC1,只发生反应CH2=CH CH2Cl (g)+HCl(g)CH2ClCHClCH3(g) ΔH3。5min反应达到平衡,测得 5 min内,用CH2ClCHClCH3表示的反应速率 v(CH2ClCHClCH3)=0.016 mol·L-1 min-1。
①平衡时,HCl的体积分数为__________________(保留三位有效数字)。
②保持其它条件不变,6 min时再向该容器中充入0.6 mol CH2=CHCH2Cl、0.2molHC1和0.1mol CH2ClCHClCH3,则起始反应速率 v正(HCl)______________ V逆(HCl)(填“>”“<” 或“=”).
(4)一定压强下,向密闭容器中充入一定量的CH2=CHCH3和C12发生反应ii。设起始的 =w,平衡时Cl2的体积分数(φ)与温度(T)、w的关系如图甲所示。W=1时,正、逆反应的平衡常数(K)与温度(T)的关系如图乙所示。
①图甲中,w2__________(填“>”“<”或“=”)1
②图乙中,表示正反应平衡常数的曲线为____________(填“A”或“B”),理由为________________。
③T1K下,平衡时氯气的转化率a(Cl2)= ________________。
(5)起始时向某恒容绝热容器中充入1 mol CH2 =CHCH3和1 mol Cl2发生反应ii,达到平衡时,容器内气体压强_________________(填“增大”“减小”或“不变”)。
27.近年科学家提出“绿色自由”构想。把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应生成可再生能源甲醇。其工艺流程如图所示:
(1)分解池中主要物质是_______________。
(2)在合成塔中,若有4400 g CO2与足量H2反应,生成气态的H2O和甲醇,可放出5370 kJ的热量,写出该反应的热化学方程式_______________。
(3)该工艺在哪些方面体现了“绿色自由”构想中的“绿色”_______________。
(4)一定条件下,往2L恒容密闭容器中充入1 mol CO2和3 mol H2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如下图所示:
(图中c点的转化率为66.67%,即转化了2/3)
①催化剂效果最佳的反应是________(填“反应I”,“反应II”,“反应III”)。
②b点v (正)_________v (逆)(填 “>”, “<”, “=”)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是____________。
④c点时该反应的平衡常数K =____________________。
答案
1D 2A 3B 4B 5C 6B 7C 8B 9C 10B 11B 12C 13A 14C 15D
16C 17C 18C 19A 20C 21D 22D
23.答案(1)减小 减小 (2)不变 不变 (3)不变 减小
24.答案(1)大于 (2)放热 (3)大于 (4)增大 不
25.答案(1) ac
(2) K1·K2
(3) =
(4) 25
(5) 50% ; 等于
26.答案332 增大 增大压强,反应ii的平衡不移动,反应i的平衡正向移动。所以CH2C1CHC1CH3的产率增大 54.5% > > B 反应ii的正反应为放热反应。温度升高, 正反应的平衡常数减小 50% 增大
27.答案 (1). KHCO3(或碳酸氢钾) (2). CO2(g)+ 3H2(g)H2O(g)+ CH3OH(g) △H=== -53.7kJ/mol (3). 减少大气中CO2并产生清洁能源甲醇;K2CO3可循环使用;能量可以循环利用,低碳经济等。 (4). ① 反应I ②. > ③. 该反应为放热反应,温度升高,平衡逆向移动 ④. K=16/3 (或K=3.70)