2018-2019学年内蒙古包头市第四中学高二上学期第二次月考化学试题 Word版
包头四中2018-2019学年度第一学期第二次月考
高二年级化学试题
满分100分 时间90分钟 出题人:
一、选择题(每小题3分,共60分。每小题只有一个正确选项)
1.关于右图所示的原电池,下列说法不正确的是
A.铜片为正极,锌片为负极
B.锌片溶解,质量减少
C.该装置将化学能转化为电能
D.电子由铜片经导线流向锌片
2.已知有如下热化学方程式
① 2C(s)+O2(g)=2CO(g) ΔH1
② 2H2(g)+O2(g)=2H2O(g) ΔH2
③ C(s)+ H2O(g)=CO(g) +H2(g) ΔH3
则下列关系正确的是:
A. ΔH3=(ΔH1+ΔH2)/2 B. ΔH3= ΔH2-ΔH1
C. ΔH3=(ΔH2-ΔH1)/2 D. ΔH3= (ΔH1-ΔH2)/2
3.某实验小组学生用50 mL 0.50 mol·L−1盐酸与50 mL 0.55 mol·L−1 NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量计算中和热。下列说法正确的是
A. 实验过程中没有热量损失
B. 图中实验装置缺少环形玻璃搅拌棒
C. 烧杯间填满碎泡沫塑料的作用是固定小烧杯
D. 酸或碱的物质的量越大,所测中和热的数值越大
4.在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:
C(s)+H2O(g) CO(g)+H2(g)。不能确定上述可逆反应在一定条件下已达到化学平衡状态的是
A. 体系的体积不再发生变化
B. v正(CO)=v逆(H2O)
C. 生成n mol CO的同时消耗n mol H20
D. 1 mol H—H键断裂的同时断裂2 mol H—O键
5.在2A(g)+B(g)3C(g)+4D(g)反应中,表示该反应速率最快的是
A. v(A)=0.5 mol·L-1·min-1 B. v(B)=0.003 mol·L-1·s-1
C. v (C)=0.8 mol·L-1·min-1 D. v(D)=0.01 mol·L-1·s-1
6.在不同温度下(T1 <T2),可逆反应2X(g) 2Y(g)+Z(g) ΔH<0中,生成物Z在反应平衡混合物中的体积分数()与反应时间(t)的关系有以下图示,正确的是
A. B.
C. D.
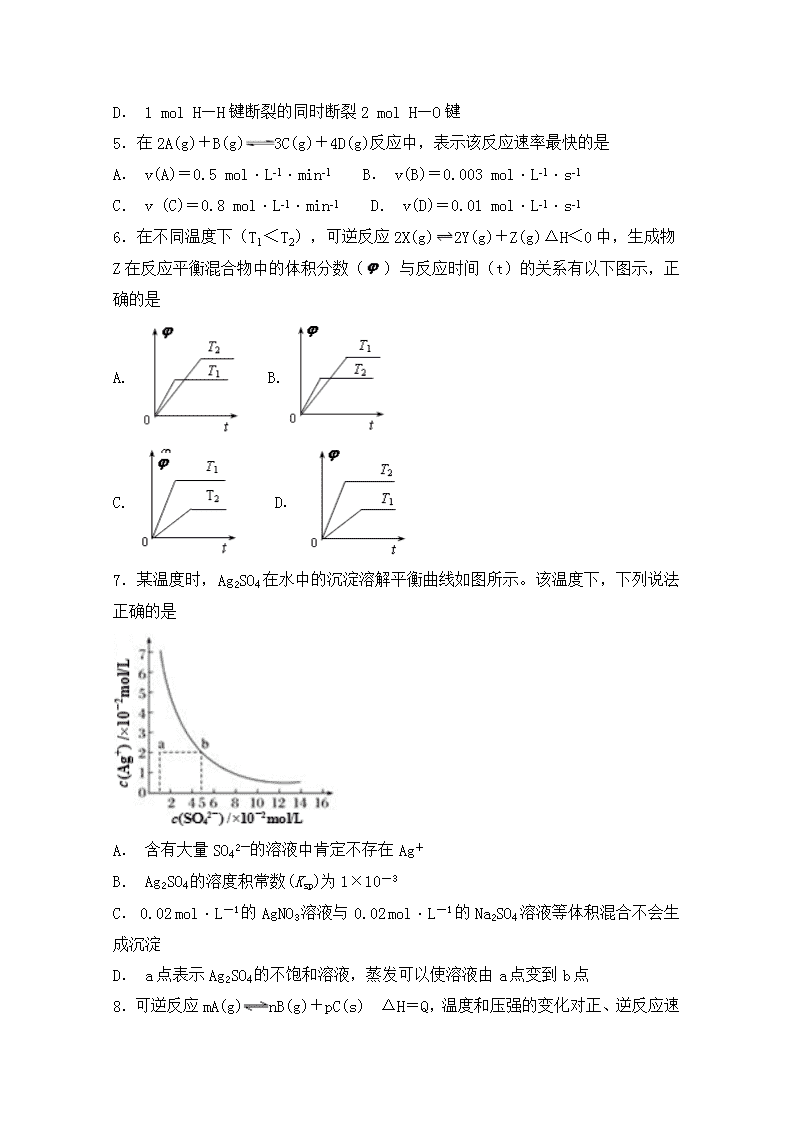
7.某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是
A. 含有大量SO42-的溶液中肯定不存在Ag+
B. Ag2SO4的溶度积常数(Ksp)为1×10-3
C. 0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
D. a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点
8.可逆反应mA(g)nB(g)+pC(s) Δ
H=Q,温度和压强的变化对正、逆反应速率的影响分别符合右图中的两个图像,以下叙述正确的是
A. m>n,Q>0 B. m>n+p,Q>0 C. m
n,Q<0
9.常温下,0.1 mol·L-1 HF溶液的pH = 2,下列关于HF溶液的表述错误的是
A. HF是弱酸 B. c(H+)> c(HF)
C. c(HF) > c(OH-) D. c(H+) > c(F-)
10.0.1mol/L的CH3COOH溶液中CH3COOH CH3COO—+ H+对于该平衡,下列叙述正确的是
A. 加水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol/L盐酸,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
11.下列物质因发生水解而使溶液呈酸性的是
A. HNO3 B. CuCl2 C. K2CO3 D. NaCl
12.室温下进行的下列实验,不能达到预期目的是
实验内容
实验目的
A
向同体积同浓度H2O2溶液中,分别加入1 mol/L的CuCl2、FeCl3溶液
比较Cu2+、Fe3+对H2O2分解速率的影响
B
向Mg(OH)2浊液中滴加少量0.1 mol/L FeCl3溶液
比较Mg(OH)2和Fe(OH)3的溶解度
C
将SO2通入酸性高锰酸钾溶液中
探究SO2的还原性
D
测定相同浓度的NaClO溶液,CH3COONa溶液的pH
比较HClO和CH3COOH的酸性强弱
13.常温下,用0.100 0 mol·L-1的盐酸滴定20.00
mL未知浓度的氨水,滴定曲线如图所示,滴加20.00 mL盐酸时所得溶液中c(Cl-)=c(NH4+)+c(NH3·H2O)+c(NH3)。下列说法错误的是
A. 该氨水的浓度为0.100 0 mol·L-1
B. 点①溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=2c(Cl-)
C. 点②溶液中c(NH4+)=c(Cl-)
D. 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-)
14.下列叙述正确的是
A. 图a,插入海水中的铁棒,越靠近底端腐蚀越严重
B. 图b,铁上镀铜,铁应与外加电源负极相连,一段时间后CuSO4溶液浓度减小
C. 图c,验证铁钉发生析氢腐蚀
D. 图d,片刻后在Fe电极附近滴入K3[Fe(CN)6]溶液,验证Fe电极被腐蚀
15.美国一个海军航空站曾安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600 ℃~700 ℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为:2H2+O2===2H2O,负极反应为:2H2+2CO32—-4e-===2H2O+2CO2,则下列推断中正确的是
A. 正极反应为4OH--4e-===O2↑+2H2O
B. 该电池的电极没有参加反应
C. 电池供应1mol水蒸气,转移的电子数为4 mol
D. O2从正极通入,发生氧化反应
16.空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。下图为RFC工作原理示意图,有关说法正确的是
A. 当有0.2 mol电子转移时,a极产生3.2g O2
B. b极上发生的电极反应是:2 H+ +2e- = H2↑
C. c极上进行还原反应,B中的H+可以通过隔膜进入A
D. d极上发生的电极反应是:O2+2H2O + 4e- = 4OH-
17.常温下,0.1mol/L的下列溶液酸性最强的是
A. NaHSO4 B. NaHSO3 C. Al2(SO4)3 D. CH3COOH
18.在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
A. 平衡向逆反应方向移动了 B. 物质A的转化率减小了
C. 物质B的质量分数增加了 D. a>b
19.常温下,对下列四种溶液的叙述正确的是
①
②
③[]
④
pH
10
10
4
4
溶液
氨水
氢氧化钠溶液
醋酸溶液
盐酸
A.四种溶液分别加水稀释10倍,pH变化最大的是①和④
B.②、④两溶液相比,两者的kw相同
C.①、②、③中分别加入少量的醋酸铵固体后,三种溶液的pH均减小
D.①、④两溶液按一定体积比混合,所得溶液中离子浓度顺序一定为:
c(NH4+)>c(Cl-)>c(H+)> c(OH-)
20.下列可用于测定溶液pH且精确度最高的是
A.酸碱指示剂 B.pH计 C.精密pH试纸 D.广泛pH试纸
二、非选择题(本题包括3小题,共40分)
21.(14分)氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题。
Ⅰ.已知H—H键的键能为436kJ·mol-1,N—H键的健能为391kJ·mol-1,NN键的键能是945.6 kJ·mol-1,则反应NH3(g) N2(g)+ H2(g)的ΔH=______,若在某温度下其平衡常数为K,则N2(g)+3H2(g) 2NH3(g)的平衡常数K1=___________(用K表示)
Ⅱ.氯氨是氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯氨、二氯氨和三氯氨(NH2Cl、NHCl2和NCl3),副产物少于其它水消毒剂。
(1)工业上可利用反应2Cl2(g)+NH3(g)NHCl2 (l)+2HCl(g)制备二氯胺。
在恒温条件下,将2molCl2和1molNH3充入某密闭容器中发生上述反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示。则A、B、C三点中Cl2转化率最高的是________点( 填“A” “B”或“C”);计算C点时该反应的压强平衡常数Kp(C)=_____________(Kp是平衡分压代替平衡浓度计算,分压= 总压×物质的量分数。)
(2) 用Cl2和NH3反应制备三氯胺的方程式为3Cl2(g)+NH3(g)NCl
3(l)+3HCl(g),向容积均为1L的甲、乙两个恒温(反应温度分别为400℃、T℃)容器中分别加入2molCl2和2molNH3,测得各容器中n(Cl2)随反应时间t的变化情况如下表所示:
t /min
0
40
80
120
160
n(Cl2)(甲容器)/mol
2.00
1.50
1.10
0.80
0.80
n(Cl2)(乙容器)/mol
2.00
1.45
1.00
1.00
1.00
①T℃__________400℃(填“>”或“<”)。
②该反应的ΔH__________0(填“>”或“<”)。
③对该反应,下列说法正确的是_________(填选项字母)。
A.若容器内气体密度不变,则表明反应达到平衡状态
B.若容器内Cl2和NH3物质的量之比为3∶1,则表明反应达到平衡状态
C.反应达到平衡后,其他条件不变,在原容器中按 = 继续充入一定量反应物,达新平衡后Cl2的转化率增大
D.反应达到平衡后,其他条件不变,加入一定量的NC13,平衡将向逆反应方向移动
22.(14分)回答下列问题:
(1)CuSO4的水溶液呈______(填“酸”“中”或“碱”)性,原因是(用离子方程式表示)___________;实验室在配制CuSO4溶液时,常先将CuSO4固体溶于较浓的硫酸中,然后用蒸馏水稀释到所需的浓度,以_____ (填“促进”或“抑制”)其水解。
(2)泡沫灭火器的灭火原理是(用离子方程式表示)____________________。
(3)已知在25℃:AgCl(s)Ag+(aq)+Cl-(aq) Ksp=1.8×10-10,Ag2S(s) 2Ag+(aq)+S2-(aq) Ksp=6.3×10-50,向浓度均为0.001 mol/L的NaCl和Na2S的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是________(填“AgCl”或“Ag2S”)。
(4)燃料电池能量转化率高,具有广阔的发展前景。天然气燃料电池中,在负极发生反应的物质是 _____(填化学式);如果该电池中的电解质溶液是KOH溶液,电极B电极上发生的电极反应式是:_____________。
23.(12分)用0.2000 mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000 mol/L的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“ 0”或“0”刻度线稍下,并记下读数;④量取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴甲基橙溶液;⑤用标准液滴定至终点,记下滴定管液面读数。⑥重复以上滴定操作2-3次。请回答:
(1)以上步骤有错误的是(填编号)_______________ _____
(2)步骤④中,量取20.00 mL待测液应使用________________(填仪器名称)
(3)步骤⑤滴定时眼睛应注视______________________________;判断到达滴定终点的依据是:______________________________________。
(4)以下是实验数据记录表
滴定
次数
盐酸体积
(mL)
NaOH溶液体积读数(mL)
滴定前
滴定后
1
20.00
0.00
18.10
2
20.00
0.00
16.20
3
20.00
0.00
16.16
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是__________
A. 锥形瓶装液前,留有少量蒸馏水
B. 滴定结束时,仰视读数
C.滴定前滴定管尖嘴无气泡,滴定结束有气泡
D.锥形瓶用待测液润洗
E. NaOH标准液保存时间过长,有部分变质
(5)根据表中记录数据,通过计算可得,该盐酸浓度为: ____________mol/L
包头四中2018-2019学年度第一学期第二次月考
高二年级化学参考答案
1.D 2.D 3.B 4.C 5.C
6.B 7.C 8.D 9.B 10.B
11.B 12.A 13.D 14.D 15.B
16.C 17.A 18.C 19.B 20.B
非选择题(每空2分)
21(14分).+46.2 kJ·mol-1 B 0.5MPa > < AC
22(14分).酸 Cu2++2H2O≒Cu(OH)2+2H+ 抑制 Al3++3HCO3-=3CO2↑+Al(OH)3↓ Ag2S CH4 O2+4e-+2H2O=4OH-
23(12分).① 酸式滴定管 锥形瓶内颜色变化 当滴入最后一滴时,溶液由红色变橙色,且半分钟内颜色不变 B D 0.1618