- 2021-08-06 发布 |
- 37.5 KB |
- 26页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
重庆市2021高考化学一轮复习专题二化学物质及其变化第1讲物质的组成分类和性质教案
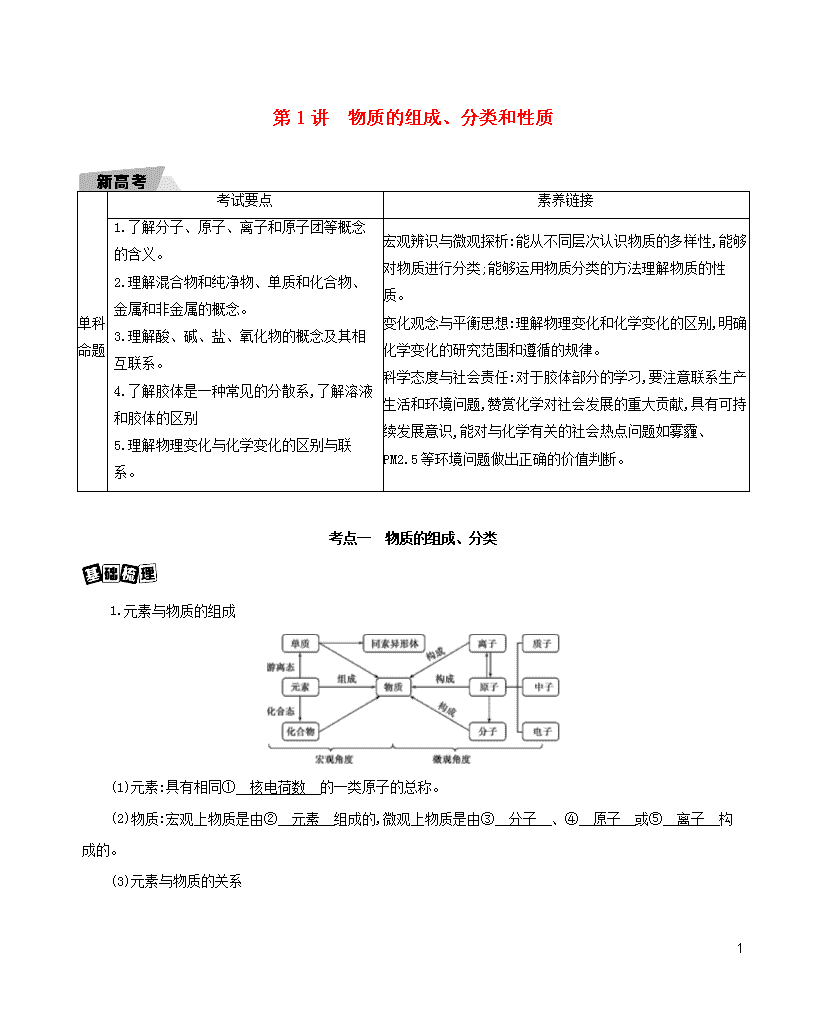
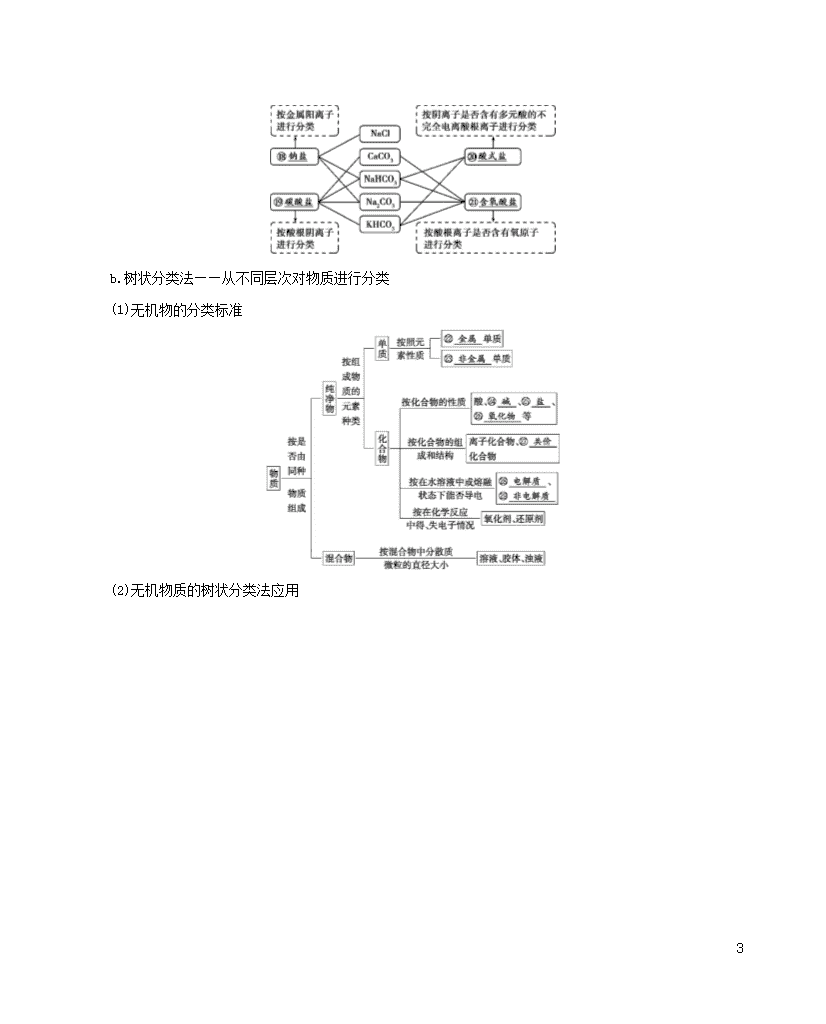
第1讲 物质的组成、分类和性质 单科命题 考试要点 素养链接 1.了解分子、原子、离子和原子团等概念的含义。 2.理解混合物和纯净物、单质和化合物、金属和非金属的概念。 3.理解酸、碱、盐、氧化物的概念及其相互联系。 4.了解胶体是一种常见的分散系,了解溶液和胶体的区别 5.理解物理变化与化学变化的区别与联系。 宏观辨识与微观探析:能从不同层次认识物质的多样性,能够对物质进行分类;能够运用物质分类的方法理解物质的性质。 变化观念与平衡思想:理解物理变化和化学变化的区别,明确化学变化的研究范围和遵循的规律。 科学态度与社会责任:对于胶体部分的学习,要注意联系生产生活和环境问题,赞赏化学对社会发展的重大贡献,具有可持续发展意识,能对与化学有关的社会热点问题如雾霾、PM2.5等环境问题做出正确的价值判断。 考点一 物质的组成、分类 1.元素与物质的组成 (1)元素:具有相同① 核电荷数 的一类原子的总称。 (2)物质:宏观上物质是由② 元素 组成的,微观上物质是由③ 分子 、④ 原子 或⑤ 离子 构成的。 (3)元素与物质的关系 26 元素单质:⑥ 只由一种元素组成 的纯净物化合物:⑦ 由多种元素组成 的纯净物 (4)元素的存在形态 游离态:元素以⑧ 单质 形式存在的状态; 化合态:元素以⑨ 化合物 形式存在的状态。 (5)纯净物和混合物 a.⑩ 纯净 物:由同种单质或化合物组成的物质; b. 混合 物:由几种不同的单质或化合物组成的物质。 (6)同位素和同素异形体 同位素 同素异形体 定义 同种元素形成的不同原子(核素) 同种元素形成的不同单质 特征 质子数相同,中子数不同,质量数不同,同价态时 化学性质 几乎完全相同 互为同素异形体的单质其 化学性质 几乎相同而 物理性质 有很大差异 举例 如 11H、12H、13H;1735Cl、1737Cl等 如O2和O3、金刚石和石墨及C60、白磷和红磷等,同素异形体间的转变为 化学变化 及时提醒 ①由同种元素组成的物质不一定是纯净物。如O2、O3组成的混合气体就是混合物。 ②由不同同位素构成的单质(或化合物)是纯净物,如H2和D2、H2O和D2O,由12C和13C组成的石墨也是纯净物。 ③冰水混合物、结晶水合物(如CuSO4·5H2O)属于纯净物而不是混合物;高分子化合物(如聚乙烯查看更多