- 2021-08-06 发布 |
- 37.5 KB |
- 13页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
河南省驻马店市2020届高三线上模拟测试(二) 化学
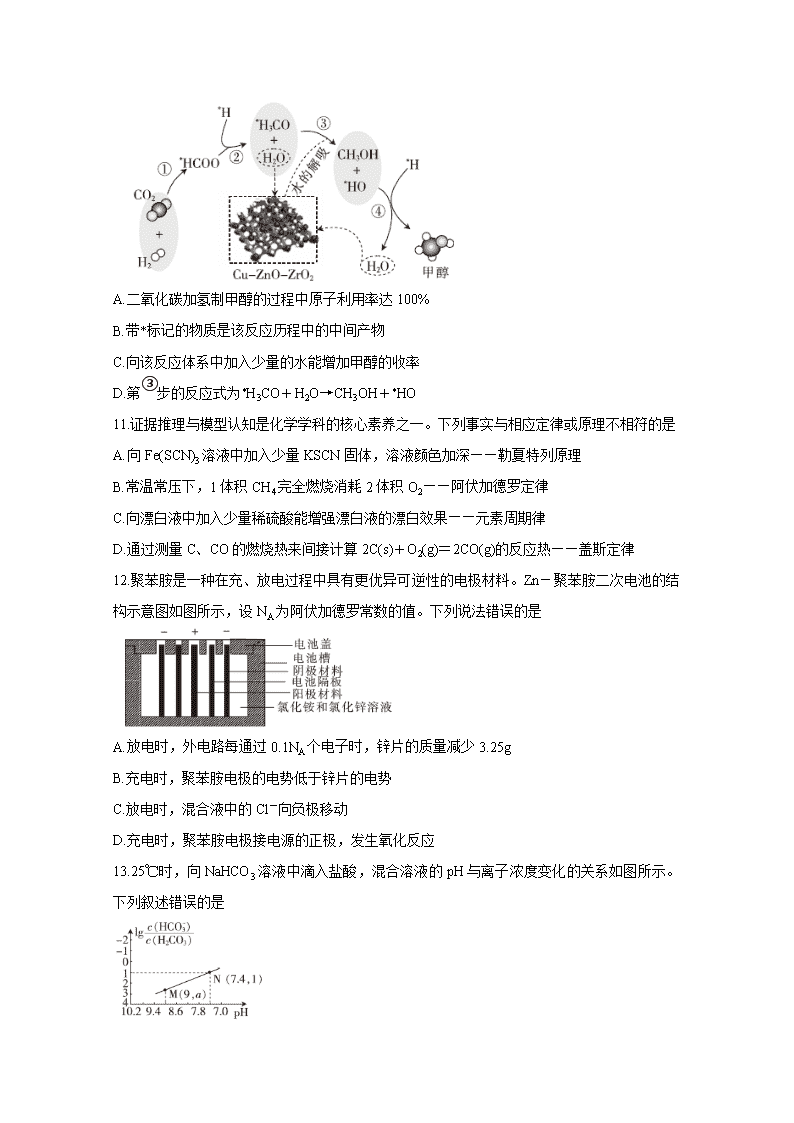
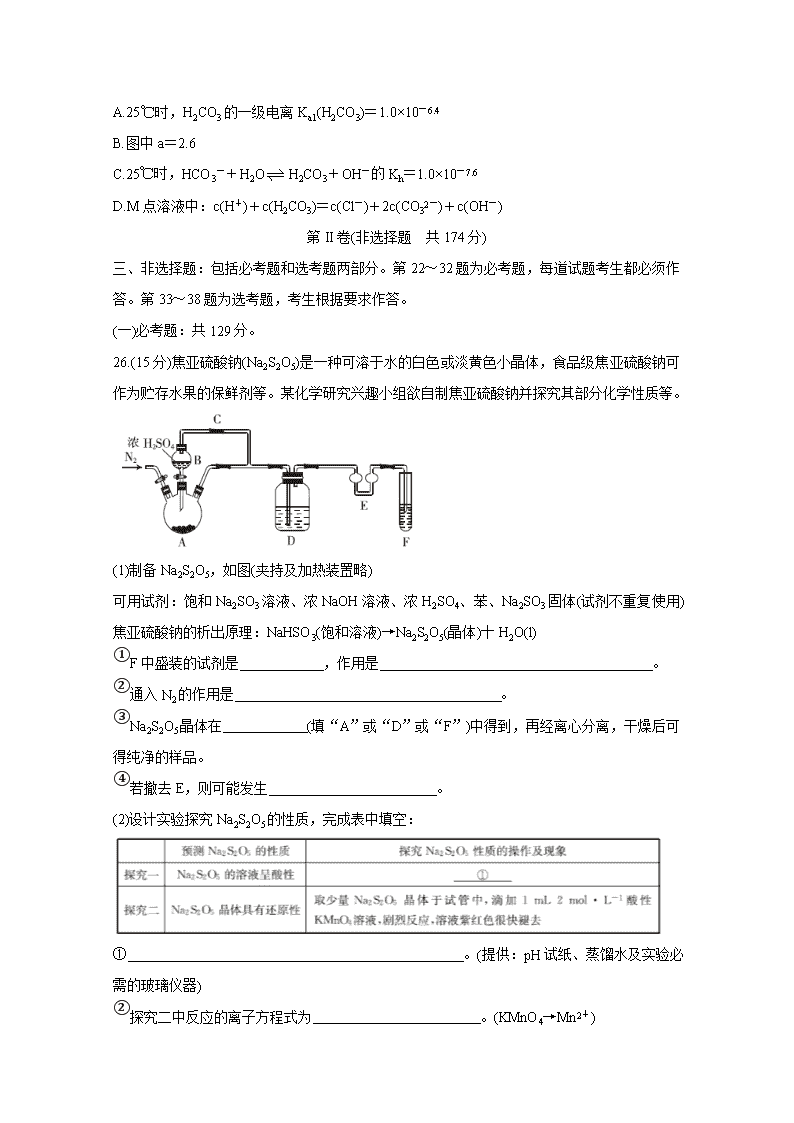
驻马店市高三年级线上模拟测试(二) 化学 第I卷(选择题 共126分) 一、选择题:本题共13小题,每小题6分。在每小题给出的四个选项中,只有一项是符合题目要求的。 7.化学与生活密切相关。下列说法正确的是 A.利用二氧化硅与碳酸钙常温反应制备陶瓷 B.纺织业利用氢氧化钠的强氧化性将其作为漂洗的洗涤剂 C.利用明矾的水溶液除去铜器上的铜锈,因Al3+水解呈酸性 D.“丹砂(主要成分为硫化汞)烧之成水银,积变又还成丹砂”中发生的反应为可逆反应 8.联合国大会宣布2019年为“国际化学元素周期表年”,中国科技馆推出“律动世界——化学元素周期表专题展”。已知短周期元素T的次外层电子数是其最外层电子数的2倍,X、W、Z、Y均与元素T相邻且原子序数依次增大,且X、Y与T同主族,W、Z与T同周期。下列判断错误的是 A.元素T在自然界主要以游离态形式存在 B.元素非金属性强弱:Z>Y C.最高价氧化物对应水化物的酸性:X>W D.X与氧元素形成的氧化物不止一种 9.螺环化合物(环与环之间共用一个碳原子的化合物)M在制造生物检测机器人中有重要作用,其结构简式如图。下列有关该物质的说法正确的是 A.分子式为C6H8O B.所有碳原子处于同一平面 C.是环氧乙烷()的同系物 D.一氯代物有2种(不考虑立体异构) 10.我国科研人员研究了在Cu-ZnO-ZrO2催化剂上CO2加氢制甲醇过程中水的作用机理,其主反应历程如图所示(H2→*H+*H)。下列说法错误的是 A.二氧化碳加氢制甲醇的过程中原子利用率达100% B.带*标记的物质是该反应历程中的中间产物 C.向该反应体系中加入少量的水能增加甲醇的收率 D.第③步的反应式为*H3CO+H2O→CH3OH+*HO 11.证据推理与模型认知是化学学科的核心素养之一。下列事实与相应定律或原理不相符的是 A.向Fe(SCN)3溶液中加入少量KSCN固体,溶液颜色加深——勒夏特列原理 B.常温常压下,1体积CH4完全燃烧消耗2体积O2——阿伏加德罗定律 C.向漂白液中加入少量稀硫酸能增强漂白液的漂白效果——元素周期律 D.通过测量C、CO的燃烧热来间接计算2C(s)+O2(g)=2CO(g)的反应热——盖斯定律 12.聚苯胺是一种在充、放电过程中具有更优异可逆性的电极材料。Zn-聚苯胺二次电池的结构示意图如图所示,设NA为阿伏加德罗常数的值。下列说法错误的是 A.放电时,外电路每通过0.1NA个电子时,锌片的质量减少3.25g B.充电时,聚苯胺电极的电势低于锌片的电势 C.放电时,混合液中的Cl-向负极移动 D.充电时,聚苯胺电极接电源的正极,发生氧化反应 13.25℃时,向NaHCO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是 A.25℃时,H2CO3的一级电离Ka1(H2CO3)=1.0×10-6.4 B.图中a=2.6 C.25℃时,HCO3-+H2OH2CO3+OH-的Kh=1.0×10-7.6 D.M点溶液中:c(H+)+c(H2CO3)=c(Cl-)+2c(CO32-)+c(OH-) 第II卷(非选择题 共174分) 三、非选择题:包括必考题和选考题两部分。第22~32题为必考题,每道试题考生都必须作答。第33~38题为选考题,考生根据要求作答。 (一)必考题:共129分。 26.(15分)焦亚硫酸钠(Na2S2O5)是一种可溶于水的白色或淡黄色小晶体,食品级焦亚硫酸钠可作为贮存水果的保鲜剂等。某化学研究兴趣小组欲自制焦亚硫酸钠并探究其部分化学性质等。 (1)制备Na2S2O5,如图(夹持及加热装置略) 可用试剂:饱和Na2SO3溶液、浓NaOH溶液、浓H2SO4、苯、Na2SO3固体(试剂不重复使用)焦亚硫酸钠的析出原理:NaHSO3(饱和溶液)→Na2S2O5(晶体)十H2O(l) ①F中盛装的试剂是 ,作用是 。 ②通入N2的作用是 。 ③Na2S2O5晶体在 (填“A”或“D”或“F”)中得到,再经离心分离,干燥后可得纯净的样品。 ④若撤去E,则可能发生 。 (2)设计实验探究Na2S2O5的性质,完成表中填空: ① 。(提供:pH试纸、蒸馏水及实验必需的玻璃仪器) ②探究二中反应的离子方程式为 。(KMnO4→Mn2+) (3)利用碘量法可测定Na2S2O5样品中+4价硫的含量。 实验方案:将a g Na2S2O5样品放入碘量瓶(带磨口塞的锥形瓶)中,加入过量c1 mol·L-1的碘溶液,再加入适量的冰醋酸和蒸馏水,充分反应一段时间,加入淀粉溶液, (填实验步骤),当溶液由蓝色恰好变成无色,且半分钟内溶液不恢复原色,则停止滴定操作,重复以上步骤两次,记录数据。(实验中必须使用的试剂有c2 mol·L-1的标准Na2S2O5溶液;已知:2Na2S2O3+I2=Na2S4O6+2NaI) (4)含铬废水中常含有六价铬[Cr(VI)]。利用Na2S2O5和FeSO4·7H2O先后分两个阶段处理含Cr2O72-的废水,先将废水中Cr2O72-全部还原为Cr3+,再将Cr3+全部转化为Cr(OH)3而除去,需调节溶液的pH范围为 。{已知:Kap[Cr(OH)3]=6.4×10-31,1g2≈0.3,c(Cr3+)<1.0×10-5 mol·L-1时视为完全沉淀} 27.(14分)2019年诺贝尔化学奖授予锂离子电池的发明者,LiFePO4是锂离子电池的正极材料。用含锂废渣(主要金属元素的含量:Li 8.50%、Ni 6.55%、Mg 13.24%)制备Li2C2O4,并用其制备LiFePO4。部分工艺流程如下(该流程可能造成水体砷污染): 已知:滤液1、滤液2中部分离子的浓度(g·L-1): I.制备Li2C2O4 (1)滤渣2的主要成分有 (填化学式)。 (2)Na2C2O4溶液中各离子的浓度由大到小顺序为 。 (3)写出加入Na2C2O4溶液时发生反应的离子方程式: 。 II.制备LiFePO4 (4)将电池极Li2C2O4和FePO4置于高温下反应,生成LiFePO4和一种温室气体,该反应的化学方程式是 。 (5)LiFePO4需要在高温下成型后才能作为电极,高温成型时要加入少量石墨,则石墨的作用是 (任写一点)。 (6)我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的As(V),其机制模型如图,其中零价铁与过硫酸钠反应的离子方程式是 。在该模型中得到的铁砷共沉淀物经灼烧(无元素化合价变化)后得到一种磁性化合物,化学式为Fe7As2O14,该物质中二价铁与三价铁的个数比为 。 28.(14分)2019年国际非政府组织“全球碳计划”12月4日发布报告:研究显示,全球二氧化碳排放量增速趋缓。CO2的综合利用是解决温室问题的有效途径。 (1)一种途径是将CO2转化成有机物实现碳循环。如: C2H4(g)+H2O(l)=C2H5OH(l) △H=-44.2 kJ·mol-1 2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) △H2=+1411.0 kJ·mol-1 2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) △H3= (2)CO2甲烷化反应是由法国化学家Paul Sabatier提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程如下: ①上述过程中,产生H2反应的化学方程式为 。 ②HCOOH是CO2转化为CH4的中间体: 。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是 (填“I”或“II”)。 (3)CO2经催化加氢可以生成低碳烃,主要有两个竞争反应: 反应I:CO2(g)+4H2(g)CH4(g)+2H2O(g) 反应II:2CO2(g)十6H2(g)C2H4(g)+4H2O(g) 在1L恒容密闭容器中充入1 mol CO2和4 mol H2,测得平衡时有关物质的物质的量随温度变化如图所示。T1℃时,CO2的转化率为 。T1℃时,反应I的平衡常数K= 。 (4)已知CO2催化加氢合成乙醇的反应原理为2CO2(g)+6H2(g)C2H5OH(g)+3H2O(g) △H。m代表起始时的投料比,即。 ①图1中投料比相同,温度T3>T2>T,则△H (填“>”或“<”)0。 ②m=3时,该反应达到平衡状态后p(总)=20a MPa,恒压条件下各物质的物质的量分数与温度的关系如图2。则曲线b代表的物质为 (填化学式),T4温度时,反应达到平衡时物质d的分压p(d)= 。 (二)选考题:共45分。请考生从给出的2道物理题、2道化学题、2道生物题中每科任选一题作答。如果多答,则每科按所答的第一题计分。 35.[化学——物质结构与性质](15分) 国家航天局计划2020年实施火星探测任务。据了解火星上存在大量的含氮化合物,科学家推测火星生命可能主要以氮、碳、硅、铜为基体构成。 (1)邻氨基吡啶()的铜配合物在有机不对称合成中起催化诱导效应。 ①邻氨基吡啶中所有元素的电负性由小到大的顺序为 (填元素符号)。设NA为阿伏加德罗常数的值,1 mol中含有σ键的数目为 。 ②一定条件下-NH2可以被氧化成-NO2,-NO2中N原子的杂化方式为 杂化。 (2)第四周期的某主族元素,其第一至第五电离能数据如图1所示, 则该元素的基态原子电子排布式为 。 (3)元素周期表中的第IVA族~第VIIA族中部分元素的最简单氢化物的沸点变化趋势线如图2,其中一个小黑点代表一种氢化物,则趋势线a代表第 族元素的最简单氢化物的沸点变化趋势,判断依据是 。 (4)干冰是常见的分子晶体,而CO2在高温高压下能形成另一种晶体其晶胞如图3所示,该CO2晶体的熔点 (填“>”“<”或“=”)SiO2晶体的熔点。 (5)一种嘌呤和一种吡啶的结构如图4。 ①嘌呤中轨道之间的夹角∠1比∠2大,原因是 。 ②分子中的大π键可以用符号表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡啶中的大π键可表示为 。 (6)火星岩石中存在大量的氮化镓,氮化镓为六方晶胞,结构如图5所示。 若该晶体密度为d g·cm-3,晶胞参数a=b≠c(单位:nm),a、b夹角为120°,阿伏加德罗常数的值为NA,则晶胞参数c= (写出代数式)nm。 36.[化学——有机化学基础](15分) 佛罗那可用于治疗新生儿高胆红素血症。以甲苯为原料制备佛罗那的合成路线如下: 回答下列问题: (1)D的名称是 ,B中官能团的名称为 。 (2)写出H的结构简式: 。 (3)结构中不含碳碳双键,有六个碳原子在同一条直线上的B的同分异构体的结构简式有 种(不考虑立体异构),写出其中一种结构的结构简式: 。 (4)上述合成路线中有字母代号的物质中有手性碳原子的是 (填字母代号)。(已知:连有四个不同的原子或原子团的碳原子称为手性碳原子) (5)H→佛罗那的反应类型为 。 (6)写出F→G的化学方程式: 。 (7)参照上述合成路线,设计以丙二酸、乙醇和氯乙烷为原料合成乙基丙二酸的合成路线(无机试剂任选)。 答案查看更多