高中化学第三章晶体结构与性质2-2原子晶体同步检测含解析 人教版选修3
第2课时 原子晶体
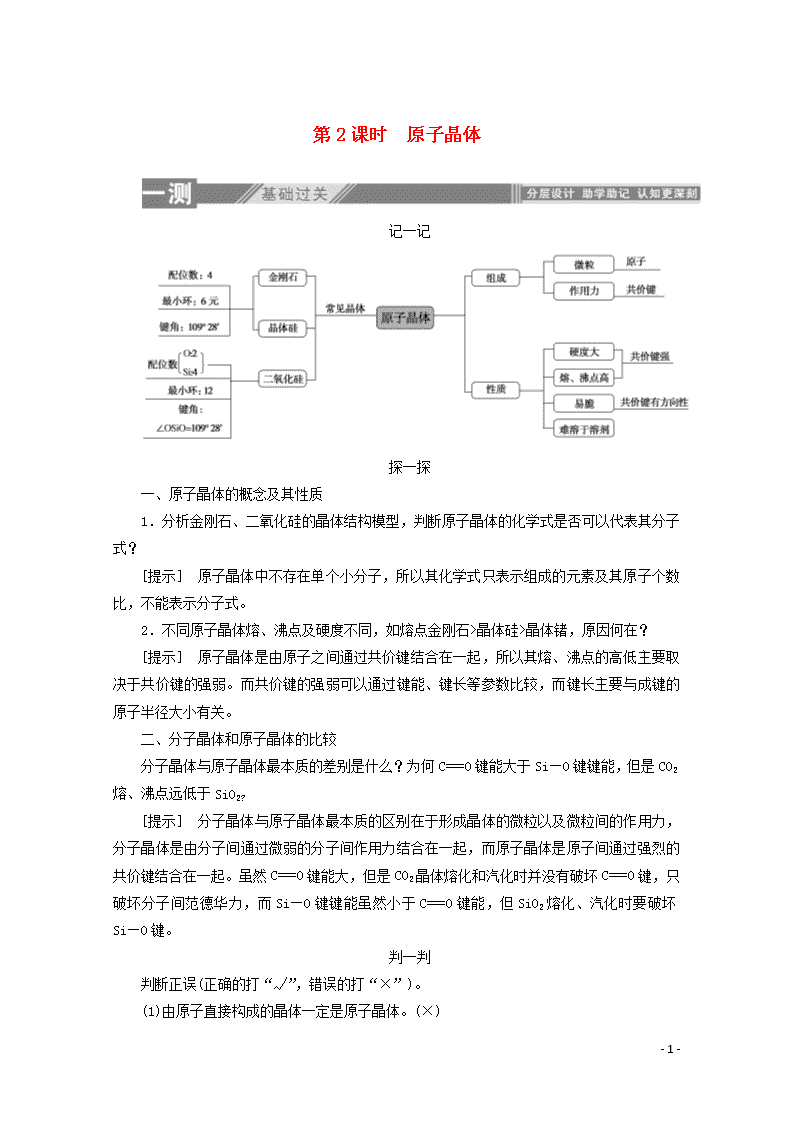
记一记
探一探
一、原子晶体的概念及其性质
1.分析金刚石、二氧化硅的晶体结构模型,判断原子晶体的化学式是否可以代表其分子式?
[提示] 原子晶体中不存在单个小分子,所以其化学式只表示组成的元素及其原子个数比,不能表示分子式。
2.不同原子晶体熔、沸点及硬度不同,如熔点金刚石>晶体硅>晶体锗,原因何在?
[提示] 原子晶体是由原子之间通过共价键结合在一起,所以其熔、沸点的高低主要取决于共价键的强弱。而共价键的强弱可以通过键能、键长等参数比较,而键长主要与成键的原子半径大小有关。
二、分子晶体和原子晶体的比较
分子晶体与原子晶体最本质的差别是什么?为何C===O键能大于Si—O键键能,但是CO2熔、沸点远低于SiO2?
[提示] 分子晶体与原子晶体最本质的区别在于形成晶体的微粒以及微粒间的作用力,分子晶体是由分子间通过微弱的分子间作用力结合在一起,而原子晶体是原子间通过强烈的共价键结合在一起。虽然C===O键能大,但是CO2晶体熔化和汽化时并没有破坏C===O键,只破坏分子间范德华力,而Si—O键键能虽然小于C===O键能,但SiO2熔化、汽化时要破坏Si—O键。
判一判
判断正误(正确的打“√”,错误的打“×”)。
(1)由原子直接构成的晶体一定是原子晶体。(×)
- 14 -
(2)具有共价键的晶体一定是原子晶体。(×)
(3)原子晶体在固态或熔化时都一定不导电。(×)
(4)原子晶体由于硬度及熔、沸点都较高,故常温时不与其他物质反应。(×)
(5)SO2与SiO2的化学键类型相同,晶体类型也相同。(×)
(6)1 mol晶体硅中含 4 mol Si—Si键。(×)
(7)60 g SiO2 晶体中含4 mol Si—O键。(√)
(8)原子晶体中不存在分子,所以SiO2 只表示原子个数比。(√)
(9)以二氧化硅为主要成分的水晶和玛瑙均为原子晶体。(×)
(10)原子晶体中每个原子周围尽可能结合更多的原子,大多数为12个。(×)
练一练
1.下列关于原子晶体的说法不正确的是( )
A.原子晶体中的成键微粒是原子
B.原子晶体中原子之间全部以共价键结合
C.原子晶体均是化合物
D.原子晶体的熔、沸点都比较高
解析:原子晶体可能是单质,如金刚石、晶体硅,也可能是化合物,如二氧化硅、碳化硅等。
答案:C
2.下列物质的晶体直接由原子构成的一组是( )
①CO2 ②SiO2 ③晶体Si ④白磷 ⑤氨基乙酸 ⑥固态He
A.①②③④⑤⑥ B.②③④⑥ C.②③⑥ D.①②⑤⑥
解析:CO2、白磷、氨基乙酸、固态He是分子晶体,其晶体由分子构成,稀有气体He由单原子分子构成;SiO2、晶体Si属于原子晶体,其晶体直接由原子构成。
答案:C
3.下列关于SiO2晶体网状结构的叙述中正确的是( )
A.最小的环上,有3个硅原子和3个氧原子
B.每个硅原子与2个氧原子成键
C.最小的环上,有6个硅原子和6个氧原子
D.存在四面体结构单元,O原子处于中心,Si原子处于4个顶角
解析:SiO2晶体中,每个硅原子与4个氧原子成键、每个氧原子与2个硅原子成键,晶体中的硅氧四面体中Si原子处于中心、O原子处于4个顶角。最小的环是十二元环,环上有6个Si原子、6个O原子,Si、O原子数之比是1:1。
答案:C
- 14 -
4.下列各组晶体物质中,化学键类型相同,晶体类型也相同的是( )
①SiO2和SO3 ②金刚石和白磷 ③CO2和SO2
④晶体硅和金刚石 ⑤晶体氖和晶体氮 ⑥硫黄和单质碘
A.①②③ B.④⑤⑥
C.③④⑥ D.①③⑤
解析:属于分子晶体的有SO3、CO2、SO2、白磷、晶体氖、晶体氮、硫黄和单质碘。属于原子晶体的有SiO2、晶体硅和金刚石。但晶体氖是由稀有气体分子构成,晶体中不存在化学键。
答案:C
知识点一 原子晶体的概念及其性质
1.下列有关原子晶体的叙述错误的是( )
A.原子晶体中,原子不遵循紧密堆积原则
B.原子晶体具有空间网状结构
C.原子晶体中不存在独立的分子
D.原子晶体熔化时不破坏共价键
解析:原子晶体中原子之间通过共价键相连,而共价键具有方向性和饱和性,所以原子晶体中,原子不遵循紧密堆积原则;原子晶体是相邻原子之间通过共价键结合而成的空间网状结构,不存在独立的分子,熔化时需要破坏共价键。
答案:D
2.根据下列性质判断,属于原子晶体的是( )
A.熔点2 700 ℃,导电性好,延展性好
B.无色晶体,熔点3 550 ℃,不导电,质硬,难溶于水和有机溶剂
C.无色晶体,能溶于水,质硬而脆,熔点为800 ℃,熔化时能导电
D.熔点-56.6 ℃,微溶于水,硬度小,固态或液态时不导电
解析:A项,延展性好不是原子晶体的性质,原子晶体中原子与原子之间以共价键结合,而共价键有一定的方向性,使原子晶体质硬而脆;B项,属于原子晶体的性质;C项,应该属于离子化合物;D项,符合分子晶体的特征。
答案:B
知识点二 分子晶体和原子晶体的比较
- 14 -
3.组成干冰和二氧化硅晶体的化合物均属于第ⅣA族元素的最高价氧化物,但它们的熔、沸点差别很大,原因是( )
A.二氧化硅的相对分子质量大于二氧化碳的相对分子质量
B.C===O键键能比Si—O键键能小
C.干冰为分子晶体,二氧化硅为原子晶体
D.干冰易升华,二氧化硅不能
解析:组成干冰和二氧化硅晶体的化合物虽然均属于第ⅣA族元素的最高价氧化物,但干冰是分子晶体,二氧化硅为原子晶体,干冰的熔、沸点取决于其分子间作用力的大小,而二氧化硅的熔、沸点则由硅氧共价键的强度决定。
答案:C
4.下列说法错误的是( )
A.干冰晶体中每个分子周围最近的分子有12个,而二氧化硅晶体中,每个硅原子周围只有4个氧原子
B.C2H5OH与C2H5Br相比,前者的相对分子质量小于后者,而沸点却高于后者,其原因是前者的分子间存在氢键
C.非金属单质只能形成分子晶体
D.金刚石熔化时断裂共价键
解析:干冰晶体采用分子密堆积,每个分子周围最近的分子有12个,而共价键有饱和性和方向性,所以二氧化硅晶体中,每个硅原子周围只有4个氧原子A项正确;乙醇的分子间易形成氢键,故其沸点高于C2H5Br,B项正确;C项Si、O是非金属元素,但金刚石、晶体硅、二氧化硅都是原子晶体,C项不正确;干冰熔化时破坏范德华力,二氧化硅、金刚石等原子晶体熔化时破坏共价键,D项正确。
答案:C
综合考查
5.下列有关物质的熔点高低顺序正确的是( )
A.HF
SiO2
D.H2O>H2S,SO2C—Si>Si—Si共价键键长越短,键能越大,则原子晶体的熔点越高。所以三者的熔点由高到低的顺序是金刚石>碳化硅>晶体硅。
答案:D
- 14 -
6.如图所示是某原子晶体A的空间结构片断,A与某物质B反应生成C,其实质是在每个A—A键中插入一个B原子,则C物质的化学式为( )
A.AB B.A5B4
C.AB2 D.A2B5
解析:由图可知,每个A原子形成4个键,每个A—A键中插入一个B原子,每个B原子形成2个键,故C物质中每个A原子形成4个A—B键,每个B原子形成2个B—A键,则A、B原子个数比为1:2,所以其化学式是AB2。
答案:C
7.设NA为阿伏加德罗常数的值。下列说法中正确的是( )
A.28 g 晶体硅中含有Si—Si键的个数为2NA
B.124 g白磷(P4)晶体中含有P—P键的个数为4NA
C.12 g金刚石中含有C—C键的个数为4NA
D.SiO2晶体中每摩尔硅原子可与氧原子形成2NA个共价键(Si—O键)
解析:晶体硅的结构与金刚石相似,每个硅原子与周围4个原子形成4个共价键,依据“均摊法”,1个硅(或碳)原子分得的共价键数为4×=2,A项正确,C项错误;白磷为正四面体结构,每个P4分子中含有6个P—P键,B项错误;SiO2晶体中每个硅原子与周围4个氧原子形成4个Si—O键,D项错误。
答案:A
8.C和Si元素在化学中占有极其重要的地位。
(1)SiC的晶体结构与晶体硅的相似,其中C原子的杂化
方式为________,微粒间存在的作用力是____________________________。SiC和晶体Si的熔、沸点高低顺序是__________________。
(2)C、Si为同一主族的元素,CO2和SiO2的化学式相似,但结构和性质有很大的不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成π键,而Si、O原子间不能形成π键:__________________________________,SiO2属于________晶体,CO2属于________晶体,所以熔点CO2________SiO2(填“<”、“=”或“>”)。
- 14 -
(3)金刚石、晶体硅、二氧化硅、CO2四种晶体的构成微粒分别是______________________________________,熔化时克服的微粒间的作用力分别是________________________________。
解析:(1)晶体硅中一个硅原子周围与4个硅原子相连,呈正四面体结构,所以杂化方式是sp3,因为Si—C的键长小于Si—Si的键长,所以熔、沸点碳化硅>晶体硅。
(2)SiO2为原子晶体,CO2为分子晶体,所以熔点SiO2>CO2。
(3)金刚石、晶体硅、二氧化硅均为原子晶体,构成微粒为原子,熔化时破坏共价键;CO2为分子晶体,由分子构成,CO2分子间以分子间作用力结合。
答案:
(1)sp3 共价键 SiC>Si
(2)Si的原子半径较大,Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,不能形成上述稳定的π键 原子 分子 <
(3)原子、原子、原子、分子 共价键、共价键、共价键、分子间作用力
基础达标
1.下列晶体熔化时,必须破坏非极性共价键的是( )
A.冰 B.晶体硅
C.溴 D.二氧化硅
解析:冰、溴为分子晶体,熔化时克服的是分子间作用力,A、C项错误;晶体硅、二氧化硅为原子晶体,二氧化硅熔化时,破坏的是Si—O极性键,晶体硅熔化时,破坏的是Si—Si非极性键,B项正确,D项错误。
答案:B
2.碳化锗GeC的一种具有类似金刚石结构的晶体,其中C原子和Ge原子的位置是交替的。在下列三种晶体①金刚石、②晶体锗、③碳化锗中,它们的熔点从高到低的顺序是( )
A.①③② B.②③①
C.③①② D.②①③
解析:C与Ge同为第ⅣA族元素,它们的相似性表现在金刚石是原子晶体,晶体锗、碳化锗也是原子晶体。从碳到锗原子半径逐渐增大,形成共价键的键能逐渐减弱,熔点决定于它们的键能,故熔点从高到低的顺序是金刚石、碳化锗、晶体锗。
答案:A
3.在化学上,常用一条短线表示一个化学键,如图所示的有关结构中,有直线(包括虚线)不表示化学键或分子间作用力的是( )
- 14 -
A.石墨的结构
B.白磷的结构
C.CCl4的结构
D.立方烷(C8H8)的结构
解析:石墨晶体中同一层内原子以共价键结合,而层与层之间为范德华力,所以物质结构中实线表示化学键,虚线表示分子间作用力(范德华力),故A项不选;白磷分子中,每个P原子形成3个共价键,达稳定结构,所以物质结构中线表示化学键,故B项不选;在CCl4中,Cl原子之间的直线只是为了表示四个Cl原子形成的正四面体而已,不表示化学键,只有C-Cl间的线表示化学键,故C项选;立方烷中碳原子之间形成共价键,所以物质结构中线表示化学键,故D项不选 。
答案:C
4.氮化铝(AlN)是一种熔点很高、硬度大、固态和熔融态均不导电、难溶于水和其他溶剂的晶体,将下列各组物质加热熔化或汽化,所克服微粒间作用力与AlN相同的是( )
A.水晶、金刚石 B.食盐、硫酸钾 C.碘、硫 D.硅、干冰
解析:氮化铝(AlN)是一种熔点很高、硬度大、不导电、难溶于水和其他溶剂的晶体,说明属于原子晶体,据此解答。水晶、金刚石都是原子晶体,熔化克服共价键,故A项正确;食盐、硫酸钾都是离子晶体,熔化克服离子键,故B项错误;碘、硫都是分子晶体,熔化克服的是分子间作用力,故C项错误;硅是原子晶体,熔化克服的是共价键;干冰是分子晶体,熔化克服的是分子间作用力,故D项错误。
答案:A
5.下列叙述中,结论(事实)和对应的解释(事实)均不正确的是( )
A.金刚石的熔、沸点高于晶体硅,因为C—C键的键能大于Si—Si键的键能
B.二氧化硅晶体中不存在SiO2分子,因为它含有硅氧四面体的空间网状结构
C.稀有气体的晶体属于原子晶体,因为其组成微粒是原子,不存在分子间作用力
D.立体构型为正四面体结构的分子中,化学键的键角不一定是109°28′,有可能为60°
解析:稀有气体的晶体属于分子晶体,存在分子间作用力,不存在共价键,C项符合题意。
答案:C
6.将SiCl4与过量的液氨反应可生成化合物Si(NH2)4。将该化合物在无氧条件下高温灼烧,可得到氮化硅(Si3N4)固体,氮化硅是一种新型耐高温、耐磨材料,在工业上有广泛的应用。下列推断可能正确的是( )
A.SiCl4、Si3N4的晶体类型相同
B.Si3N4晶体是立体网状结构
C.原子晶体C3N4的熔点比Si3N4的低
- 14 -
D.SiCl4晶体在熔化过程中化学键断裂
解析:SiCl4是分子晶体,在熔化过程中克服的是分子间作用力,化学键不断裂。Si3N4是原子晶体,其晶体为立体网状结构。根据C、Si的原子半径推知C—N键的键能比Si—N键的键能大,故C3N4的熔点比Si3N4的高。
答案:B
7.根据量子力学计算,氮化碳结构有五种,其中一种β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示。下列有关氮化碳的说法不正确的是( )
A.该晶体中的碳、氮原子核外都满足8电子稳定结构
B.氮化碳中碳显+4价,氮显-3价
C.每个碳原子与四个氮原子相连,每个氮原子和三个碳原子相连
D.氮化碳的分子式为C3N4
解析:根据图中结构可知,每个碳原子周围有四个共价键,每个氮原子周围有三个共价键,碳原子最外层有4个电子,形成四个共价健后成8电子稳定结构,氮原子最外层有5个电子,形成三个共价键后,也是8电子稳定结构,A项正确;由于元素的非金属性N>C,所以形成共价键时,共用电子对偏向N,偏离C,所以氮化碳中碳显+4价,氮显-3价,B项正确;根据晶体结构可知每个碳原子与四个氮原子相连,每个氮原子和三个碳原子相连,C项正确;由于氮化碳是原子晶体,不存在分子,因此没有分子式,D项错误。
答案:D
8.美国 lawrece liremore 国家实验室的V·Lota·C·S·You和H·Cynn成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体的说法正确的是( )
A.CO2的原子晶体和分子晶体互为同分异构体
B.在一定的条件下,转化为分子晶体是物理变化
C.CO2的原子晶体和分子晶体具有相同的物理性质和化学性质
D.一定条件下,该晶体可能会与氢氧化钠反应
解析:二氧化碳原子晶体的化学式是原子个数比,不是分子组成,分子晶体是分子式表示分子组成,二者不具有相同的分子式,不属于同分异构体,A项错误;二氧化碳分子晶体和二氧化碳原子晶体的构成微粒不同,空间构型不同,所以其物理性质不同。二氧化碳原子晶体和二氧化碳分子晶体属于不同物质,所以在一定条件下,CO2
- 14 -
原子晶体转化为分子晶体是化学变化不是物理变化,即二者之间的转化是化学变化,选项B、选项C错误;类比二氧化硅能与氢氧化钠反应,该CO2原子晶体可能会与氢氧化钠反应,D项正确。
答案:D
9.下列事实与化学键或氢键的方向性无关的是( )
A.冰的密度比水小
B.金刚石虽然很硬,但是易碎
C.S和H形成的化合物分子组成为H2S而不是H3S
D.固态氨不能采用分子密堆积
解析:冰的密度比水小是因为冰晶体中存在氢键,而氢键有方向性,A项正确;金刚石没有延展性,是因为共价键有方向性,B项正确;S和H形成的化合物分子组成为H2S而不是H3S,是因为共价键有饱和性,C项错误;固态氨不能采用分子密堆积是因为氨气分子间能形成氢键,而氢键有方向性,D项正确。
答案:C
10.氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。关于这两种晶体的说法,正确的是( )
A.立方相氮化硼含配位键B→N
B.六方相氮化硼层间作用力小,所以质地软,熔点低
C.两种氮化硼中的硼原子都是采用sp2杂化
D.六方相氮化硼晶体其结构与石墨相似却不导电,原因是没有可以自由移动的电子
解析:B原子最外层有3个电子,存在一个空轨道,N原子最外层有5个电子,存在一个孤电子对,由晶体结构可知,立方相氮化硼为空间网状结构与金刚石类似,立方相氮化硼中B形成4个共价键,其中1个为B←N配位键,故A项错误;六方相氮化硼具有层状结构,层间作用力小,所以质地软,但层内原子间通过共价键结合,导致熔点很高,故B项错误;立方相氮化硼中硼原子形成4个共价键,所以立方相氮化硼中硼原子采用的是sp3杂化,故C项错误;晶体中存在可以自由移动的电子能导电,六方相氮化硼晶体中没有可以自由移动的电子,所以不导电,故D项正确。
- 14 -
答案:D
11.有下列几种晶体:A.无色水晶,B.冰醋酸,C.白磷,D.金刚石,E.晶体氩,F.干冰。
(1)属于分子晶体的是________(填序号,下同)。
(2)属于原子晶体的化合物是________。
(3)直接由原子构成的晶体是________。
(4)受热熔化时化学键不发生变化的晶体是________,受热熔化时需克服共价键的晶体是________。
(5)晶体中存在氢键的是________。
(6)晶体中不存在化学键的是________。
解析:本题解题的关键是弄清分子晶体与原子晶体的区别。根据构成晶体的微粒不同,可知分子晶体仅由分子构成,原子晶体中无分子。属于分子晶体的有B、C、E、F,晶体氩是单原子分子,晶体中无化学键;属于原子晶体的有A、D,但化合物只有A;分子晶体熔化时,一般不破坏化学键;原子晶体熔化时,破坏化学键;CH3COOH分子中存在—OH,分子间能形成氢键。
答案:(1)B、C、E、F (2)A (3)A、D、E (4)B、C、F A、D (5)B (6)E
12.氮化硅是化工行业已合成的一种硬度很大的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:
(1)氮化硅的化学式可能是________。晶体中N和Si的杂化方式分别为________。
(2)氮化硅的晶体类型为________,该晶体中存在的作用力是________。氮化硅硬度大于单质硅,原因为
________________________________________________________________________。
(3)氮化硅可能具有的性质或特点有________。
①硬度大 ②熔点高 ③可以导电 ④不存在单个分子 ⑤具有空间网状结构
解析:
(1)因为N和Si分别要形成3个与4个共价键,所以氮化碳的化学式为Si3N4;二者的价层电子对数均为4,所以均采取sp3杂化。
(2)因为氮化硅的硬度极大,所以它属于原子晶体,晶体中存在的作用力是共价键,由于N原子半径比Si小,所以键长短键能大,硬度大;
(3)Si3N4为原子晶体,其性质为硬度大熔点高,又因它是由原子以共价键形成的晶体,所以不存在单个分子,且为空间网状结构。选①②④⑤。
答案:(1)Si3N4 sp3杂化 (2)原子晶体 共价键 N原子半径小于Si,所以N— Si 键长比Si—Si键长短,键能大 (3)①②④⑤
13.硅是一种重要的非金属单质,硅及其化合物的用途非常广泛。根据所学知识回答硅及其化合物的相关问题。
- 14 -
(1)基态硅原子的核外电子排布式为________。
(2)晶体硅的微观结构与金刚石相似,晶体硅中Si—Si键之间的夹角大小约为________。
(3)请在框图中补充完成SiO2晶体的结构示意图(部分原子已画出),并进行必要的标注。
(4)下表列出有三种物质(晶体)的熔点。
物质
SiO2
SiCl4
SiF4
熔点/℃
1 710
-70.5
-90.2
简要解释熔点产生差异的原因:
①SiO2和SiCl4:
________________________________________________________________________;
②SiCl4和SiF4:
________________________________________________________________________。
解析:(2)晶体硅以一个硅原子为中心,与另外4个硅原子形成正四面体结构,所以Si—Si键之间的夹角大小约为109°28′。(3)图中给出的是硅晶体的结构,SiO2晶体相当于在硅晶体结构中的每个Si—Si键中插入一个氧原子,所以只要在每两个硅原子之间画一个半径比硅原子小的原子,再用实线连起来即可。(4)晶体类型不同,其熔点具有很大的差别,一般原子晶体的熔点高,而分子晶体的熔点低。
答案:
(1)1s22s22p63s23p2
(2)109°28′
(3)如图所示:
(4)①SiO2是原子晶体,微粒间作用力为共价键。SiCl4是分子晶体,微粒间作用力为范德华力,故SiO2熔点高于SiCl4 ②SiCl4和SiF4均为分子晶体,微粒间作用力为范德华力,结构相似时相对分子质量越大,范德华力越大,故SiCl4熔点高于SiF4
14.C60、金刚石和石墨的结构模型如图所示(石墨仅表示出其中的一层结构)。
- 14 -
(1)C60、金刚石和石墨三者互为________。
A.同分异构体 B.同素异形体
C.同系物 D.同位素
(2)固态时,C60属于________(填“原子”或“分子”)晶体,其熔点比金刚石________(填“高”或“低”)。
(3)硅晶体的结构跟金刚石相似,1 mol硅晶体中含有Si—Si键的数目约是________NA。二氧化硅的结构相当于在硅晶体结构中每个Si—Si键之间插入1个氧原子。二氧化硅的空间网状结构中,硅、氧原子形成的最小环上氧原子数目是________。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是________。
解析:(1)C60、金刚石、石墨为碳元素的三种单质,互为同素异形体。
(2)构成C60晶体的粒子是C60分子,所以它属于分子晶体,熔点比金刚石(为原子晶体)低。
(3)每个硅原子形成4个Si—Si键,同时每个Si—Si键为两个原子所共有,所以1 mol硅晶体中含有2 mol Si—Si键。在晶体硅的最小环上有6个Si—Si键(6条边),分别插入一个氧原子,则变成十二元环,有6个氧原子。
(4)石墨晶体中每个碳原子与另外3个碳原子成键,所以每个六边形占有的碳原子个数为6×=2。
答案:(1)B (2)分子 低 (3)2 6 (4)2
能力达标
15.2017年,中外科学家团队共同合成T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代形成碳的一种新型三维立方晶体结构,如图。下列说法错误的是( )
A.每个T-碳晶胞中含32个碳原子
B.T-碳中碳与碳的最小夹角为109.5°
C.T-碳属于原子晶体
- 14 -
D.如图是T-碳晶胞的俯视图
解析:一个金刚石晶胞中,含有C的数目为8×1/8+6×1/2+4=8,将每个C原子换成四面体结构的C,则T-碳晶胞中含有碳原子数目为8×4=32个,故A正确;4个碳原子组成的正四面体结构单元,T-碳中碳与碳的最小夹角为60°,故B错误;C原子间以共价键结合成空间网状结构,T-碳属于原子晶体,故C正确;T-碳晶胞的俯视图正确,突出了四面体结构,及四面体之间碳与碳的共价键,故D正确。
答案:B
16.锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]________,有________个未成对电子。
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因________。
GeCl4
GeBr4
GeI4
熔点/℃
-49.5
26
146
沸点/℃
83.1
186
约400
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为________,微粒之间存在的作用力是________。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(1/2,0,1/2);C为(1/2,1/2,0)。则D原子的坐标参数为________;
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a pm,其密度为________g·cm-3(列出计算式即可)。
解析:(1)在元素周期表中,锗和硅属于同主族,锗位于硅的下一周期,即锗的原子序数为14+18=32,基态原子核外电子排布式为[Ar] 3d104s24p2
- 14 -
;由于4p能级有3个能量相同的轨道,根据洪特规则,4p上2个电子分别占据两个轨道且自旋方向相同,因此未成对电子为2;
(2)根据表格数据得出,三种锗卤化物都是分子晶体,不含分子间氢键,因此熔沸点随着相对分子质量的增大,范德华力增大,熔沸点升高;
(3)锌、锗位于同周期,同一周期从左向右元素的电负性逐渐增大,而氧位于元素周期表右上角,电负性仅次于F,得出三种元素的电负性大小顺序是氧>锗>锌;
(4)类比金刚石,晶体锗属于原子晶体,每个锗与其周围的4个锗原子形成4个单键,锗原子的杂化类型为sp3,微粒间的作用力是共价键;
(5)①对照晶胞图示,坐标系以及A、B、C点坐标,选A点为参照点,观察D点在晶胞中位置,即体对角线的,D的坐标参数为;
②类似金刚石晶胞,1个晶胞含有8个锗原子,即晶胞的质量为g,晶胞的体积为(a×10-10)3cm3,即晶胞的密度为 g/cm3。
答案:(1)3d104s24p2 2 (2)相对分子质量的增大,范德华力增大,熔沸点升高 (3)氧>锗>锌 (4)sp3 共价键 (5)① ②
- 14 -