【化学】湖南省娄底一中2019-2020学年高一下学期第一次月考试题
湖南省娄底一中2019-2020学年高一下学期第一次月考试题
时间:90分钟 满分:100分
H 1 O 16 Na 23 Mg 24 Al 27
一、 选择题(每小题只有一个正确答案,共22小题,每小题2分,共44分)
1、联合国大会确定2019年是“国际化学元素周期表年”。下列说法错误的是( )
A. 短周期共有18种元素
B. 元素周期表中有118种元素,即发现了118种原子
C. 在元素周期表金属与非金属的分界处可以找到半导体材料
D. 元素周期表中的每个周期都是按原子序数递增的顺序从左到右进行排列的
2. 试判断115号元素在元素周期表中的位置是( )。
A.第七周期第IIIA族 B.第七周期第VA族
C.第五周期第VIIA族 D.第五周期第IIIA族
3. 下列反应既是氧化还原反应,又是放热反应的是( )。
A. Ba(OH)2·8H2O与NH4Cl的反应 B. 灼热的炭与CO2的反应
C.铝片与稀硫酸的反应 D.红热的焦炭与水蒸气的反应
4.下列电子式或用电子式表示化合物形成过程正确的是( )
A. NH4Cl的电子式: B. 次氯酸的电子式
C. D.
5. 下列分子中所有原子都满足最外层为8电子结构的是( )
A.CO2 B.H2O C.PCl5 D.NH3
6、下列说法中不正确的是( )
A. 熔化状态下能导电的化合物一定是离子化合物
B. 双原子分子中不一定含有极性键
C. 由非金属元素组成的化合物不一定是共价化合物
D. 不同元素组成的多原子分子内一定不存在非极性键
7、下列关于物质性质的比较,不正确的是( )
A. 沸点:HF﹥HCl﹥HBr﹥HI B. 离子半径大小: Al3+
W>Y>Z B.还原性:
C.质子数: D.离子半径:
10、下列变化中,不需要破坏化学键的是( )
A. 氯化氢溶于水 B. 加热氯酸钾使其分解
C. 干冰气化 D. 氯化钠熔化
11、应用元素周期律的有关知识,可以预测我们不熟悉的一些元素的单质及其化合物的性质。下列预测中正确的是( )
①第2周期非金属元素的气态氢化物溶于水后,水溶液均为酸性 ②砹(At)单质为有色固体,AgAt不溶于水③Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱 ④硫酸锶(SrSO4)是难溶于水的白色固体⑤硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
A.②④ B.①②③④ C.①③⑤ D.②④⑤
12、已知反应A+B= C+D的能量变化如下图所示,下列说法正确的是( )
A. 该反应是放热反应
B. 只有在加热条件下才能进行
C. 反应物的总能量高于生成物的总能量
D. 反应中断开化学键吸收的总能量高于形成化学键放出的总能量
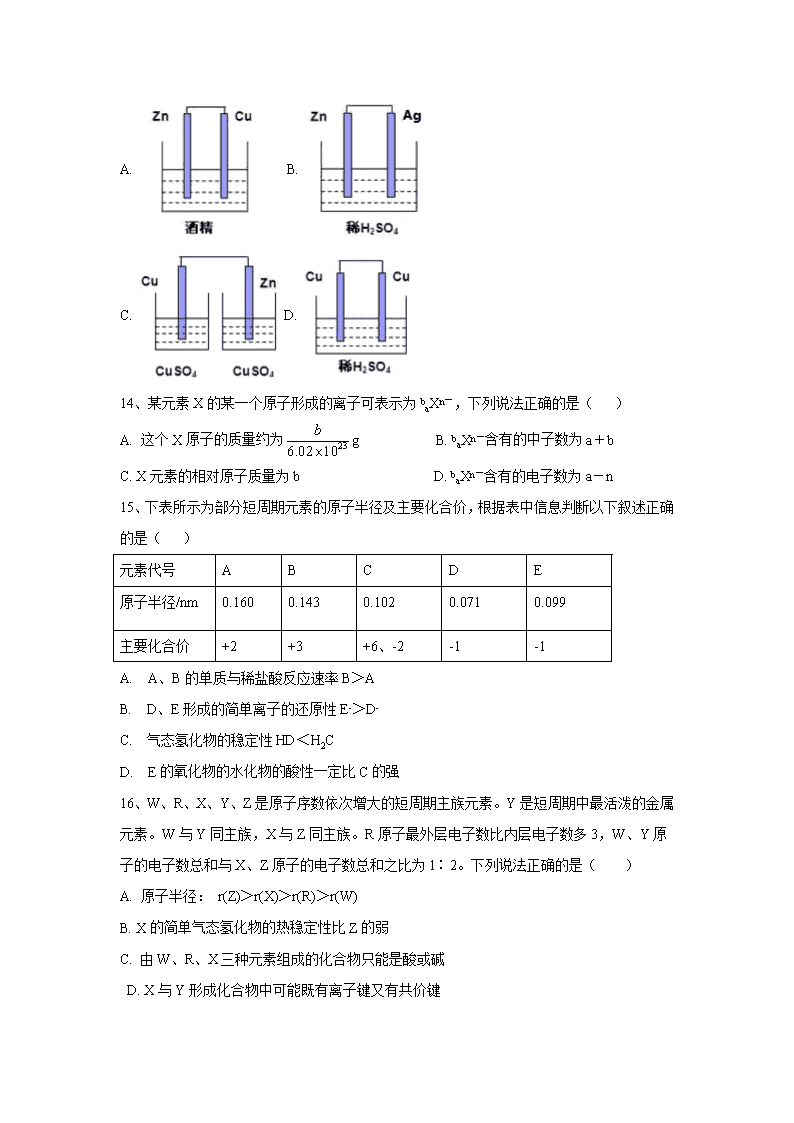
13、下列装置能构成原电池的是( )
A. B.
C. D.
14、某元素X的某一个原子形成的离子可表示为baXn-,下列说法正确的是( )
A. 这个X原子的质量约为g B. baXn-含有的中子数为a+b
C. X元素的相对原子质量为b D. baXn-含有的电子数为a-n
15、下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是( )
元素代号
A
B
C
D
E
原子半径/nm
0.160
0.143
0.102
0.071
0.099
主要化合价
+2
+3
+6、-2
-1
-1
A. A、B的单质与稀盐酸反应速率B>A
B. D、E形成的简单离子的还原性E->D-
C. 气态氢化物的稳定性HD<H2C
D. E的氧化物的水化物的酸性一定比C的强
16、W、R、X、Y、Z是原子序数依次增大的短周期主族元素。Y是短周期中最活泼的金属元素。W与Y同主族,X与Z同主族。R原子最外层电子数比内层电子数多3,W、Y原子的电子数总和与X、Z原子的电子数总和之比为1∶2。下列说法正确的是( )
A. 原子半径: r(Z)>r(X)>r(R)>r(W)
B. X的简单气态氢化物的热稳定性比Z的弱
C. 由W、R、X三种元素组成的化合物只能是酸或碱
D. X与Y形成化合物中可能既有离子键又有共价键
17、某同学在研究前18号元素时发现,可以将它们排成如下图所示的“蜗牛”形状,图中每个弧线上的“·”代表一种元素,其中O点代表氢元素。下列说法中错误的是( )
A.离O点越远的元素原子半径越大
B.虚线相连的元素处于同一族
C.B元素是图中金属性最强的元素
D.A、B两种元素组成的化合物中可能含有共价键
18、燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极。下列叙述不正确的是 ( )
A.a极是负极,该电极上发生氧化反应
B.b极反应是O2+4OH--4e-===2H2O
C.总反应方程式为2H2+O2===2H2O
D.氢氧燃料电池是一种具有应用前景的绿色电源
19、可用于电动汽车的铝—空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法正确的是( )
A.比较钠、镁、铝三种金属空气电池,Na-空气电池的理论比能量最高
B.以NaOH溶液为电解液时,负极反应为Al+3OH--3e-===Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的碱性保持不变
D.以NaCl溶液或NaOH溶液为电解液时,正极反应都为O2+2H2O+4e-===4OH-
20、一种微生物燃料电池如图所示,下列关于该电池的说法正确的是( )
A.a电极为正极
B.H+由右室通过质子交换膜进入左室
C.a电极的电极反应式为C6H5OH-28e-+11H2O===6CO2↑+28H+
D.当b电极上产生1 mol N2时,溶液中将有10 mol e-通过
21、微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2===6CO2+6H2O
22、汽车的启动电源常用铅蓄电池。其结构如下图所示,放电时的电池反应如下:
PbO2+Pb+2H2SO4===2PbSO4+2H2O 根据此反应判断下列叙述中正确的是 ( )
A.PbO2是电池的负极 B.Pb是负极
C.PbO2得电子,被氧化 D.电池放电时,溶液酸性增强
二、填空题(每空2分,共56分)
23. (16分)(1)有①168 O 、 17 8O 、 188O ;②H2、D2、T2;③石墨、金刚石;④11H 、21H、 31H;四组微粒或物质。互为同位素的是 (填编号,下同),互为同素异形体的是 。
(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391k J。则由氢气和氮气反应生成1 mol NH3需要 (填“放出”或“吸收”)
k J能量。
(3)控制和治理SO2是减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。若A为SO2,B为O2,C为H2SO4.则负极是 ______ (填“A”或“B”),负极反应式为 。
(4)已知由甲烷CH4和氧气构成的燃料电池,电解质溶液为KOH溶液时,负极通入的气体为 ,(填化学式),负极反应式为 ,
24.(12分)下表是元素周期表的一部分,按要求填空:
族
周期
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
2
①
②
3
③
④
⑤
⑥
⑦
⑧
4
⑨
⑩
(1)在这些元素中,最活泼的金属元素与最活泼的非金属元素形成的化合物是是:_____ (填化学式)。
(2)元素③、④、⑤的最高价氧化物的水化物中碱性最强的物质的电子式是:_______________;元素⑥、⑦、⑧的最高价氧化物的水化物的酸性最弱是_____________(填化学式)。③⑤⑧三种物质最高价的氧化物对应水化物两两能相互发生反应,写出⑤的最高价氧化物的水化物分别与③、⑧的最高价氧化物对应水反应反应的离子方程式________________________________________ __________________________
(3)用电子式表示元素⑦的氢化物的形成过程 。
25.(10分) 归纳整理是科学学习的重要方法之一。氧族元素的各种性质可归纳整理为如下表所示的表格(部分)。
元素
性质
8O
16S
34Se
52Te
单质熔点(℃)
-218.4
113
450
单质沸点(℃)
-183
444.6
685
989
主要化合价
-2
-2,+4,+6
-2,+4,+6
原子半径
逐渐增大
单质与H2反应情况
点燃时易化合
加热化合
加热难化合
不能直接化合
请根据表回答下列问题:
(1)硒的熔点范围可能是________________________________________________。
(2)碲的化合价可能有__________________________________________________。
(3)氢硒酸有较强的________(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生反应的化学方程式为________________________________________。
(4)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
______Al2Te3+( )===____Al(OH)3↓+______H2Te↑
26、(18分)某研究性学习小组设计了一组实验来探究元素周期律。甲同学设计了如图1装置,根据元素非金属性与对应最高价含氧酸之间的关系,可以一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、蘸有碱液的棉花。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
根据实验图1作答:
(1)写出选用试剂分别 B__________,C____________;
其中装置B中所盛试剂的作用为______________;C中反应的离子方程式为___________________;从实验所得非金属性C____Si(填“大于”或“小于”)
根据实验图2作答:
(2)写出 A处的离子方程式: ___________________________________________;
B处的现象 ,C处药品的作用 。
通过图2 装置实验得出同主族元素性质的递变规律为______________________________
【参考答案】