试题君之课时同步君2016-2017学年高二化学人教版选修4 (第3
绝密★启用前
人教版《选修四》第三章第四节
难溶电解质的溶解平衡
一、 选择题
1.Mg(OH)2在下列四种情况下,其溶解度最大的是( )
A.在纯水中
B.在0.1 mol·L-1的MgCl2溶液中
C.在0.1 mol·L-1的NH3·H2O中
D.在0.1 mol·L-1的CH3COOH溶液中
2.纯净的氯化钠是不潮解的,但家庭所用的食盐却很容易潮解,这主要是因为含有杂质MgCl2。为得到纯净的氯化钠,有人设计了这样一个实验:把买来的食盐放入纯氯化钠饱和溶液中一段时间,过滤,即得纯净的氯化钠固体。下列说法中正确的是( )
A.食盐的晶粒大一些有利于提纯
B.设计实验的根据是MgCl2比NaCl易溶于水
C.设计实验的根据是NaCl的溶解平衡
D.在整个过程中NaCl的浓度会变大
3.已知25 ℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol·L-1 HF溶液中加入1 L 0.2 mol·L-1 CaCl2溶液。则下列说法中正确的是( )
A.25 ℃时,0.1 mol·L-1 HF溶液pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中没有沉淀产生
D.该体系中HF与CaCl2反应产生沉淀
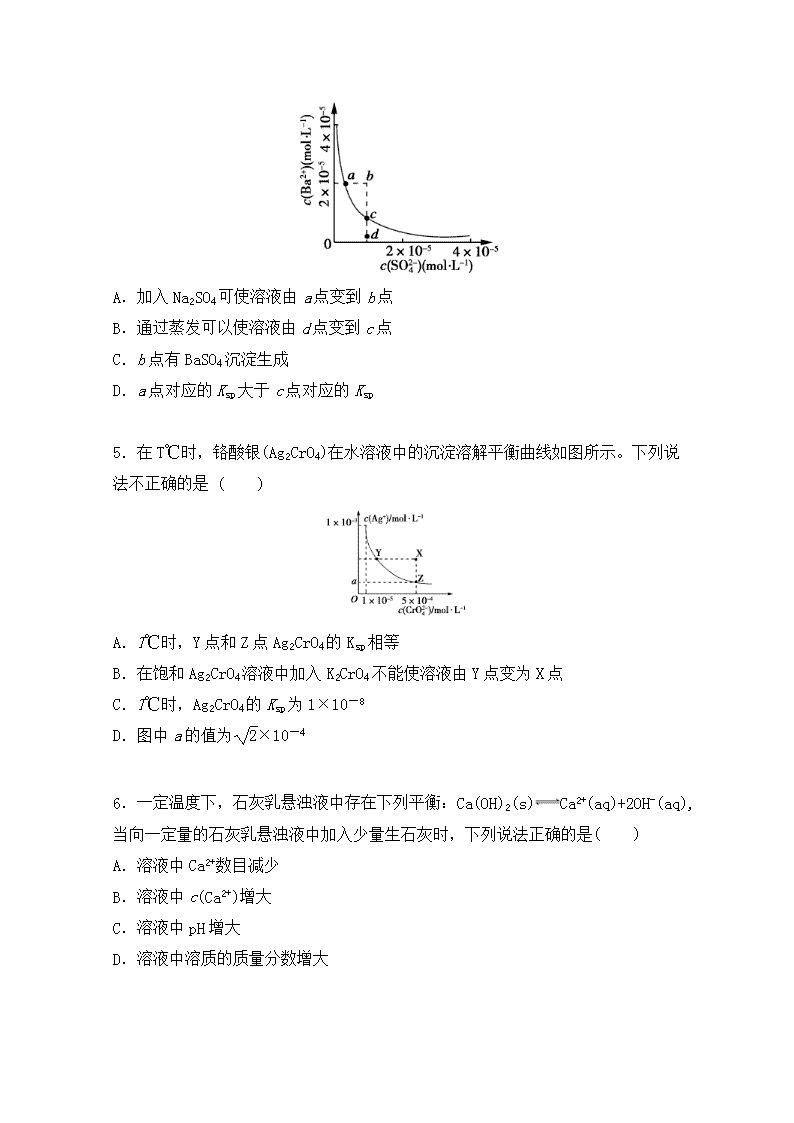
4.某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
A.加入Na2SO4可使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.b点有BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
5.在T℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示。下列说法不正确的是 ( )
A.T℃时,Y点和Z点Ag2CrO4的Ksp相等
B.在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.T℃时,Ag2CrO4的Ksp为1×10-8
D.图中a的值为×10-4
6.一定温度下,石灰乳悬浊液中存在下列平衡:Ca(OH)2(s)Ca2+(aq)+2OH-(aq),当向一定量的石灰乳悬浊液中加入少量生石灰时,下列说法正确的是( )
A.溶液中Ca2+数目减少
B.溶液中c(Ca2+)增大
C.溶液中pH增大
D.溶液中溶质的质量分数增大
7.实验:
①0.1 mol·L-1 AgNO3溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1 mol·L-1KI溶液,出现浑浊;
③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为黄色。
下列分析不正确的是( )
A.浊液a中存在沉淀溶解平衡:AgCl(s)Ag+(aq)+Cl-(aq)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶
8.锅炉水垢是一种安全隐患,除去水垢中的CaSO4,可先用Na2CO3溶液处理,使之转化为易溶于酸的CaCO3,而后用酸除去。下列说法不正确的是( )
A.CaCO3的溶解度小于CaSO4的
B.沉淀转化的实质是沉淀溶解平衡的移动
C.沉淀转化的难易与溶解度差别的大小无关
D.CaSO4到CaCO3的沉淀转化中并存着两个沉淀溶解平衡
9.要使工业废水中的重金属离子Pb2+沉淀,可用硫酸盐、碳酸盐、硫化物等作沉淀剂,已知Pb2+与这些离子形成的化合物的溶解度如下:
化合物
PbSO4
PbCO3
PbS
溶解度/g
1.03×10-4
1.81×10-7
1.84×10-14
由上述数据可知,选用的沉淀剂最好是( )
A.硫化物 B.硫酸盐
C.碳酸盐 D.以上沉淀剂均可
10.(双选)硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下。下列说法正确的是( )
A.温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小
B.三个不同温度中,313 K时Ksp(SrSO4)最大
C.283 K时,图中a点对应的溶液是不饱和溶液
D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
11.某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是( )
A.Ksp[Fe(OH)3]
1,A项错误。Ksp不随浓度变化而变化,B项错误。Ka(HF)= ==3.6×10-4,则c2(F-)=3.6×10-5,c(Ca2+)=0.1 mol·L-1,则Qc=c2(F-)·c(Ca2+)=3.6×10-6>1.46×10-10,体系中有CaF2沉淀析出,C项错误,D项正确。
【题型】选择题
【难度】容易
4. 【答案】C
【解析】BaSO4在水中存在着溶解平衡BaSO4(s)Ba2+(aq)+SO(aq),a点在平衡曲线上,加入Na2SO4会增大c(SO),平衡左移,c(Ba2+)应降低,A项错误;d点时溶液不饱和,蒸发溶剂水,c(SO)、c(Ba2+)均增大,B项错误;b点时溶液过饱和,有沉淀生成,C项正确;Ksp是一常数,温度不变Ksp不变,在曲线上的任意一点Ksp都相等,D项错误。
【题型】选择题
【难度】一般
5. 【答案】C
【解析】Ksp只与温度有关,故温度不变,Y、Z两点的Ksp相等,A项正确;在饱和Ag2CrO4溶液中加入K2CrO4,所得溶液仍为饱和Ag2CrO4溶液,点仍在曲线上,B项正确;T℃时Ksp(Ag2CrO4)=c2(Ag+)·c(CrO)=(1×10-3)2×1×10-5=1×10-11,C项错误;a点的值为=×10-4,D项正确。
【题型】选择题
【难度】容易
6. 【答案】A
【解析】生石灰溶于水可以和水化合生成氢氧化钙,同时放出大量的热,溶剂水减少,溶质减少,同时氢氧化钙的溶解度随温度的升高而降低,氢氧化钙的沉淀溶解平衡左移,所以溶液中一定有晶体析出,浓度也会降低。
【题型】选择题
【难度】容易
7. 【答案】B
【解析】浊液有AgCl和NaNO3组成,AgCl的浊液中存在沉淀溶解平衡AgCl(s)Ag+(aq)+Cl-(aq),A项正确、B项错误;由③及难溶沉淀可以转化为更难溶沉淀可知C、D项正确。
【题型】选择题
【难度】容易
8. 【答案】C
【解析】沉淀转化的方向是难溶物向更难溶的方向转化,所以沉淀的溶解度差别越大,越易转化,C选项错误。
【题型】选择题
【难度】容易
9. 【答案】A
【解析】产生的沉淀的溶解度越小,沉淀反应进行的越完全。在某种沉淀中加入适当的沉淀剂,可使原来的沉淀溶解而转化为另一种溶解度更小的沉淀。
【题型】选择题
【难度】容易
10. 【答案】BC
【解析】温度一定,Ksp(SrSO4)不变,A项错误;由题中沉淀溶解平衡曲线可知,313 K时,c(Sr2+)、c(SO42-)最大,则Ksp最大,B项正确;曲线上的点为饱和状态,a点c(Sr2+)小于平衡时c(Sr2+),故未达到饱和,沉淀继续溶解,C项正确;从283 K升温到363 K要析出固体,依然为饱和溶液,D项错误。
【题型】选择题
【难度】一般
11. 【答案】B
【解析】b、c两点金属阳离子的浓度相等,设都为x,c(OH-)b=10-12.7 mol·L-1,c(OH-)c=10-9.6 mol·L-1,则Ksp[Fe(OH)3]=x×(10-12.7)3,Ksp[Cu(OH)2]=x×(10-9.6)2,故Ksp[Fe(OH)3]Ksp
,要析出沉淀,故D选项正确。
【题型】选择题
【难度】一般
12. 【答案】B
【解析】Mg(OH)2的溶度积小,故其电离的Mg2+浓度要小一些,A项错误;NH可以结合Mg(OH)2电离出的OH-离子,从而促使Mg(OH)2的电离平衡正向移动,c(Mg2+)增大,B项正确;Ksp仅与温度有关,C项错误;只要Qc>KSP则生成MgF2沉淀,D项错误。
【题型】选择题
【难度】一般
13. 【答案】D
【解析】饱和AgCl溶液中c(Ag+)=c(Cl-),依据Ksp(AgCl)=c(Ag+)·c(Cl-)=c2(Ag+)=1.56×10-10可知c(Ag+)=×10-5 mol·L-1,同理Ag2CrO4溶液中c(Ag+)=2c(CrO),Ksp(Ag2CrO4)=c2(Ag+)·c(CrO)=c3(Ag+)=1×10-12可知c(Ag+)=×10-4 mol·L-1,A项错误;依据CrO+2Ag+===Ag2CrO4↓,溶液中c(Ag+)==2×10-4 mol·L-1,依据Ksp(Ag2CrO4)=c2(Ag+)·c(CrO)=1×10-12,可知溶液中c(CrO)=2.5×10-5 mol·L-1>10-5 mol·L-1,C项错误;AgCl开始沉淀时c(Cl-)= mol·L-1=1.56×
10-7 mol·L-1;Ag2CrO4开始沉淀时c(CrO)= mol·L-1=10-6 mol·L-1,D项正确。
【题型】选择题
【难度】一般
14. 【答案】(1)有机羧酸电离出H+与Ca5(PO4)3OH电离出的OH-发生反应;H++OH-H2O,使Ca5(PO4)3OH的溶解平衡向右移动
(2)F-与Ca5(PO4)3OH溶解产生的Ca2+、PO43-发生反应生成更难溶的Ca5(PO4)3F,5Ca2++
3PO43-+F-Ca5(PO4)3F↓
(3)在牙膏中加Ca2+,使上述溶解平衡向左移动
【解析 】(1)有机羧酸电离出H+与Ca5(PO4)3OH电离出的OH-发生反应:H++OH-H2O,使Ca5(PO4)3OH的溶解平衡向右移动,Ca5(PO4)3OH逐渐溶解,导致牙齿腐蚀出现龋齿。
(2)根据难溶电解质的转化规律,溶解度较小的物质可以转化成溶解度更小的物质。依据题给信息可知:F-可以替代平衡中的OH-,生成溶解度更小、质地更坚硬的Ca5(PO4)3F,从而保护牙齿防止龋齿:5Ca2++3PO43-+F-Ca5(PO4)3F↓。
(3)促进矿化的方法之一就是使Ca5(PO4)3OH的溶解平衡向左移动,减少Ca5(PO4)3OH的溶解。一种可行的方法是在牙膏中加Ca2+,使上述溶解平衡向左移动。
【难度】容易
15. 【答案】(1)①变小 ②不变 ③变小 变大
(2)B、E
(3)AgI、AgBr AgBr(s)+I-(aq)AgI(s)+Br-(aq)
【解析】(1)①加入AgNO3固体,使c(Ag+)增大,AgI溶解平衡向左移动,c(I-)变小。②加入更多的AgI固体,仍是该温度下的饱和溶液,各离子浓度不变。③因AgBr的溶解度大于AgI的溶解度,所以加入AgBr固体时,使c(Ag+)变大,而使AgI的溶解平衡向生成AgI的方向移动,c(I-)变小。
(2)相同类型的难溶电解质,Ksp越小,溶解度才越小,不同类型的难溶电解质不能根据Ksp判断溶解度的大小,A项错误;温度不变,Ksp与S均不变,B项正确;Ksp是各离子浓度的幂之积,C项错误;生成沉淀的先后还与离子的浓度有关,D项错误、E正确;同离子效应不会改变Ksp,F项错误。
(3)等体积混合后c(Br-)=c(I-)=0.001mol/L,c(Ag+)=2×10-3 mol/L.因Ksp(AgI)<Ksp(AgBr),AgI先沉淀,当I-完全沉淀时,消耗c(Ag+)=c(I-)=0.001mol/L,剩余c(Ag+)=2×10-3 mol/L-0.001mol/L=0.001mol/L,Q(AgBr)=0.001mol/L×0.001mol/L=1×10-6>4.9×10-13,所以有AgBr沉淀生成;而再向其中加入适量NaI固体时,会有AgBr转化为AgI。
【难度】容易
16. 【答案】(1)①B ②C、D (2)4 3 可行
【解析】(1)①四个选项中的物质均能将Fe2+氧化成Fe3+,但只有H2O2的还原产物为H2O,不引入新的杂质。
②加入CuO或Cu(OH)2时既不引入新的杂质,同时能消耗Fe3+水解生成的H+,从而促进Fe3+完全水解为Fe(OH)3而除去。
(2)Ksp[Cu(OH)2]=c(Cu2+)·c2(OH-),则c(OH-)==1.0×10-10(mol·L-1),则c(H+)=1.0×10-4 mol·L-1,pH=4。Fe3+完全沉淀时;Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-),则c(OH-)==1.0×10-11 mol·L-1。此时c(H+)=1×10-3 mol·L-1,pH=3,因此上述方案可行。
【难度】一般
17. 【答案】(1)使碘化铅快速、充分溶解
(2)产生黄色沉淀或黄色浑浊 减小
(3)1.35×10-8 (4)偏小
【解析】Ⅰ.PbI2为难溶电解质,因此搅拌的目的是使PbI2快速充分地溶解,滴加0.1
mol·L-1 KI溶液,c(I-)增大,PbI2(s)Pb2+(aq)+2I-(aq)向左移动,c(Pb2+)减小,并析出PbI2沉淀。II.由2RH+Pb2+===R2Pb+2H+知,n(Pb2+)=3.000×10-5 mol×=1.500×10-5mol,所以c(Pb2+)==1.500×10-3 mol·L-1,c(I-)=1.500×10-3mol·L-1×2=3.000×
10-3mol·L-1,Ksp=c(Pb2+)·c2(I-)=1.500×10-3×(3.000×10-3)2=1.35×10-8;若步骤Ⅰ盛装滤液的烧杯中有少量水,会使c(Pb2+)减少,Ksp偏小。
【难度】一般