2017-2018学年重庆市铜梁县第一中学高二10月月考化学试题
2017-2018 学年重庆市铜梁县第一中学高二 10 月月考化学试题
命题人:车耀 审题人:廖云峰
一:选择题(3 分/题,共 20 个小题,60 分)
1.下列反应既属于氧化还原反应,又属于吸热反应的是( )
A.铝片和稀盐酸反应 B. Ba(OH)2·8H2O 与 NH4Cl 的反应
C.灼热的碳与二氧化碳的反应 D.甲烷在氧气中的燃烧
2.已知:H2(g)+F2(g) 2HF(g) ΔH=-270 kJ·mol-1。下列说法正确的是( )
A.2 L 氟化氢气体分解成 1 L 氢气与 1 L 氟气吸收 270 kJ 热量
B.1 mol 氢气与 1 mol 氟气反应生成 2 mol 液态氟化氢放出的热量小于 270 kJ
C.在相同条件下,1 mol 氢气与 1 mol 氟气的能量总和大于 2 mol 氟化氢气体的能量
D.1 个氢气分子与 1 个氟气分子反应生成 2 个氟化氢气体分子放出 270 kJ 热量
3.对于可逆反应 3H2+N2 2NH3,下列措施能使反应物中活化分子百分数、化学
反应速率和化学平衡常数都变化的是( )
A.增大压强 B.充入更多 N2 C.使用高效催化剂 D.降低温度
4.对可逆反应 4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时 4v 正(O2)=5v 逆(NO)
B.若单位时间内生成 x mol NO 的同时,消耗 x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系:2v 正(NH3)=3v 正(H2O)
5.某小组为研究电化学原理,设计如图 2 装置。下列叙述不正确...的是( )
A.a 和 b 不连接时,铁片上会有金属铜析出
B.a 和 b 用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C.无论 a 和 b 是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D.a 和 b 分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
6.实验测得:101 kPa 时,1 mol H2 完全燃烧生成液态水,放出 285.8 kJ 的热量;1 mol CH4
完全燃烧生成液态水和 CO2,放出 890.3 kJ 的热量。下列热化学方程式的书写正确的是
( )
①CH4(g)+2O2(g) CO2(g)+2H2O(l);ΔH=+890.3 kJ·mol-1
②CH4(g)+2O2(g) CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
③CH4(g)+2O2(g) CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1
④2H2(g)+O2(g) 2H2O(l);ΔH=-571.6 kJ·mol-1
A.② B.②④ C.②③④ D.①②③④
7.下列热化学方程式书写正确的是( 的绝对值均正确)
A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=—1367.0 kJ/mol
(燃烧热)
B. NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中
和热)
C.S(s)+O2(g)===SO2(g);△H=—269.8kJ/mol(反应热)
D. 2NO2==O2+2NO;△H=+116.2kJ/mol(反应热)
8.已知:2CO(g)+O2(g)=2CO2(g) △H=—566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g)
△H=—226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO 的燃烧热为 283kJ
B.右图可表示由 CO 生成 CO2 的反应过程和能量关系
C.2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=—452kJ/mol
D.CO(g)与 Na2O2(s)反应放出 509kJ 热量时,电子转移数为 6.02×1023
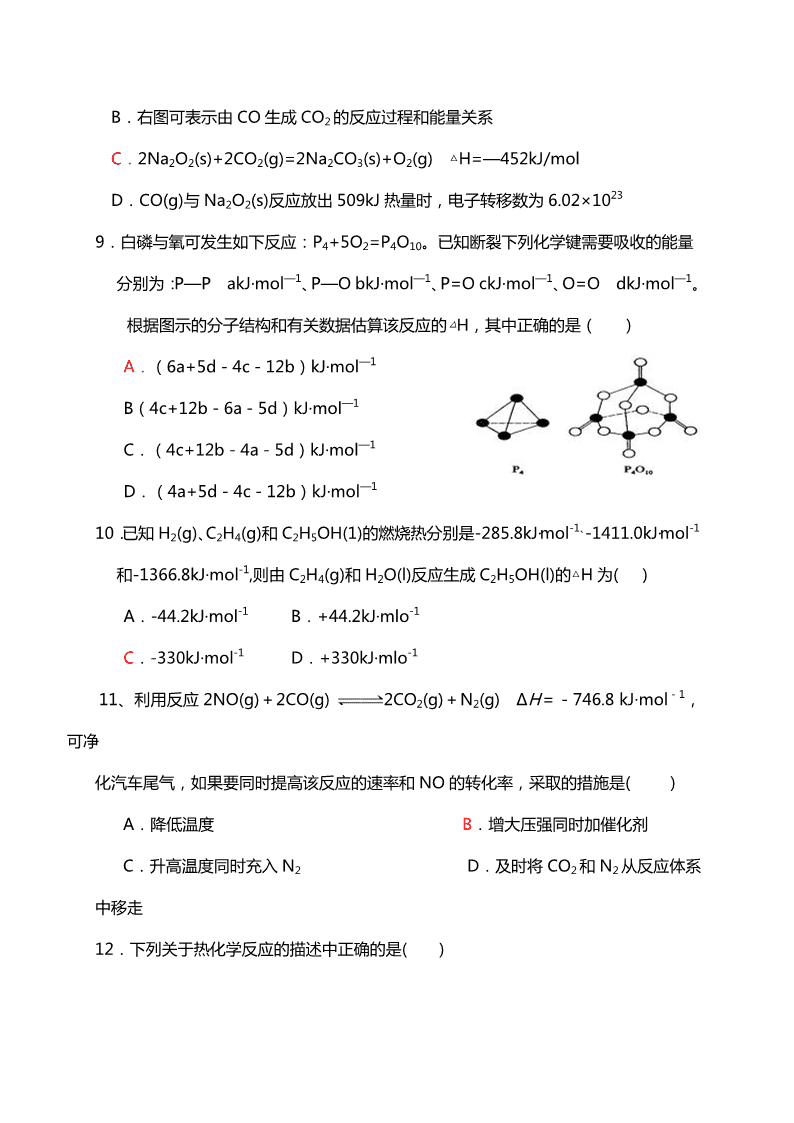
9.白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量
分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A.(6a+5d-4c-12b)kJ·mol—1
B(4c+12b-6a-5d)kJ·mol—1
C.(4c+12b-4a-5d)kJ·mol—1
D.(4a+5d-4c-12b)kJ·mol—1
10.已知 H2(g)、C2H4(g)和 C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1
和-1366.8kJ·mol-1,则由 C2H4(g)和 H2O(l)反应生成 C2H5OH(l)的△H 为( )
A.-44.2kJ·mol-1 B.+44.2kJ·mlo-1
C.-330kJ·mol-1 D.+330kJ·mlo-1
11、利用反应 2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,
可净
化汽车尾气,如果要同时提高该反应的速率和 NO 的转化率,采取的措施是( )
A.降低温度 B.增大压强同时加催化剂
C.升高温度同时充入 N2 D.及时将 CO2 和 N2 从反应体系
中移走
12.下列关于热化学反应的描述中正确的是( )
A.HCl 和 NaOH 反应的中和热△H=-57.3kJ/mol,则 H2SO4 和 Ca(OH)2 反应的
中和热△H=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是 283.0kJ/mol,则 2CO2(g)===2CO(g)+O2(g)反应的△H=2
×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
13.一定条件下,在密闭容器中,能表示反应 X(g)+2Y(g) 2Z(g)一定达到化学
平衡状态的是( )
①X、Y、Z 的物质的量之比是 1∶2∶2 ②X、Y、Z 的浓度不再发生变化
③容器中的压强不再发生变化 ④单位时间内生成 n mol Z,同时生成 2n
mol Y
A.①② B.①④ C.②③ D.③④
14.反应 CH3OH(l)+NH3(g)===CH3NH2(g)+H2O(g)在某温度自发向右进行,若反
应的|ΔH|=17 kJ·mol-1,|ΔH-TΔS|=17 kJ·mol-1,则下列正确的是( )
A.ΔH>0,ΔH-TΔS<0 B.ΔH<0,ΔH-TΔS>0
C.ΔH>0,ΔH-TΔS>0 D.ΔH<0,ΔH-TΔS<0
15.一定条件下,在某密闭容器中进行如下反应:mA(g)+nB(g) pC(g)+qD(g),
若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图 15 所示,则
对该反应的叙述正确的是( )
A.正反应是吸热反应 B.逆反应是放热反应
C.m+n
p+q
16.一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合图 19 的是( )
A.CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g) ΔH<0
B.CO2(g)+H2(g) CO(g)+H2O(g) ΔH>0
C.CH3CH2OH(g) CH2FCH2(g)+H2O(g) ΔH>0
D . 2C6H5CH2CH3(g) + O2(g) 2C6H5CH F CH2(g) +
2H2O(g)ΔH<0
17.将等物质的量的 X、Y 气体充入一个密闭容器中,在一定条件下发生如下反应并达
到平衡:X(g)+Y(g) 2Z(g) ΔH<0。当改变某个条件并达到新平衡后,下列叙述
正确的是( )
A.升高温度,X 的体积分数减小
B.增大压强(缩小容器体积),Z 的浓度不变
C.保持容器体积不变,充入一定量的惰性气体,Y 的浓度减小
D.保持容器体积不变,充入一定量的 Z,X 的体积分数不变
18.金属镍有广泛的用途。粗镍中含有少量 Fe、Zn、Cu、Pt 等杂质,可用电解法制备
高纯度的镍,下列叙述正确的是(已知:氧化性 Fe2+<Ni2+<Cu2+)( )
A. 阳极发生还原反应,其电极反应式:Ni2++2e- =Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在的金属阳离子只有 Fe2+和 Zn2+
D. 电解后,电解槽底部的阳极泥中只有 Cu 和 Pt
19.关于下列装置说法正确的是( )
A.装置①中,盐桥中的 K+移向 ZnSO4 溶液 B.用装置③精炼铜时,c 极为粗铜
C.装置②工作一段时间后,a 极附近溶液的 pH 增大
D.装置④中电子由 Zn 流向 Fe,装置中有 Fe2+生成
20.关于铅蓄电池 Pb+PbO2+2H2SO4 PbSO4+2H2O 的说法正确的是( )
A.在放电时,正极发生的反应是 Pb(s) +SO4
2—(aq)= PbSO4(s) +2e—
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO4(s)+2e—= Pb(s)+ SO4
2—(aq)
二、填空题(共 40 分)
21.(共 14 分)(一)在一个 1 L 的密闭容器中,加入 2 mol A 和 1 mol B,发生下列
反应:2A(g)+B(g) 3C(g)+D(s),达到平衡时,C 的浓度为 1.2 mol·L-1。
(1)维持容器的温度不变,若缩小容器的体积,则平衡________移动(填“向正反应方
向”或“向逆反应方向”或“不”)。
(2)维持容器的体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C 的
浓度仍是 1.2 mol·L-1 的是________。
A.4 mol A+2 mol B B.3 mol C+1 mol D
C.2 mol A+1 mol B+1 mol D
(3)若维持容器内的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,
达到平衡时,C 的浓度仍是 1.2 mol·L-1,则 C 的起始物质的量应满足的条件是________。
(二)Ⅰ.工业上利用 H2 和 CO2 合成二甲醚的反应如下:6H2(g)+2CO2(g)
CH3OCH3(g)+3H2O(g) ΔH<0
温度升高,该化学平衡移动后到达新的平衡,CH3OCH3 的产率将________(填“变大”、
“变小”或“不变”,下同),混合气体的平均相对分子质量将________;
Ⅱ.某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新
型硝化剂反应 4NO2(g)+O2(g) 2N2O5(g) ΔH<0 的影响。
(1)图像中 T1 和 T2 的关系是 T1________T2(填“>”、“<”或“=”);
(2)比较 a、b、c 三点所处的平衡状态中,反应物 NO2 的转化率最
大的是________(填字母);
22.(2 分/空:共 16 分)Ⅰ、北京奥运会“祥云”火炬燃料是丙烷
(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
丙烷脱氢可得丙烯。
已知:C3H8(g)===CH4(g)+HC≡CH(g)+H2(g);△H1=156.6 kJ·mol-1
CH3CH=CH2(g)===CH4(g)+HC=CH(g);△H2=32.4 kJ·mol-1
则相同条件下,反应 C3H8(g)===CH3CH=CH2(g)+H2(g)的△H=_
kJ·mol-1
Ⅱ、红磷 P(s)和 Cl2(g)发生反应生成 PCl3(g)和
PCl5(g)。反应过程和能量关系如图所示(图
中的△H 表示生成 1mol 产物的数据)。
根据上图回答下列问题:
(1)P 和 Cl2 反应生成 PCl3 的热化学方程式_________________________________。
(2)PCl5 分解成 PCl3 和 Cl2 的热化学方程式_________________________________,上述分
解反应是一个可逆反应,温度 T1 时,在密闭容器中加入 0.80molPCl5,反应达到
平衡时 PCl5 还剩 0.60mol,其分解率α1 等于_________;若反应温度由 T1 升高到
T2,平衡时 PCl5 的分解率为α2,α2_______α1(填“大于”、“小于”或“等于”)。
(3)工业上制备 PCl5 通常分两步进行,先将 P 和 Cl2 反应生成中间产物 PCl3,然后降
温,再和 Cl2 反应生成 PCl5。原因是________________________________________。
(4)P 和 Cl2 分两步反应生成 1molPCl5 的△H3=_________,P 和 Cl2 一步反应生成
1molPCl5 的△H4______△H3(填“大于”、“小于”或“等于”)。
23.I、(共 10 分)如图所示,水槽中试管内有一枚铁钉,放置数天观察:
(1)铁钉在逐渐生绣。
(2)若试管内液面上升,发生 腐蚀,电极反应:
负极: ,
正极: 。
(3)若试管内液面下降,则原溶液呈 性,发生的电极反应:
正极: 。
II、电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液 a;X、Y
是两块电极板,通过导线与直流电源相连。请回答以下问题:若 X、Y 都是惰性电极,a
是饱和 NaCl 溶液,实验开始时,同时在两边各滴入几滴酚酞试液,
则
电解池中 X 极上的电极反应式
是 。
在 X 极附近观察到的现象是 。
Y 电极上的电极反应式是 ,(2 分)
在 Y 极附近观察到的现象是 。[]
铜梁一中高二上期第一次月考答题卷
二、填空题:
21.(共 14 分)
(一)(1) (填“向正反应方向”或“向逆反应方向”或“不”)。
(2) 。
(3 。
(二)Ⅰ. (填“变大”、“变小”或“不变”,下同), ;
Ⅱ. (1)图 T1________T2(填“>”、“<”或“=”);
(2) (填字母);
22.(2 分/空:共 16 分)Ⅰ、△H= kJ·mol-1
Ⅱ、 (1) 。
(2) ;_ ;;
α2_______α1(填“大于”、“小于”或“等于”)。
(3) 。
(4)△H3= ,△H4______△H3(填“大于”、“小于”或“等于”)。
23.I、(共 10 分)
(2) 腐蚀,
负极: ,
正极: 。
(3) 性,
正极: 。
II、 。
。
,(2 分)
。
答案为红色选项部分
一:选择题(3 分/题,共 20 个小题,60 分)
1.下列反应既属于氧化还原反应,又属于吸热反应的是( )
A.铝片和稀盐酸反应 B. Ba(OH)2·8H2O 与 NH4Cl 的反应
C.灼热的碳与二氧化碳的反应 D.甲烷在氧气中的燃烧
2.已知:H2(g)+F2(g) 2HF(g) ΔH=-270 kJ·mol-1。下列说法正确的是( )
A.2 L 氟化氢气体分解成 1 L 氢气与 1 L 氟气吸收 270 kJ 热量
B.1 mol 氢气与 1 mol 氟气反应生成 2 mol 液态氟化氢放出的热量小于 270 kJ
C.在相同条件下,1 mol 氢气与 1 mol 氟气的能量总和大于 2 mol 氟化氢气体的能量
D.1 个氢气分子与 1 个氟气分子反应生成 2 个氟化氢气体分子放出 270 kJ 热量
3.对于可逆反应 3H2+N2 2NH3,下列措施能使反应物中活化分子百分数、化学
反应速率和化学平衡常数都变化的是( )
A.增大压强 B.充入更多 N2 C.使用高效催化剂 D.降低温度
4.对可逆反应 4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时 4v 正(O2)=5v 逆(NO)
B.若单位时间内生成 x mol NO 的同时,消耗 x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系:2v 正(NH3)=3v 正(H2O)
5.某小组为研究电化学原理,设计如图 2 装置。下列叙述不正确...的是( )
A.a 和 b 不连接时,铁片上会有金属铜析出
B.a 和 b 用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C.无论 a 和 b 是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D.a 和 b 分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
6.实验测得:101 kPa 时,1 mol H2 完全燃烧生成液态水,放出 285.8 kJ 的热量;1 mol CH4
完全燃烧生成液态水和 CO2,放出 890.3 kJ 的热量。下列热化学方程式的书写正确的是
( )
①CH4(g)+2O2(g) CO2(g)+2H2O(l);ΔH=+890.3 kJ·mol-1
②CH4(g)+2O2(g) CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
③CH4(g)+2O2(g) CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1
④2H2(g)+O2(g) 2H2O(l);ΔH=-571.6 kJ·mol-1
A.② B.②④ C.②③④ D.①②③④
7.下列热化学方程式书写正确的是( 的绝对值均正确)
A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=—1367.0 kJ/mol
(燃烧热)
B. NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中
和热)
C.S(s)+O2(g)===SO2(g);△H=—269.8kJ/mol(反应热)
D. 2NO2==O2+2NO;△H=+116.2kJ/mol(反应热)
8.已知:2CO(g)+O2(g)=2CO2(g) △H=—566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g)
△H=—226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO 的燃烧热为 283kJ
B.右图可表示由 CO 生成 CO2 的反应过程和能量关系
C.2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=—452kJ/mol
D.CO(g)与 Na2O2(s)反应放出 509kJ 热量时,电子转移数为 6.02×1023
9.白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量
分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A.(6a+5d-4c-12b)kJ·mol—1
B(4c+12b-6a-5d)kJ·mol—1
C.(4c+12b-4a-5d)kJ·mol—1
D.(4a+5d-4c-12b)kJ·mol—1
10.已知 H2(g)、C2H4(g)和 C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1
和-1366.8kJ·mol-1,则由 C2H4(g)和 H2O(l)反应生成 C2H5OH(l)的△H 为( )
A.-44.2kJ·mol-1 B.+44.2kJ·mlo-1
C.-330kJ·mol-1 D.+330kJ·mlo-1
11、利用反应 2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,
可净
化汽车尾气,如果要同时提高该反应的速率和 NO 的转化率,采取的措施是( )
A.降低温度 B.增大压强同时加催化剂
C.升高温度同时充入 N2 D.及时将 CO2 和 N2 从反应体系
中移走
12.下列关于热化学反应的描述中正确的是( )
A.HCl 和 NaOH 反应的中和热△H=-57.3kJ/mol,则 H2SO4 和 Ca(OH)2 反应的
中和热△H=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是 283.0kJ/mol,则 2CO2(g)===2CO(g)+O2(g)反应的△H=2
×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
13.一定条件下,在密闭容器中,能表示反应 X(g)+2Y(g) 2Z(g)一定达到化学
平衡状态的是( )
①X、Y、Z 的物质的量之比是 1∶2∶2 ②X、Y、Z 的浓度不再发生变化
③容器中的压强不再发生变化 ④单位时间内生成 n mol Z,同时生成 2n
mol Y
A.①② B.①④ C.②③ D.③④
14.反应 CH3OH(l)+NH3(g)===CH3NH2(g)+H2O(g)在某温度自发向右进行,若反
应的|ΔH|=17 kJ·mol-1,|ΔH-TΔS|=17 kJ·mol-1,则下列正确的是( )
A.ΔH>0,ΔH-TΔS<0 B.ΔH<0,ΔH-TΔS>0
C.ΔH>0,ΔH-TΔS>0 D.ΔH<0,ΔH-TΔS<0
15.一定条件下,在某密闭容器中进行如下反应:mA(g)+nB(g) pC(g)+qD(g),
若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图 15 所示,则
对该反应的叙述正确的是( )
A.正反应是吸热反应 B.逆反应是放热反应
C.m+np+q
16.一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合图 19 的是( )
A.CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g) ΔH<0[
B.CO2(g)+H2(g) CO(g)+H2O(g) ΔH>0
C.CH3CH2OH(g) CH2FCH2(g)+H2O(g) ΔH>0
D . 2C6H5CH2CH3(g) + O2(g) 2C6H5CH F CH2(g) +
2H2O(g)ΔH<0
17.将等物质的量的 X、Y 气体充入一个密闭容器中,在一定条件下发生如下反应并达
到平衡:X(g)+Y(g) 2Z(g) ΔH<0。当改变某个条件并达到新平衡后,下列叙述
正确的是( )
A.升高温度,X 的体积分数减小
B.增大压强(缩小容器体积),Z 的浓度不变
C.保持容器体积不变,充入一定量的惰性气体,Y 的浓度减小
D.保持容器体积不变,充入一定量的 Z,X 的体积分数不变
18.金属镍有广泛的用途。粗镍中含有少量 Fe、Zn、Cu、Pt 等杂质,可用电解法制备
高纯度的镍,下列叙述正确的是(已知:氧化性 Fe2+<Ni2+<Cu2+)( )
A. 阳极发生还原反应,其电极反应式:Ni2++2e- =Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等]
C. 电解后,溶液中存在的金属阳离子只有 Fe2+和 Zn2+
D. 电解后,电解槽底部的阳极泥中只有 Cu 和 Pt
19.关于下列装置说法正确的是( )
A.装置①中,盐桥中的 K+移向 ZnSO4 溶液 B.用装置③精炼铜时,c 极为粗铜
C.装置②工作一段时间后,a 极附近溶液的 pH 增大
D.装置④中电子由 Zn 流向 Fe,装置中有 Fe2+生成
20 关于铅蓄电池 Pb+PbO2+2H2SO4 PbSO4+2H2O 的说法正确的是( )
A.在放电时,正极发生的反应是 Pb(s) +SO4
2—(aq)= PbSO4(s) +2e—
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO4(s) +2e—= Pb(s)+ SO4
2—(aq)
21.(每空两分)
(一)(1)不 (2)BC (3)1.2 mol
查看更多