山东省2021届高三等级考化学冲刺卷(二) Word版含答案
等级考仿真冲刺卷(二)
(时间:90 分钟 满分:100 分)
可能用到的相对原子质量:H 1 C 12 O 16 K 39 Cu 64 Zn 65
Se 79
一、选择题:本题共 10 小题,每小题 2 分,共 20 分。每小题只有一个
选项符合题意。
1.2020 年春节期间举行的《中国诗词大会》第五季精彩纷呈,体现了
中国诗词博大精深。下列诗词分析错误的是( )
A.“弄风柳絮疑成雪,满地榆钱买得春”中的“柳絮”和棉花的成分
均含纤维素
B.“日暮汉宫传蜡烛,轻烟散入五侯家”中的“蜡烛”是高级脂肪酸
酯,也是高分子化合物
C.“炎炎日正午,灼灼火俱燃”中的“炎炎”体现自然界中太阳能与
热能的转化
D.“煮豆持作羹,漉鼓以为汁”中的“漉鼓”涉及的基本操作是过滤
2.根据如图的转化关系判断下列说法正确的是(反应条件已略去)
( )
A.反应①②③④⑤均属于氧化还原反应和离子反应
B.反应⑤说明该条件下铝的还原性强于锰
C.相同条件下生成等量的 O2,反应③和④转移的电子数之比为 1∶1
D.反应①中氧化剂与还原剂的物质的量之比为 1∶4
3.下列各项比较中,一定相等的是( )
A.相同质量的 Fe 完全转化为 FeCl2 和 FeCl3 时转移的电子数
B.相同质量的苯和乙炔所含的碳原子的数目
C.标准状况下的 2.24 L HCl 气体和 1 L 0.1 mol·L-1 盐酸中所含 Cl-
的数目
D.相同物质的量浓度的 NH4Cl 和(NH4)2Fe(SO4)2 溶液中 N
H4
+
的浓度
4.下列解释事实的方程式不正确的是( )
A.“84”消毒液(有效成分为 NaClO)中加入少量白醋可增强消毒效
果:ClO-+ CH3COOH HClO + CH3COO-
B.用 Na2CO3 将水垢中的 CaSO4 转化为易于除去的 CaCO3:CaSO4 +
C
O3
2
- CaCO3 + S
O4
2
-
C.稀硫酸酸化的淀粉 KI 溶液在空气中放置一段时间后变蓝:2I-+
S
O4
2
-+ 4H+ I2+ SO2+ 2H2O
D.用 Na2S2O3 做碘量法实验时,溶液 pH 不可太低:S2
O3
2
-+ 2H+ SO2 +
S↓ + H2O
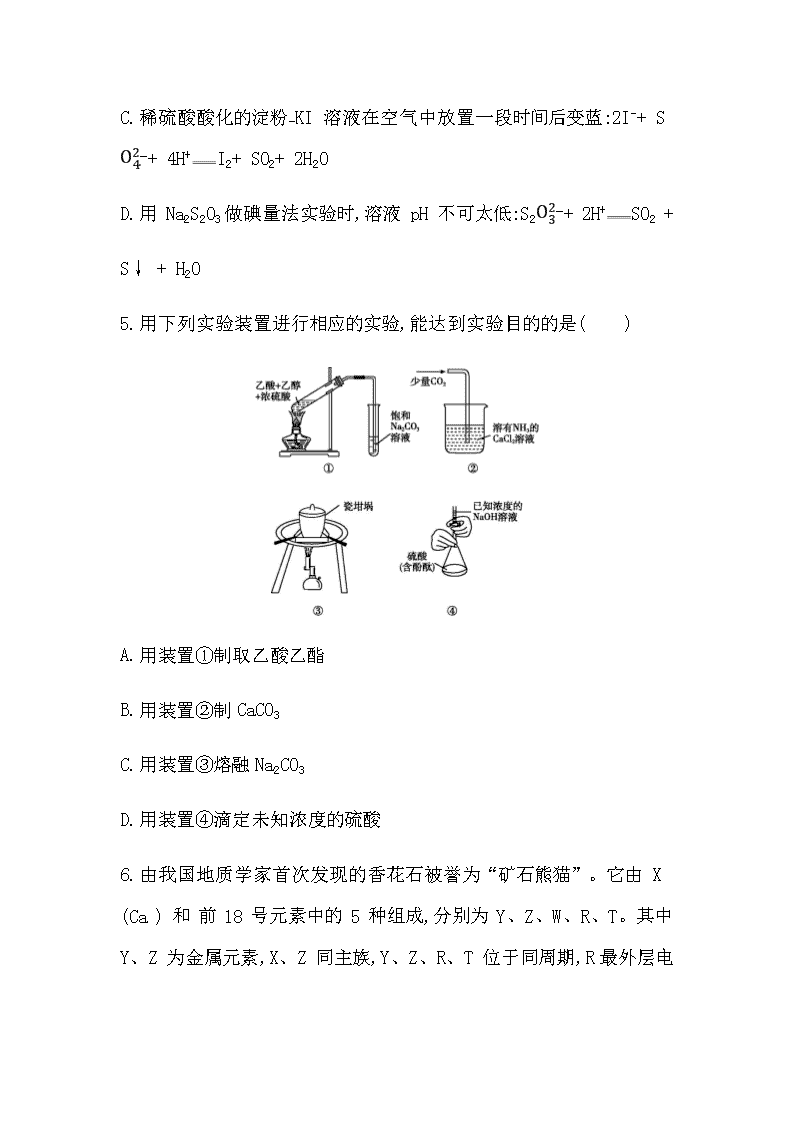
5.用下列实验装置进行相应的实验,能达到实验目的的是( )
A.用装置①制取乙酸乙酯
B.用装置②制 CaCO3
C.用装置③熔融 Na2CO3
D.用装置④滴定未知浓度的硫酸
6.由我国地质学家首次发现的香花石被誉为“矿石熊猫”。它由 X
(Ca ) 和 前 18 号元素中的 5 种组成,分别为 Y、Z、W、R、T。其
中 Y、Z 为金属元素,X、Z 同主族,Y、Z、R、T 位于同周期,R 最外
层电子数是次外层的 3 倍,T 无正价,X 与 R 原子序数之和是 W 的 2 倍。
下列说法错误的是( )
A.XR2、 WR2 两种化合物均为离子晶体
B.原子半径:Y>Z>R>T
C.最高价氧化物对应的水化物的碱性:X>Z
D.气态氢化物的稳定性:W
”“=”或“<”)vⅡ。
Ⅰ.410 ℃、
�
(
HCl
)
�
(
O2
) =3、
�
(催化剂)
�
(
HCl
) =350 g·min·mol-1;Ⅱ.390 ℃、
�
(
HCl
)
�
(
O2
) =
4、
�
(催化剂)
�
(
HCl
) =350 g·min·mol-1。
(3)在 101.325 kPa 时,以含 N2 的 HCl 和 O2 的混合气体测定不同温度
下 HCl 催化氧化反应中 HCl 的平衡转化率,得到如图结果。
①360 ℃时反应的平衡常数 K360 与 400 ℃时反应的平衡常数 K400 之间
的关系是 K360 (填“>”“=”或“<”)K400。
②一定温度下随着
�
(催化剂)
�
(
HCl
) 的增大,HCl 的平衡转化率 (填“增
大”“减小”或“不变”),原因为
。
19.(12 分)苯二氮卓类药物氟马西尼(F)的合成路线如图所示。请回
答下列问题:
(1)A 中官能团有氟原子、 和 。
(均填名称)
(2)C3H5O2Cl 的结构式为 。
(3)反应①和②的反应类型相同,其反应类型是 。
(4)化合物 D 的分子式为 。
(5)反应⑤生成“ 物质 F” 和 HCl,则 E→F 的化学反应方程式为
。
(6) 是 F 的同分异构体,其中 X 部分含—COOH 且没有支链,满
足该条件的同分异构体有 种(不考虑立体异构)。
(7)已知氨基酸之间脱水能够形成含肽键的化合物,请设计由甘氨酸
(HOOCCH2NH2)和 CNCH2COOC2H5 制备 的合成路线(无机试
剂任选)。
20.(12 分)Kx[Cu(C2O4)y]·zH2O[水合草酸铜(Ⅱ)酸钾]是一种化工原
料,实验室制备少量水合草酸铜酸钾并测定样品的组成,实验步骤
如下:
Ⅰ.制备 CuO
用图 1 所示装置将溶液混合后,小火加热至蓝色沉淀变黑色生成 CuO,
煮沸 5~10 min。稍冷却后全部转移至图 2 装置过滤,并用蒸馏水洗
涤沉淀 2~3 次。
(1)①指出图 2 装置中操作中的错误
,
图 2 操作需用蒸馏水洗涤沉淀 2~3 次,其目的为
。
②检验沉淀洗涤干净的方法为
。
Ⅱ.制备 KHC2O4 和 K2C2O4 混合溶液
称取 3.0 g H2C2O4·2H2O 放入 250 mL 烧杯中,加入 40 mL 蒸馏水,微热
(温度低于 80 ℃)溶解。稍冷后分数次加入 2.2 g 无水 K2CO3,充分反
应后生成含 KHC2O4 和 K2C2O4 的混合物。
(2)该步骤中所得混合物中 n(KHC2O4)∶n(K2C2O4)=
(取整数)。
Ⅲ.制备水合草酸铜酸钾晶体
将 KHC2O4 和 K2C2O4 混合溶液水浴微热,再将 CuO 连同滤纸一起加入该溶
液中,充分反应至 CuO 沉淀全部溶解,取出滤纸后,加热浓缩、冷却结
晶、过滤,用乙醇淋洗,自然晾干,称量得到样品 2.976 0 g(电子天平
称量)。
(3)①步骤Ⅲ中 KHC2O4 的作用是
。
②用乙醇淋洗而不用水的优点是
。
③溶解 CuO 沉淀时,连同滤纸一起加入溶液中的目的是
。
Ⅳ.测定水合草酸铜酸钾晶体的成分
取少量制得的样品配成溶液。用标准酸性高锰酸钾溶液滴定 C2
O4
2
-、
用标准 EDTA 溶液(PAR 为指示剂)滴定 Cu2+,经计算样品中 n(Cu)∶
n(C2
O4
2
-)=1∶2,假设制备样品的过程中 Cu2+无损耗。
(4)水合草酸铜(Ⅱ)酸钾晶体的化学式为
。
参考答案
1.B “柳絮”和棉花的主要成分均为纤维素,A 正确;高级脂肪酸酯
不属于高分子化合物,B 错误;“炎炎”体现了太阳能转化为热能,C 正
确;由“漉鼓以为汁”可知,“漉鼓”涉及过滤,D 正确。
2.B 反应①②③④⑤中均有元素化合价的变化,均为氧化还原反应,
而③④⑤中没有离子参加反应,则不属于离子反应,A 错误;⑤为铝热
反应,Al 失去电子,为还原剂,Mn 为还原产物,则还原性:Al>Mn,B 正确;
由 6H2O2~3O2~6e-、2KClO3~3O2~12e-知,生成等量的 O2,反应③和④
转移的电子数之比为 1∶2,C 错误;反应①为
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,锰元素的化合价降低,氯元素的化
合价升高,4 mol HCl 中只有 2 mol HCl 作还原剂,则氧化剂与还原剂
的物质的量之比为 1∶2,D 错误。
3.B FeCl2 中 Fe 元素是+2 价,FeCl3 中 Fe 元素是+3 价,则相同质量或
等物质的量的 Fe 完全转化为 FeCl2 和 FeCl3 时转移的电子数之比为 2∶
3,肯定不相等,故 A 错误;苯和乙炔的最简式相同,均为 CH,所含碳元
素的质量分数也相同,则质量相同的苯和乙炔所含的碳原子的数目一
定相等,故 B 正确;HCl 是共价化合物,HCl 气体中不含 Cl-,盐酸中含有
Cl-,则所含 Cl-的数目肯定不相等,故 C 错误;相同物质的量浓度的
NH4Cl 和(NH4)2Fe(SO4)2 溶液,如果不考虑 N
H4
+
水解,后者溶液中 N
H4
+
浓
度是前者的2倍,事实上两溶液中N
H4
+
水解程度不同,且(NH4)2Fe(SO4)2
溶液中 Fe2+的水解能抑制 N
H4
+
水解,则两溶液中 N
H4
+
的浓度肯定不相
等,故 D 错误。
4.C A.“84”消毒液(有效成分为 NaClO)中加入少量白醋可增强消
毒效果,更利于生成 HClO:ClO-+ CH3COOH HClO + CH3COO-,正确;B.
用 Na2CO3 将水垢中的 CaSO4 转化为易于除去的 CaCO3,利用难溶物的溶
解平衡原理:CaSO4 +
CO3
2
- CaCO3 +
SO4
2
-,正确;C.稀硫酸酸化的淀粉
KI 溶液在空气中放置一段时间后变蓝:2I- + O2+ 4H+ I2+ 2H2O,不
正确;D.用 Na2S2O3 做碘量法实验时,溶液 pH 不可太低,易发生反应出
现浑浊:S2
O3
2
-+ 2H+ SO2 + S↓ + H2O,正确。
5.B 导管插入碳酸钠溶液液面以下会引起倒吸,故 A 错误;二氧化碳
与氯化钙溶液不能直接反应,溶有氨气后溶液显碱性可以更好的吸收
二氧化碳,生成碳酸根,从而生成碳酸钙,故 B 正确;高温条件下碳酸
钠可以和瓷坩埚中二氧化硅发生反应,不能用瓷坩埚熔融碳酸钠,故 C
错误;NaOH 溶液呈碱性,不能使用酸式滴定管,故 D 错误。
6.A R 原子最外层电子数为其次外层电子数的 3 倍,R 原子只能有 2
个电子层,最外层电子数为 6,则 R 为 O 元素;Y、Z、R、T 位于同周期,
即处于第二周期,T 元素无正价,则 T 为 F 元素;X、Z 位于同主族,X 为
Ca 元素,则 Z 为 Be 元素;Y 为金属元素,则 Y 为 Li;X 为 Ca 元素,则由
X 与 R 原子序数之和是 W 的 2 倍,则(20+8)÷2=14,推出 W 为 Si 元素,
符合题意,据此解答。
A.XR2、WR2 两化合物 CaO2、SiO2,CaO2 为离子晶体,SiO2 为共价晶体,故
错误;B.Y 为锂元素、Z 为铍元素、R 为氧元素、T 为氟元素,位于同周
期,元素的原子半径从左向右逐渐在减小,即原子半径:Y>Z>R>T,故正
确;C.X 为钙元素、Z 为铍元素,金属性:Ca>Be,则最高价氧化物对应的
水化物碱性:氢氧化钙>氢氧化铍,故正确;D.W 为硅元素、R 为氧元素、
T 为氟元素,非金属性:F>O>Si,则气态氢化物的稳定性:W105),因此反应不趋于完全,故D错误。
16.解析:“溶浸”时,SiO2 不溶于稀硫酸,通过过滤除去,所得溶液含
H+、Mn2+、Fe2+、Cu2+、S
O4
2
-等离子;“溶浸”所得溶液通过“除铁”将
Fe3+转化为 Fe(OH)3 沉淀,然后过滤除去;“除铁”后所得溶液通过“净
化”将 Ca2+、Cu2+转化为 CaF2、CuS 沉淀,然后过滤除去;“净化”所得
溶液主要含 Mn2+、N
H4
+
、S
O4
2
-,通过“沉锰”得到 MnCO3,再经过滤、洗
涤、烘干获得无水 MnCO3,据此解答。
(1)将矿石研磨粉碎,可以增大反应物的接触面积,从而提高浸取速
率,A 不满足题意;连续搅拌可以增大反应物的接触面积,从而提高浸
取速率,B 不满足题意;延长浸取时间不能提高浸取速率,C 满足题意;
升高温度可以加快反应速率,从而提高浸取速率,D 不满足题意;增大
反应物的浓度,可以加快反应速率,从而提高浸取速率,E 不满足题意;
由题图可知,温度高于 90 ℃,副产物 MnS2O6 的百分率低且随温度升高
百分率几乎不再变化。
(2)软锰矿的主要成分为 MnO2,具有较强的氧化性,将“溶浸”所得的
Fe2+氧化为 Fe3+,发生反应的离子方程式为
MnO2+2Fe2++4H+ 2Fe3++Mn2++2H2O。
(3)Ksp(CaF2)=c(Ca2+)×c2(F-),所以 c(Ca2+)
=
�sp
(
CaF2
)
�2
(
F
-) =
1
.
5×10
-
10
0
.
022
mol·L-1=3.75×10-7mol·L-1。
(4)“沉锰”时加入 NH4HCO3 后有无色无味的气体放出,根据元素守恒
可知该气体为 CO2,所以“沉锰”发生反应的离子方程式为 Mn2++
2HC
O3
- MnCO3↓+ CO2↑+ H2O。
(5)MnCO3 难溶于水和乙醇,潮湿时易被空气氧化,且乙醇易挥发,洗涤
后更容易干燥,所以应用乙醇洗涤,乙醇化学式为 C2H6O,整个流程来
看,N
H4
+
、S
O4
2
-未除去,所以过滤出 MnCO3 沉淀后废液的主要成分为
(NH4)2SO4。
(6)由题图可知,电解质溶液中的阴离子向左边电极移动,左边电极为
阳极,A 为电源的正极,B 为电源的负极,结合电荷守恒可得 Mn2+发生副
反应的电极反应式为 Mn2++2H2O-2e- MnO2+4H+。
答案:(1)C 90 ℃ (2)MnO2+2Fe2++4H+ 2Fe3++Mn2++2H2O
(3)3.75×10-7 mol·L-1 (4)Mn2+ + 2HC
O3
- MnCO3 ↓+ CO2↑+ H2O
(5)C2H6O
(NH4)2SO4 (6)负 Mn2++2H2O-2e- MnO2+4H+
17.解析:(1)Ge 是 32 号元素,基态 Ge 原子核外电子排布式为
[Ar]3d104s24p2,所以价电子排布图为 ;Ge 原子的电子发
生跃迁时会吸收或发出不同的光,可用光谱分析仪获得线状光谱。
(2)①Na2GeO3 中锗原子的价层电子对数为 3+
4+2
-
2×3
2
=3,所以杂化方式
为 sp2;
②GenH2n+2 与甲烷类似,所以分子中的共价键均为σ键,n 个 Ge 原子之
间形成(n-1)个σ键,与 2n+2 个 H 原子形成(2n+2)个σ键,则 1 个分子
中σ键的个数为(2n+2)+(n-1)=3n+1,所以 1 mol GenH2n+2 中含有的σ键
的数目为(3n+1)NA。
(3)①该物质由 EMIM+和[AlCl4]-构成,所以属于离子晶体;
②EMIM+的组成元素为 H、C、N,非金属性越强电负性越大,非金属
性:H107.3°。
(5)以顶面面心的 Se 原子为例,该晶胞中有 2 个 Zn 距离 Se 原子最近
且距离相等,而在该晶胞的上方的晶胞中还有两个同样的 Zn 原子,所
以 Se 原子的配位数为 4;A 点坐标为(0,0,0),B 点坐标为(
�
2
,a,
�
2
),所以
A 为原点,各坐标轴的方向为 ,根据俯视图可知 D 点的 x、y 坐
标参数为
3�
4
、
�
4
,根据晶胞结构示意图可知 z 坐标参数为
3�
4
,所以 D 点坐
标为(
3�
4
,
�
4
,
3�
4
);晶胞的边长为 a pm,则晶胞的体积 V=a3
pm3=(a×10-10)3cm3;根据均摊法可知一个晶胞中 Zn 原子的个数为 4,Se
原子个数为 4,所以晶胞的质量 m=(
65+79
)
×4
�A
g,所以晶胞的密度ρ
=
�
�
=
(
65+79
)
×4
�A g(
�×10
-
10
)
3
cm
3
,解得 NA=
4×144
��
3
×1030
答案:(1) 线状 (2)①sp2 ②(3n+1)NA (3)①离子晶
体 ②HvⅡ;
(3)①由图可知,当
�
(催化剂)
�
(
HCl
) 相同时,温度越高 HCl 平衡转化率越小,说
明该反应是放热反应,升高温度,平衡逆向移动,K 值减小,则 K360>K400;
②一定温度下随着
�
(催化剂)
�
(
HCl
) 增大,通过催化剂的混合气体中 HCl 和 O2
量变小,N2 的量变大,相当于反应物和生成物的浓度同时变小相同倍
数,根据浓度商 Qc=
�
(
H2O
)
�
(
Cl2
)
�2
(
HCl
)
�
1
2
(
O2
)
,若各物质浓度变小相同倍数时,会使 Qc
大于 K,此时平衡逆向移动,HCl 的平衡转化率减小。
答案:(1)2HCl(g)+
1
2
O2(g) H2O(g)+Cl2(g) ΔH=ΔH1+ΔH2+ΔH3
(2)①
1
2
c1V1×10-3 ②0.56 ③
1
2 400
④>
(3)①> ②减小 随着
�
(催化剂)
�
(
HCl
) 增大,N2 含量增大,HCl(g)、O2(g)、
H2O(g)和 Cl2(g)的浓度均使反应体系的浓度商 Q>K,平衡逆向移
动,HCl 的平衡转化率减小
19.解析:根据合成路线可知,A 与 C3H5O2Cl 发生取代反应生成 B,B 与
C2H5OH 发生酯化反应并成环得到 C,C 与 CH3NHCH2COOH 反应生成 D,D 经
过反应④得到 E,E 与 CNCH2COOC2H5 反应得到 F 和 HCl,据此分析解答问
题。
(1)A 的结构简式为 ,分子中含有的官能团有氟原子、氨基和
羧基。
(2)根据上述分析可知,A 与 C3H5O2Cl 发生取代反应生成 B,B 的结构简
式为 ,逆推可得 C3H5O2Cl 的结构式为 。
(3)反应①为 A 与 C3H5O2Cl 发生取代反应生成 B,反应②为 B 与 C2H5OH
发生酯化反应并成环得到 C,两者都是取代反应。
(4)化合物 D 的结构式为 ,根据各原子的成键原理,可知其分
子式为 C10H9N2O2F。
(5)E 与 CNCH2COOC2H5 反应得到 F 和 HCl,反应方程式为
。
(6) 是 F 的同分异构体,则 X 为—C4H7O2,又 X 部分含—COOH 且
没有支链,则 X 有—CH2CH2CH2COOH、—CH2CH(COOH)CH3、—
CH(COOH)CH2CH3 3 种结构,即满足条件的同分异构体有 3 种。
(7)结合题干信息,制备 时,可先将两个甘氨酸
(HOOCCH2NH2)分子间脱水缩合得到 , 再与 POCl3 反应得到
, 与 CNCH2COOC2H5 反应制得 ,合成路线为
HOOCCH2NH2 。
答案:(1)氨基 羧基 (2) (3)取代反应
(4)C10H9N2O2F
(5)
(6)3
(7)HOOCCH2NH2
20.解析:本实验的目的是制备少量水合草酸铜酸钾并测定样品的组
成;首先利用硫酸铜和氢氧化钠溶液制取氢氧化铜沉淀,加热使其分
解得到 CuO;然后 H2C2O4·2H2O 和无水 K2CO3 制备 KHC2O4 和 K2C2O4 混合溶
液;然后将 KHC2O4 和 K2C2O4 混合溶液水浴微热,再将 CuO 连同滤纸一起
加入该溶液中,充分反应,经系列操作得到样品;最后测定水合草酸铜
酸钾晶体的成分。
(1)①图 2 装置中操作中的错误为过滤时转移固液混合物没有通过玻
璃棒引流;为除去沉淀表面吸附的可溶性杂质离子,需要用蒸馏水洗
涤沉淀 2~3 次。
②得到的 CuO 固体表面可能附着有硫酸钠,可以通过检验硫酸根来确
定沉淀是否洗涤干净,具体方法为取少量最后一次洗涤流出液于试管
中,滴入 BaCl2 溶液,若无白色沉淀生成,则已经洗涤干净。
(2)3.0 g H2C2O4·2H2O 的物质的量为
3
.
0 g
126 g
/
mol
≈0.023 8 mol,2.2 g 无
水 K2CO3 的物质的量为
2
.
2 g
138 g
/
mol
≈0.015 9 mol,则根据碳元素守恒可
得:n(KHC2O4)+n(K2C2O4)=0.023 8 mol,根据 K 元素守恒可得
n(KHC2O4)+2n(K2C2O4)=(0.0159×2) mol,联立解得 n(KHC2O4)=0.015 8
mol,n(K2C2O4)=0.008 0 mol,所以 n(KHC2O4)∶n(K2C2O4)≈2∶1。
(3)①KHC2O4 可以电离出氢离子,加快 CuO 的溶解;
②用乙醇淋洗可以减少水合草酸铜酸钾的溶解损耗,同时乙醇易挥发
可以加快晶体表面水分挥发;
③滤纸上附着有 CuO,连同滤纸一起加入溶液中可以减少 CuO 的损耗。
(4)已知样品中 n(Cu)∶n(C2
O4
2
-)=1∶2,所以 y=2,根据电荷守恒可知
x=2,所以根据 n(K2C2O4)=0.008 0 mol,可知
n{K2[Cu(C2O4)2]·zH2O}=0.008 0 mol,样品质量为 2.976 0 g,所以有
2
.
976 0 g(
39×2+64+12×4+16×8+18�
)
g
/
mol
=0.008 0 mol,解得 z=3,所以水合草酸铜
(Ⅱ)酸钾晶体的化学式为 K2[Cu(C2O4)2]·
3H2O。
答案:(1)①过滤时转移固液混合物没有通过玻璃棒引流 除去沉淀
表面吸附的可溶性杂质离子 ②取少量最后一次洗涤流出液于试管
中,滴入 BaCl2 溶液,若无白色沉淀生成,则已经洗涤干净
(2)2∶1
(3)①加快 CuO 的溶解(或酸性环境促进 CuO 的溶解)
②减少水合草酸铜酸钾的溶解损耗,加快晶体表面水分挥发 ③减少
CuO 的损耗
(4)K2[Cu(C2O4)2]·3H2O