【化学】甘肃省兰州市第一中学2019-2020学年高一4月月考试题(解析版)
甘肃省兰州市第一中学2019-2020学年高一4月月考试题
说明:本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分。考试时间100分钟。答案写在答题卡上,交卷时只交答题卡。
可能用到的相对原子量:H-1 C-12 N-14 O-16 Na-23 Fe-56 Cu-64
第I卷(共40分)
一、单选题(1-10每小题1分,11-25每小题2分)
1.下列反应中,既属于氧化还原反应同时又是吸热反应的是( )
A. Ba(OH)2•8H2O与NH4Cl反应 B. 灼热的碳与高温水蒸气的反应
C. 铝与稀盐酸 D. H2与O2的燃烧反应
【答案】B
【解析】A.Ba(OH)2·8H2O与NH4Cl反应为吸热反应,但该反应中各元素的化合价没有发生变化,故A不选;B.灼热的碳与高温水蒸气的反应为吸热反应,反应中C、H元素化合价变化,属于氧化还原反应,故B选;C.铝与盐酸的反应属于放热反应,故C不选;D.H2与O2的燃烧反应属于放热反应,故D不选;故选B。
2.下列关于化学观或化学研究方法的叙述中,错误的是( )
A. 在化工生产中应遵循“绿色化学”的思想
B. 在过渡元素中寻找优良的催化剂
C. 在元素周期表的金属和非金属分界线附近寻找半导体材料
D. 根据元素周期律,由HClO4可以类推出氟元素的最高价氧化物的水化物为HFO4
【答案】D
【解析】
【详解】A.化工生产主要考虑原料的利用率和减少污染性物质的排放,遵循“绿色化学”的思想,故A正确;
B.制取催化剂的元素位于周期表第ⅢB至ⅡB族之间,属于过渡金属元素,故B正确;
C.在元素周期表的金属和非金属分界线附近的元素既有金属性也有非金属性,常用于制备半导体材料,故C正确;
D.F无正价,不能形成含氧酸,故D错误;
故答案为D。
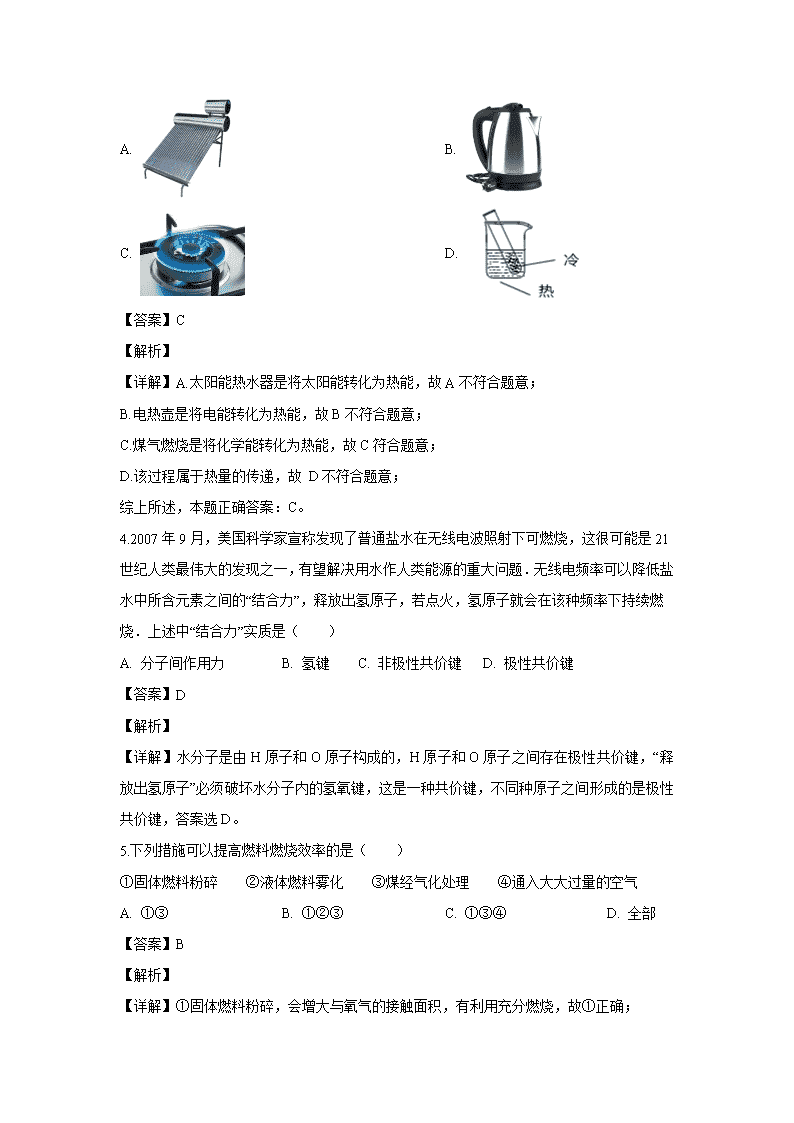
3.使用下列装置给液体升温时,将化学能转化为热能的是( )
A. B.
C. D.
【答案】C
【解析】
【详解】A.太阳能热水器是将太阳能转化为热能,故A不符合题意;
B.电热壶是将电能转化为热能,故B不符合题意;
C.煤气燃烧是将化学能转化为热能,故C符合题意;
D.该过程属于热量的传递,故 D不符合题意;
综上所述,本题正确答案:C。
4.2007年9月,美国科学家宣称发现了普通盐水在无线电波照射下可燃烧,这很可能是21世纪人类最伟大的发现之一,有望解决用水作人类能源的重大问题.无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该种频率下持续燃烧.上述中“结合力”实质是( )
A. 分子间作用力 B. 氢键 C. 非极性共价键 D. 极性共价键
【答案】D
【解析】
【详解】水分子是由H原子和O原子构成的,H原子和O原子之间存在极性共价键,“释放出氢原子”必须破坏水分子内的氢氧键,这是一种共价键,不同种原子之间形成的是极性共价键,答案选D。
5.下列措施可以提高燃料燃烧效率的是( )
①固体燃料粉碎 ②液体燃料雾化 ③煤经气化处理 ④通入大大过量的空气
A. ①③ B. ①②③ C. ①③④ D. 全部
【答案】B
【解析】
【详解】①固体燃料粉碎,会增大与氧气的接触面积,有利用充分燃烧,故①正确;
②液体燃料雾化,会增大与氧气的接触面积,有利用充分燃烧,故②正确;
③煤经气化处理,燃烧会增大与氧气的接触面积,有利用充分燃烧,故③正确;
④通入大大过量的空气,会带走热量,使燃烧效率减低,故④错误;
正确的有①②③,答案选B。
6.下列说法正确的是( )
A. 、、三种核素的化学性质都不相同
B. 16O2、18O2彼此是同位素
C. 14N、14C两种核素的中子数相同,质子数不同
D. 白磷与红磷是磷元素的两种同素异形体
【答案】D
【解析】
【详解】A. 、、三种核素的核外电子排布相同,化学性质相同,A错误;
B. 16O2、18O2均表示氧气分子,B错误;
C. 14N、14C两种核素的中子数分别是14-7=7、14-6=8,质子数分别是7和6,C错误;
D. 白磷与红磷是磷元素的两种单质,互为同素异形体,D正确,
答案选D。
7.下列说法正确的是( )
A. 共价化合物中可能含有离子键
B. 离子化合物中只含有离子键
C. 区别离子化合物和共价化合物的方法是看其水溶液是否能够导电
D. 离子化合物熔融状态能电离出自由移动的离子,而共价化合物熔融状态不能电离出自由移动的离子
【答案】D
【解析】A. 共价化合物中只有共价键,不可能含有离子键,A错误;B. 离子化合物中一定有离子键,也可能含有共价键,如氯化铵、氢氧化钠等等,B不正确; C. 区别离子化合物和共价化合物的方法是看其在熔融状态下是否能够导电,离子化合物和部分共价化合物在水溶液中能发生电离,所以C不正确; D. 离子化合物熔融状态能电离出自由移动的离子,而共价化合物熔融状态不能电离出自由移动的离子,D正确。本题选D。
8.现将下列物质分别装入有水的锥形瓶里(见下图),立即塞紧带 U 形管的塞子, 发现 U
形管内滴有红墨水的水面如图所示状态,判断加入的物质不可能是( )
A. NaOH 固体 B. 浓硫酸 C. 晶体 D. CaO固体
【答案】C
【解析】
【详解】A.NaOH溶于水放热,锥形瓶内压强增大,将U形管中的红墨水向右压,使U形管中液面左低右高,A正确;
B.浓H2SO4溶于水放热,锥形瓶内压强增大,将U形管中的红墨水向右压,使U形管中液面左低右高,B正确;
C.NH4NO3溶于水吸热,锥形瓶内压强减小,大气压将U形管中的红墨水向左压,使U形管中液面左高右低,C错误;
D.CaO与水反应放热,锥形瓶内压强增大,将U形管中的红墨水向右压,使U形管中液面左低右高,D正确。
答案选C。
9. 随着碱金属、卤素原子半径的增大,下列递变规律正确的是( )
A. 碱金属和卤素单质的熔沸点都逐渐降低
B. 碱金属和卤素单质的密度都依次变大
C. 卤素的气态氢化物稳定性逐渐增强
D. 碱金属单质还原性逐渐增强
【答案】D
【解析】
【分析】
【详解】A. 碱金属熔沸点逐渐降低,卤素单质的熔沸点都逐渐升高,A错误;
B. 碱金属和卤素单质的密度呈增大的趋势,有的元素有反常,B错误;
C. 随着卤素原子半径的增大,非金属性逐渐减弱,卤素的气态氢化物稳定性逐渐减弱,C错误;
D. 随着碱金属原子半径的增大,金属性增强,金属单质的还原性逐渐增强,D正确;
答案选D。
10.2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(37Rb)同周期。下列说法不正确的是( )
A. In是第五周期第ⅢA族元素
B. 11549In的中子数与电子数的差值为17
C. 原子半径:In>Al
D. 碱性:In(OH)3>RbOH
【答案】D
【解析】
【分析】
A.根据原子核外电子排布规则,该原子结构示意图为,据此判断该元素在周期表中的位置;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数,原子的质子数=电子数;
C.同主族元素的原子,从上到下,电子层数逐渐增多,半径逐渐增大;
D.同周期元素,核电荷数越大,金属性越越弱,最高价氧化物对应水化物的碱性越弱;
【详解】A.根据原子核外电子排布规则,该原子结构示意图为,因此In位于元素周期表第五周期第IIIA族,故A不符合题意;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数,因此该原子的质子数=电子数=49,中子数为115-49=66,所以中子数与电子数之差为66-49=17,故B不符合题意;
C.Al位于元素周期表的三周期IIIA族,In位于元素周期表第五周期IIIA族,同主族元素的原子,从上到下,电子层数逐渐增多,半径逐渐增大,因此原子半径In>Al,故C不符合题意;
D.In位于元素周期表第五周期,铷(Rb)位于元素周期表第五周期第IA族,同周期元素,核电荷数越大,金属性越越弱,最高价氧化物对应水化物的碱性越弱,因此碱性:In(OH)3<RbOH,故D符合题意;
综上所述,本题应选D。
11.下列关于元素金属性和非金属性强弱比较的说法不正确的是( )
A. 将大理石加入稀盐酸中,能产生CO2气体,说明Cl的非金属性强于C
B. Si与H2化合所需温度远高于S与H2化合的温度,说明S的非金属性强于硅
C. Na与冷水能发生反应,而Mg与冷水反应缓慢,说明Na的金属性强于Mg
D. 石灰乳能溶于盐酸,Be(OH)2与盐酸和NaOH都能反应,说明Ca的金属性强于Be
【答案】A
【解析】
【详解】A.C、Cl非金属性的判断可通过比较它们最高价氧化物的水合物的酸性:酸性越强其非金属性越强,而盐酸是无氧酸,所以不能判断C、Cl非金属性的强弱,故A错误;
B.Si、S处于同周期,非金属性:S>Si,所以Si与H2化合的难易程度小于S与H2化合,即Si与H2化合所需温度远高于S与H2化合的温度,故B正确;
C.Na、Mg处于同周期,金属性:Na>Mg,所以Na与水反应速率大于Mg与水反应,故C正确;
D.石灰乳能溶于盐酸,Be(OH)2与盐酸和NaOH都能反应,说明石灰乳主要成分Ca(OH)2是碱、Be(OH)2显两性,即Ca的金属性强于Be,故D正确;
故选A。
12.化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆 开)1mol 化学键时释放(或吸收)的能量。已知白磷和的分子结构如下图所示,现提供以下化学键的键能(kJ/mol):P—P:198,P—O:360,O=O:498,则对于反应 表述正确的是 ( )
A. 放出1638 kJ 的热量 B. 吸收1638 kJ 的热量
C. 放出126 kJ 的热量 D. 吸收126 kJ 的热量
【答案】A
【解析】
【详解】由图可知:1个白磷分子含6个P-P键,1个含12个P-O键,1个O2分子含1个O=O,那么,1mol白磷参与上述反应时,旧键断裂吸收的能量=6×198kJ+3×498kJ=2682kJ,新键形成放出的能量=12×360kJ=4320kJ,故反应放出(4320-2682)kJ能量,即放出1638kJ能量,A符合。
答案选A。
13.反应A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为( )
①v(A)=0.15mol·L-1·s-1
②v(B)=0.6mol·L-1·s-1
③v(C)=0.4mol·L-1·s-1
④v(D)=0.45mol·L-1·s-1
该反应进行的快慢顺序为( )
A. ②>④>③>① B. ④>②=③>①
C ②=③>①>④ D. ②>③=④>①
【答案】B
【解析】
【详解】在同一化学反应中,用不同的物质表示化学反应速率其数值之比等于化学计量数之比,即;可知反应速率与化学计量数的比值越大,反应速率越快,则①,②,③,④,则④>②=③>①,B符合题意;
答案选B。
14.反应A+B→C((放热)分两步进行:①A+B→X(吸热)②X→C(放热),下列示意图中能正确表示总反应过程中能量进变化的是( )
A. B.
C. D.
【答案】D
【解析】
【详解】A+B→C为放热反应,则A+B的总能量大于生成C的总能量,排除A、 B选项,A+B→X(吸热),则X的能量大于A+B的总能量,X→C(放热),则X的能量大于C的总能量,排除C选项;
答案选D
15.a,b,c,d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层的电子数相同;c所在周期数与族数相同;d与a同族。下列叙述正确的是( )
A. 4种元素中b的金属性最强 B. 原子半径:d>c>b>a
C. c的氧化物的水化物是强碱 D. d单质的氧化性比a单质的氧化性强
【答案】A
【解析】
【分析】a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层的电子数相同,则a的核外电子总数应为8,所以a为O元素,则b、c、d为第三周期元素,c所在周期数与族数相同,则c为Al元素,d与a同族,则d为S元素,b可能为Na或Mg,结合元素化合物的性质及元素周期律进一步解答即可。
【详解】由上述分析可知:a为O元素、b为Na或Mg元素、c为Al元素、d为S元素。
A项,同周期元素从左到右元素的金属性减弱,则金属性b>c,又因为a、d为非金属,所以4种元素中b的金属性最强,故A正确;B项,同周期元素从左到右原子半径逐渐减小,应为b>c>d,同主族元素从上到下原子半径逐渐增大,所以a
r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示的变化,其中A为X、Y组成的双原子分子,B和C均为10电子分子。下列说法不正确的是( )
A. X元素位于第VIA族 B. A不能溶于B中
C. A是典型的酸性氧化物 D. B的沸点高于C的沸点
【答案】C
【解析】
【分析】X、Y、Z三种短周期主族元素,B和C均为10电子分子,应该为氢化物,由转化关系可知,Z为H,Y、Z位于第二周期;X、Y、Z原子序数之和为16,则X、Y的原子序数之和为15,原子半径Y>X,若Y为C元素,X为F,若Y为N,X为O,由转化关系可知,单质X、Y反应生成A,A为X、Y组成的双原子分子,则A为NO,结合原子半径可知,Y为N、X为O元素,X单质与Z单质反应生成的B为H2O,Y单质与Z单质反应生成的C为NH3。则X为O、Y为N、Z为H,A为NO、B为H2O、C为NH3。
【详解】A.由分析可知,A为O,原子序数为8,位于第VIA族,A正确;
B.A为NO、B为H2O,NO难溶于水,B正确;
C.A是不成盐氧化物,非酸性氧化物,C错误;
D. B为H2O,常温下是液体,C为NH3,常温下是气体,故B的沸点高于C的沸点,D正确;
答案选C。
18.美国科学家用某有机分子和球形笼状分子C60制成了“纳米车”(如图所示),每辆“纳米车”是由一个有机分子和4个C60分子构成。“纳米车”可以用来运输单个的有机分子。下列说法正确的是( )
A. 人们用肉眼可以清晰看到“纳米车”的运动
B. “纳米车”诞生说明人类操纵分子的技术进入了一个新阶段
C. C60是一种新型的化合物
D. C60与12C是同位素
【答案】B
【解析】A、因纳米车很小,我们不能直接用肉眼清晰地看到这种“纳米车”的运动,选项A错误;
B、“纳米车”的诞生,说明人类操纵分子的技术进入一个新阶段,选项B正确;C、由不同种元素形成的纯净物是化合物,C60是一种单质,选项C错误;D、质子数相同,中子数不同的同一种元素的不同核素互称为同位素,C60是单质,不是核素,选项D错误。答案选B。
19.已知R2-的核内有n个中子,R原子的质量数为M,则mg R2-中含有电子的物质的量为( )
A. mol B. mol
C. mol D. mol
【答案】D
【解析】
【详解】由R2-的核内有n个中子,R的质量数为M,则质子数为M-n,故R2-阴离子的核外电子数为M-n+2,mg R2-的物质的量mol,所以mgR2-阴离子含有的电子的物质的量为mol×(M-n+2)=mol,故选D。
20.镁—次氯酸盐电池的工作原理如图,该电池反应为:Mg+ClO-+H2O=Mg(OH)2+Cl-。下列有关说法正确的是( )
A. 电池工作时,正极a附近的pH将不断增大
B. 电池工作时,c溶液中的溶质是MgCl2
C. 负极反应式:ClO-+2e-+H2O=Cl-+2OH-
D. a电极发生还原反应,每转移0.2mol电子,理论上生成0.2molCl-
【答案】A
【解析】
【分析】根据电池的装置示意图和电池反应分析可知,ClO-→Cl-,化合价降低,得电子,根据原电池的工作原理,a极为正极,b极为负极,正极反应式为ClO-+H2O+2e-=Cl-+2OH-,负极反应式为Mg+2OH--2e-=Mg(OH)2,据此分析解答。
【详解】A.根据上述分析可知,正极a为正极,电极反应式为ClO-+H2O+2e-=Cl-+2OH-,因此正极a附近的pH将不断增大,A选项正确;
B.根据分析可知,Mg失电子生成Mg(OH)2,则c溶液中的溶质不是MgCl2,B选项错误;
C.b极为负极,电极反应式为Mg+2OH--2e-=Mg(OH)2,C选项错误;
D.根据a电极的电极反应式ClO-+H2O+2e-=Cl-+2OH-可知,每转移0.2mol电子,理论上生成0.1molCl-,D选项错误;
答案选A。
21.下列有关元素周期表的结构叙述正确的是( )
A. 元素周期表有七个横行,代表七个周期;有18个纵行,代表18个族
B. 元素周期表中同周期ⅡA、ⅣA元素的原子序数之差可能为2、12、26
C. 元素周期表中包含元素数目最多的是第一列
D. 元素周期表中某些元素不可能既位于同一周期,又位于同一族
【答案】B
【解析】
【详解】A.元素周期表有七个横行,代表七个周期;有18个纵行,七个主族,七个副族,一个第Ⅷ族,一个零族共16个族,故A错误;
B.由于元素周期表中中间部分是过渡元素,则同周期第ⅡA族与第ⅣA族元素的原子序数差值是2或12或26,故B正确;
C.元素周期表中包含元素数目最多的是ⅢB(含有镧系和錒系),为第三列,故C错误;
D.元素周期表中镧系、锕系各有15种元素分别为第六、七周期的ⅢB,故D错误;
答案为B。
22.如图所示是部分短周期元素原子半径与原子序数的关系,则下列说法正确的是( )
A. Z、N两种元素形成的化合物熔融状态下可以导电
B. X、N两种元素的气态氢化物的沸点相比,前者较低
C. Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液中
D. 由X与M两种元素组成的化合物能与水反应
【答案】C
【解析】
【分析】同周期自左而右原子半径减小,同主族自上而下原子半径增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为氧元素,Y为Na元素,Z为Al元素,M为Si元素,N为Cl元素,据此分析作答。
【详解】根据上述分析可知,
A.Z、N两种元素的离子分别为Al3+、Cl-
,最外层电子数相同,电子层越多离子半径越大,故离子半径Al3+<Cl-,故A错误;
B.X为O元素,N为Cl元素,H2O分子间存在氢键,所以沸点较高,故沸点性H2O>HCl,故B错误;
C.氧化铝是两性氧化物,能与氢氧化钠反应生成偏铝酸钠,能与盐酸反应生成氯化铝,故C正确;
D.由X与M两种元素组成的化合物是SiO2,能与强碱反应,能与氢氟酸反应,但不与反应,故D错误;
故选C。
23.把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。①a、b相连时,a为负极;②c、d相连时,电流方向为由d到c;③a、c相连时,a极质量减轻;④b、d相连时,b上有大量气泡产生。则四种金属的活动性强弱顺序为( )
A. B.
C. D.
【答案】B
【解析】
【详解】根据原电池原理,一般负极金属的活动性比正极金属的活动性强;电子流动方向是由负极流向正极,电流方向与电子流动方向相反;由此可对金属活动性强弱作出如下判断:①,②c>d,③,④,则金属活动性强弱顺序为,故答案选B。
24.硫代硫酸钠溶液与稀硫酸反应的化学方程式为: Na2S2O3+ H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是( )
实验
反应温度/℃
Na2S2O3溶液
稀H2SO4
H2O
V/mL
c/(mol·L-1)
V/mL
c/(mol·L-1)
V/mL
A
25
5
0.1
10
0.1
5
B
25
5
0.2
5
0.2
10
C
35
5
0.1
10
0.1
5
D
35
5
0.2
5
0.2
10
【答案】D
【解析】
【详解】“最先出现浑浊”,即反应速率最快;A项与B项温度相同、H2SO4浓度相同,B项中Na2S2O3的浓度比A项大,反应速率:B项>A项;C项与D项温度相同、H2SO4浓度相同,D项中Na2S2O3的浓度比C项大,反应速率:D项>C项;B项与D项Na2S2O3、H2SO4浓度都相同,D项温度高于B项,反应速率:D项>B项;则反应最快的是D项,D项最先出现浑浊,答案选D。
25.在恒温、恒容的密闭容器中进行反应A(g)+B(g)=C(g),若反应物A浓度从2mol·L-1降到0.8mol·L-1需20s,则反应物A的浓度由0.8mol·L-1降到0.2mol·L-1所需的反应时间( )
A. 等于10s B. 大于10s
C. 小于10s D. 无法判断
【答案】B
【解析】
【详解】反应物A浓度从2mol·L-1降到0.8mol·L-1需20s,该时间段内△c(A)=1.2mol/L,反应物A的浓度由0.8mol·L-1降到0.2mol·L-1,△c(A)=0.6mol/L,若该时段内反应速率与前一段时间内相同,则所需时间为10s,但由于反应进行A的浓度降低,反应速率变慢,所以由0.8mol·L-1降到0.2mol·L-1所需时间要大于10s,故答案为B。
第II卷(非选择题,共60分)
26.根据下列提供的一组物质回答问题:
①NH4Cl ②MgCl2 ③H2S ④Na2O2 ⑤MgO ⑥Cl2 ⑦NaOH ⑧H2O2 ⑨NH3 ⑩CO2
(1)既有极性共价键又有非极性共价键的是__(用序号表示)。
(2)既有离子键又有共价键的是__(用序号表示)。
(3)共价化合物有___(用序号表示)。
(4)CO2的电子式___;Na2O2的电子式__。
(5)用电子式表示MgCl2的形成过程:___。
【答案】(1). ⑧ (2). ①④⑦ (3). ③⑧⑨⑩ (4). (5). (6).
【解析】
【分析】①NH4Cl中和Cl-形成离子键,为离子化合物;
②MgCl2中Mg2+和Cl-形成离子键,为离子化合物;
③H2S分子中H原子和S原子形成极性共价键,为共价化合物;
④Na2O2中Na+和形成离子键,中O原子和O原子形成非极性共价键,为离子化合物;
⑤MgO中Mg2+和O2-形成离子键,为离子化合物;
⑥Cl2中Cl原子和Cl原子形成非极性共价键;
⑦NaOH中Na+和OH-形成离子键,OH-中O原子和H原子形成极性共价键,为离子化合物;
⑧H2O2中H原子和O原子形成极性共价键,O原子和O原子形成非极性共价键,为共价化合物;
⑨NH3中N原子和H原子形成极性共价键,为共价化合物;
⑩CO2中C原子和O原子形成极性共价键,为共价化合物;
据此分析解答问题。
【详解】(1)根据上述分析可知,既有极性共价键又有非极性共价键的是H2O2,故答案为:⑧;
(2)既含有离子键又有共价键的是NH4Cl、Na2O2、NaOH,故答案为:①④⑦;
(3)共价化合物有H2S、H2O2、NH3、CO2,故答案为:③⑧⑨⑩;
(4)CO2中C原子和O原子形成极性共价键,其电子式为,Na2O2中Na+和形成离子键,中O原子和O原子形成非极性共价键,其电子式为,故答案为:;;
(5) MgCl2中Mg2+和Cl-形成离子键,其形成过程为,故答案为:。
27.1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R电子层数相同,R与Y最外层电子数相同,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同。请回答下列问题:
①W的原子结构示意图__,R离子的电子式__。
②X与Y元素可形成一种常用的消毒剂,其结构式为_。
③Y、Z、W、R形成的简单离子半径由大到小顺序为__(用化学符号表示)。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置__。
②关于铷的下列说法中正确的是__(填序号)。
a.与水反应比钠更剧烈
b.在空气中易吸收水和二氧化碳
cRb2O2与水能剧烈反应并释放出O2
d.单质具有很强的还原性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
①棉花中浸有NaOH溶液的作用是__(用离子方程式表示)
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到__;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是__。
【答案】(1). (2). (3). H-O-O-H (4). S2->O2->Na+>Al3+ (5). 第五周期IA族 (6). abcd (7). Cl2+2OH-=H2O+Cl-+ClO- (8). 出现分层,上层几乎呈无色,下层呈紫红色 (9). 过量的Cl2也会氧化I-生成I2
【解析】
【分析】X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,X为H元素,Y原子最外层电子数是次外层电子数的3倍,Y为O元素,Z、W、R电子层数相同,R与Y最外层电子数相同,R为S元素,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同,Z为Na元素、W为Al元素。
【详解】(1)①W为Al,Al的原子序数为13,其原子结构示意图为;R为S,硫离子带有2个负电荷,其电子式为;
②H、O形成的双氧水具有强氧化性,能够杀菌消毒,双氧水为共价化合物,其结构式为H-O-O-H;
③Y、Z、W、R形成的简单离子分别为O2-、Na+、Al3+、S2-,电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,则离子半径:S2->O2->Na+>Al3+;
(2)①铷是37号元素,原子结构中有5个电子层,最外层电子数为1,则位于第五周期第IA族;
②a.铷排在钠的下方,活泼性强于铷,铷与水反应比钠更剧烈,故a正确;
b.依据氧化钠性质可知,氧化铷为碱性氧化物,在空气中易吸收水生成氢氧化铷和与二氧化碳反应生成碳酸铷,故b正确;
c.依据过氧化钠与水反应生成氢氧化钠和氧气,可知:Rb2O2与水能剧烈反应并释放出O2,故c正确;
d.铷金属性强于钠,所以单质铷有极强的还原性,故d正确;
e.铷金属性强于钠,所以RbOH的碱性比同浓度的NaOH强,故e错误;
综上所述答案为abcd;
(3)①棉花中浸有的NaOH溶液可吸收氯气,防止氯气扩散到空气中,发生的离子反应为Cl2+2OH-=Cl-+ClO-+H2O;
②溴与KI反应生成碘,碘易溶于四氯化碳,充分振荡、静置,可观察到溶液分层,上层几乎无色,下层呈紫红色;由于过量的Cl2也会氧化I-生成I2,所以要控制氯气的加入量。
28.化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解液。放电时总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
①写出放电时负极的电极反应式:__。
②铅蓄电池放电时,溶液的pH将_(填增大、减小或不变);当外电路上有0.5mol电子通过时,溶液中消耗H2SO4的物质的量为__。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为___;若将负极材料改为CH4,写出其负极反应方程式__。
(3)法国格勒诺布尔(Grenoble)约瑟夫﹒傅立叶大学的研究小组发明了第一块可植入人体为人造器官提供电能的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶(蛋白质)的作用下发生反应:C6H12O6+6O26CO2+6H2O(酸性环境)。下列有关该电池的说法正确的是__。
A.该生物燃料电池不能在高温下工作
B.该电池负极的电极反应式为:C6H12O6+6H2O-24e-=6CO2↑+24H+
C.消耗1mol氧气时转移4mol电子,H+向负极移动
D.提高葡萄糖生物燃料电池的效率,可使其在将来为更多可植入医疗设备提供电能
(4)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂—碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中___作正极,负极的电极反应为__。
【答案】(1). Pb-2e-+SO42-=PbSO4 (2). 增大 (3). 0.5mol (4). O2+4e-+2H2O=4OH- (5). CH4-8e-+10OH-=CO32-+7H2O (6). ABD (7). 石墨 (8). Li-e-=Li+
【解析】
【详解】(1) ①铅蓄电池中,负极是铅,失电子发生氧化反应,电极反应式:Pb+SO42--2e- =PbSO4;
②总反应Pb+PbO2+2H2SO4=2PbSO4+2H2O,放电时,消耗硫酸,溶液pH增大;反应转移2mol电子,消耗硫酸2mol,当外电路上有0.5mol电子通过时,溶液中消耗H2SO4的物质的量为0.5mol;
(2) 氢氧燃料电池,正极反应为O2
在碱性介质中的反应,电极反应式为:O2+4e-+2H2O=4OH-;CH4做负极反应时,在碱性介质中生成CO32-,电极反应式为:CH4-8e-+10OH-= CO32-+7H2O;
(3)A.酶是一种蛋白质,在高温下会变性,失去生理活性,所以该生物燃料电池不可以在高温下工作,A正确;
B.葡萄糖生物燃料电池中葡萄糖在负极反应失电子生成二氧化碳,其电极反应式为:C6H12O6+6H2O-24e-=6CO2+24H+,B正确;
C.氧气在正极得电子,其电极方程式为:O2+4e-+4H+=2H2O,消耗1mol氧气则转移4mol e-,在溶液中阳离子向正极移动,所以H+会向正极移动,C错误;
D.提高葡萄糖生物燃料电池的效率,能提高葡萄糖的能量利用率,向外提高较多的电量,D正确。
正确的有ABD;
(4) 由电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,SOCl2得到电子,化合价降低,正极材料为石墨;Li失去电子,化合价升高,做负极,负极的电极反应式为:Li-e-=Li+。
29.(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g)+4NH3(g)5N2(g)+6H2O(g)。
①能说明该反应已达到平衡状态的标志是___。
a.反应速率v(NH3)=v(N2)
b.容器内压强不再随时间而发生变化
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO)∶n(NH3)∶n(N2)∶n(H2O)=6∶4∶5∶6
e.12mol N-H键断裂的同时生成5mol N≡N键
②某次实验中测得容器内NO及N2的物质的量随时间变化如图所示,图中b点对应的速率关系是v(正)___v(逆);d点对应的速率关系是v(正)___v(逆)。(填﹥、﹤或﹦)。
(2)一定条件下,在2L密闭容器内,反应2NO2(g)N2O4(g),n(NO2)随时间变化如下表:
①用N2O4表示0~2s内该反应的平均速率为___。在第5s时,NO2的转化率为___。
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是__。
【答案】(1). bc (2). > (3). = (4). 0.00375mol·L-1·s-1(或0.225mol·L-1·min-1) (5). 87.5% (6). 随着反应的进行,反应物NO2的物质的量浓度减小,因而反应速率减小
【解析】
【详解】(1)①a.该反应达到平衡状态时,5v正(NH3)=4v逆(N2),故a错误;
b.该反应是一个反应前后气体体积增大的可逆反应,容器体积恒定,所以未平衡时压强会发生改变,当压强不再变化时说明反应平衡,故b正确;
c.容器内N2的物质的量分数不再随时间而发生变化说明浓度不在改变,反应达到平衡,故c正确;
d.物质的量之比不能说明正逆反应速率相等或者浓度不变,故d错误;
e.只要反应进行12mol N-H 键断裂的同时就会生成5mol N≡N键,二者均表示正反应速率,故e错误;
故答案为:bc;
②据图可知b点之后氮气的浓度增大,NO的浓度减小,说明此时反应正向进行,及v(正)> v(逆);d点时NO的浓度不再变化,说明反应达到平衡,所以v(正)= v(逆);
(2)①0~2s内v(NO2)==0.0075mol·L-1·s-1,同一反应同一时段内不同物质的反应速率之比等于计量数之比,所以v(N2O4)=0.5v(NO2)=0.00375mol·L-1·s-1;第5s时,二氧化氮的转化率为=87.5%;
②随着反应的进行,反应物NO2的物质的量浓度减小,因而反应速率减小。
30.用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图1所示。
①作负极的物质化学式为___________。
②正极的电极反应式是_________________________________________。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH
pH=2.5
pH=4.5
NO3-的去除率
接近100%
<50%
24小时pH
接近中性
接近中性
铁的最终物质形态
pH=4.5时,NO3-的去除率低。其原因是_____________________________________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率。对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏FeO(OH)氧化层。
①做对比实验,结果如图2所示,可得到的结论是____________________。
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4,该反应的离子方程式为_________,解释加入Fe2+提高NO3-去除率的原因:_____________________________________。
【答案】(1). Fe (2). NO3-+8e-+10H+=NH4++3H2O (3).
FeO(OH)不导电,阻碍电子转移 (4). 本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率 (5). Fe2++2FeO(OH)=Fe3O4+2H+ (6). Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移
【解析】
分析】(1)原电池中负极材料失电子,正极是NO3-得电子生成NH4+;
(2)根据图示pH=4.5生成了较多的FeO(OH),FeO(OH)不导电;
(3)①根据图2可知,只加入Fe2+的水中NO3-的去除率为0,加入Fe2+、Fe的水中NO3-的去除率最高;
②根据得失电子守恒配平Fe2+与FeO(OH)反应生成Fe3O4的离子方程式;
【详解】(1)①原电池中负极材料失电子,根据图1,铁失电子,所以作负极的物质化学式为Fe;
②根据示意图,正极是NO3-得电子生成NH4+,正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O;
(2)根据图示,pH=4.5时,NO3-的去除率低的原因是:pH=4.5生成了较多的FeO(OH),FeO(OH)不导电,阻碍电子转移,所以NO3-的去除率低;
(3)①根据图2可知,只加入Fe2+的水中NO3-的去除率为0,加入Fe2+、Fe的水中NO3-的去除率最高,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率;
②根据得失电子守恒,Fe2+与FeO(OH)反应生成Fe3O4的离子方程式是Fe2++2FeO(OH)=Fe3O4+2H+;加入Fe2+提高NO3-去除率的原因是:Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移,所以加入Fe2+提高NO3-去除率。