- 2021-07-08 发布 |
- 37.5 KB |
- 10页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
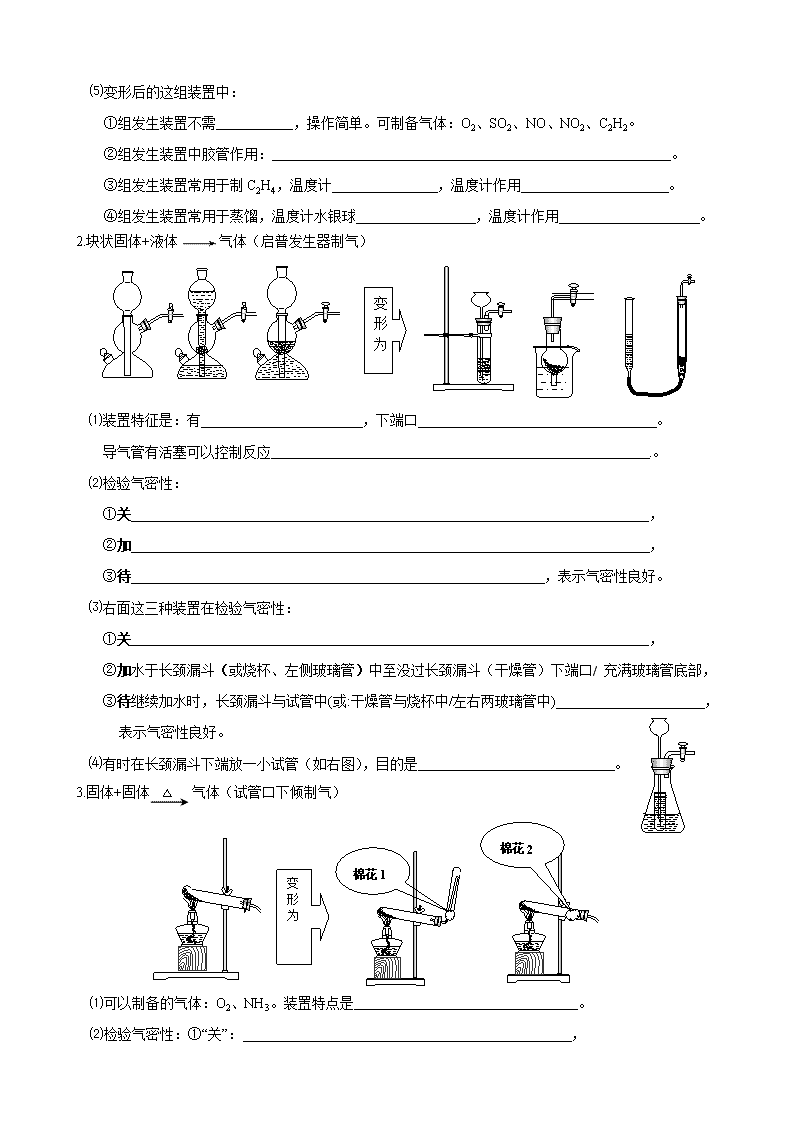
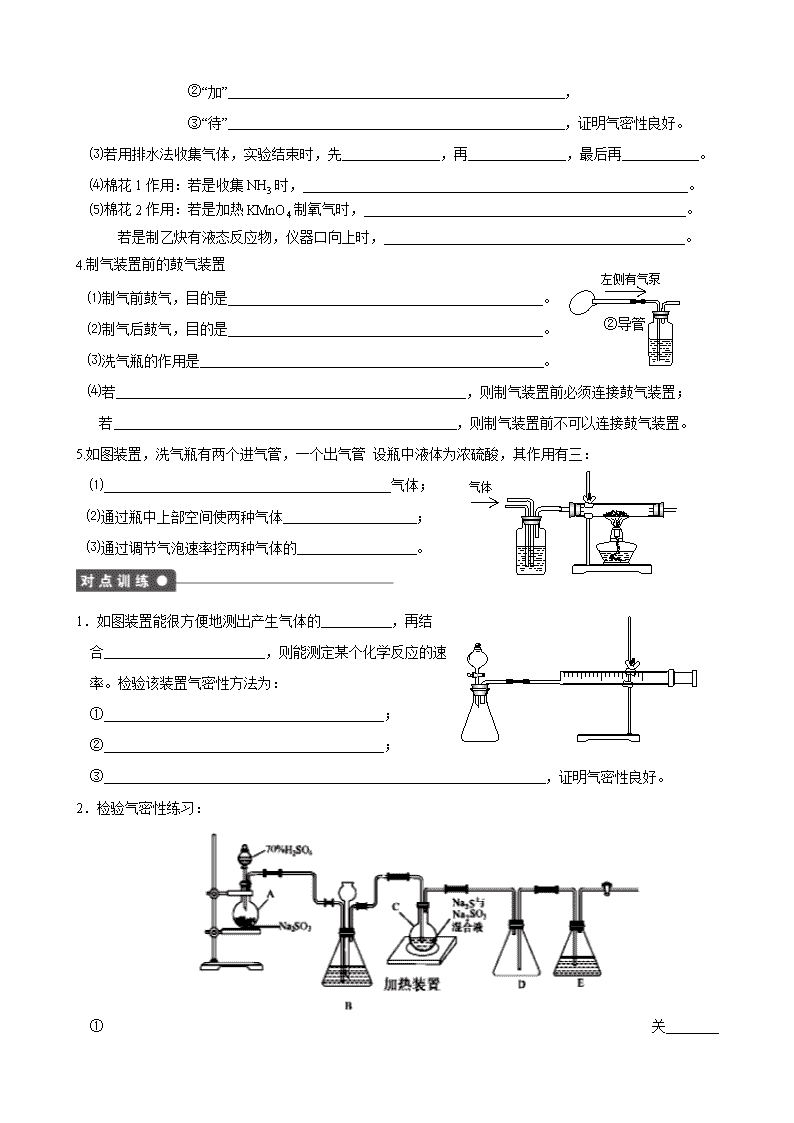
2020届一轮复习人教版气体制备实验学案
第一章 从实验学化学 第一节 化学实验基本方法(3)——气体制备实验 一、总述: 1.制备气体种类:H2 、O2 、CO2 、NH3 、NO 、NO2 、SO2 、Cl2 、HCl 、C2H4 、C2H2 。 2.操作顺序:连 → 检 →装 →开 →收 →拆 。 3.装置顺序(从左到右):(鼓 →)制 →安 →净 →收 →尾 。 ⑴鼓气:考虑问题——制气前通气目的。制气后通气目的。 ⑵制气:考虑问题——三种制气装置类型特点及选择;检验气密性方法。 ⑶安全:考虑问题——防倒吸;防堵塞;临时贮存气体。 ⑷净化:考虑问题——净化装置;净化试剂;净化顺序。 ⑸收集(验证):考虑问题——收集方法;测量体积;测量质量;验证性质。 ⑹尾气处理:考虑问题——防污染;防倒吸;防外界气体进入。 二、制气装置(发生装置) ① ② ④ ③ 变形为 1.固体(液体)+ 液体气体(烧瓶制气) ⑴装置特征是都有 ,分液漏斗的下端口 ,不能 。 可制备气体:O2 、NH3 、NO 、NO2 、SO2 、Cl2 、HCl 、C2H4 、C2H2 。 ⑵检验气密性方法Ⅰ: ①关 , ②加 , ③待 。表示气密性良好。 ⑶加热时烧瓶中液体不多于 ,不少于 。 ⑷有时烧瓶采用液浴加热方式, 低于100℃时常用 ,高于100℃时常用其它 。 液浴加热目的是: 。 ⑸变形后的这组装置中: ①组发生装置不需 ,操作简单。可制备气体:O2、SO2、NO、NO2、C2H2。 ②组发生装置中胶管作用: 。 ③组发生装置常用于制C2H4,温度计 ,温度计作用 。 ④组发生装置常用于蒸馏,温度计水银球 ,温度计作用 。 2.块状固体+液体气体(启普发生器制气) 变形为 ⑴装置特征是:有 ,下端口 。 导气管有活塞可以控制反应 .。 ⑵检验气密性: ①关 , ②加 , ③待 ,表示气密性良好。 ⑶右面这三种装置在检验气密性: ①关 , ②加水于长颈漏斗(或烧杯、左侧玻璃管)中至没过长颈漏斗(干燥管)下端口/ 充满玻璃管底部, ③待继续加水时,长颈漏斗与试管中(或:干燥管与烧杯中/左右两玻璃管中) ,表示气密性良好。 ⑷有时在长颈漏斗下端放一小试管(如右图),目的是 。 3.固体+固体气体(试管口下倾制气) 棉花2 棉花1 变形为 ⑴可以制备的气体:O2、NH3。装置特点是 。 ⑵检验气密性:①“关”: , ②“加” , ③“待” ,证明气密性良好。 ⑶若用排水法收集气体,实验结束时,先 ,再 ,最后再 。 ⑷棉花1作用:若是收集NH3时, 。 ⑸棉花2作用:若是加热KMnO4制氧气时, 。 若是制乙炔有液态反应物,仪器口向上时, 。 ②导管 左侧有气泵 4.制气装置前的鼓气装置 ⑴制气前鼓气,目的是 。 ⑵制气后鼓气,目的是 。 ⑶洗气瓶的作用是 。 ⑷若 ,则制气装置前必须连接鼓气装置; 若 ,则制气装置前不可以连接鼓气装置。 5.如图装置,洗气瓶有两个进气管,一个出气管 设瓶中液体为浓硫酸,其作用有三: 气体 ⑴ 气体; ⑵通过瓶中上部空间使两种气体 ; ⑶通过调节气泡速率控两种气体的 。 1.如图装置能很方便地测出产生气体的 ,再结合 ,则能测定某个化学反应的速率。检验该装置气密性方法为: ① ; ② ; ③ ,证明气密性良好。 2.检验气密性练习: ①关 , ②加 , ③待 ,表示气密性良好。 3.检验气密性练习: A B C D 方法1: ① ; ② ; ③ 。 方法2: ① ; ② ; ③ 。 二.安全装置 1.安全装置之一: ⑴装置特点是 。 其作用是 和 。 ⑵此类装置一般连在 与 之间。 2.安全装置之二: ⑴在前面所述装置的基础上,另有一个长颈漏斗(或长导管连接另一个试剂瓶)。该装置作用有三: 防 ; 防 ; 导管右侧有活塞时, 。 若右侧某处导管堵塞,可观察到现象是: , , 。 ⑵第三个装置,可以除掉气体中的杂质,同时兼起安全瓶作用。 (能/不能)防倒吸。能够防 和 。 三、净化装置 1.液体净化试剂: ⑴洗气瓶中只能装 试剂。 ①盛水,用于吸收 。 ②一些酸式盐溶液,用于吸收较强的酸性气体。如: 除Cl2中的HCl用 ; 除SO2中的HCl用 ; 除CO2中的HCl及SO2用 ; 除H2S中的HCl用 。 ③碱溶液,用于吸收 ,如吸收CO2 、NO2 、SO2 、H2S 、Cl2 、HCl 等气体。 ④浓硫酸,用于 。浓硫酸不能干燥 。 ⑵洗气瓶必须从 管进气 管出气,液体 。 ⑶多种杂质要一一除去时,先除 的气体,后除 的气体,最后除 。 2.固体净化试剂: ⑴干燥管和U形管中只能装 试剂。 ①氯化钙,用于 ,不能干燥 。 ②碱石灰,用于 ;不能干燥 。 ③无水硫酸铜,用于 ,不能 。 ⑵干燥管必须从 口进气 口出气,而U形管进气出气无方向性。 3.需加热除杂的试剂: ⑴加热除杂情况,如盛装 除O2;盛装 除CO、H2等。 ⑵一般连在干燥装置之 ,以确保仪器不炸裂。 四、气体收集装置 1.排液体法: 变形为 ⑴排水法收集的气体有:H2、O2、NO、CH4、C2H2、C2H4 等在水中溶解度 的气体。 ⑵排特殊溶液收集:Cl2 ;SO2 ; CO2 ;H2S 。 ⑶后三个装置除排水收集之外,还有 作用。若测量可溶于水的气体体积,需要 。在正确读数之前,要注意的是: ①恢复 ; ②保持 。 ③读数时要 。 2.向上排气法收集(设气流从左向右): ⑴装置特点是进气管口在 ,出气管口在 。 ⑵可收集 气体。如: 收集Cl2、HCl、SO2、H2S、NO2 等气体。 3.向下排气法收集: 棉花 ⑴装置特点是进气管口在 ,出气管口在 。 ⑵可收集 气体。如: 收集 H2、NH3、CH4等气体。 ⑶管口棉花作用: 。 ⑷验满方法是:(以NH3为例) 。 五、 尾气处理装置 1.液体吸收 ⑴导管直接通入液体中,可用于吸收 气体,如Cl2。 ① (能/不能)防倒吸; ② (能/不能)防止污染空气。 ⑵带安全装置吸收方法。可用于吸收溶解性 的气体。如HCl、NH3。 ①漏斗口 。 ②能防止因 产生的倒吸。 ③能防止因体系 产生的倒吸。 ⑶两层液体吸收方法。用于吸收溶解度 气体,如HCl、NH3。 ①上层为水,下层为CCl4,导管插入 。 ②能防止因 产生的倒吸。 ③不能防止因体系 产生的倒吸。 2.固体吸收 ⑴用固态试剂吸收有污染气体,如碱石灰可吸收 如SO2、HCl、Cl2等。 ⑵若此装置连在尾气吸收之处,可能有两种作用: ① ; ②防止 。 ⑶若有两个干燥管连续使用,其作用是 第一个干燥管 。 第二个干燥管是 。 3.点燃或气球吸收 ⑴导管中尾气通入燃着的酒精灯火焰中, 吸收 气体,如CO。 ⑵一般地用一个空的气球,吸收 气体,然后另行处理。 1.工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行实验。 回答下列问题: (1)制取无水氯化铁的实验中,A中反应的化学方程式为 ,装置B中加入的试剂是 。 (2)制取无水氯化亚铁的实验中,装置A用来制取 。尾气的成分是 。若仍用D装置进行尾气处理,存在的问题是 、 。 (3)若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3常用的试剂是 。欲制得纯净的FeCl2,在实验操作中应先 ,再 。 参考答案 【基础落实】 一、总述: 2. 接装置 验气密性 试剂 始反应 集或验证 除装置 3. 气装置 气装置 全装置 化装置 集(验证)装置 气处理装置 二、制气装置(发生装置) 1.⑴ 分液漏斗 永远悬在液面上 插入液面下 ⑵闭分液漏斗活塞 ,将导管末端口浸没水中 热烧瓶,导管末端有气泡 停止加热后,导管末端有一段 稳定的高于液面的水柱 ⑶容积的2/3 容积的1/3 ⑷水浴加热 油浴加热 受热均匀,便于控制温度 ⑸①加热 ②平衡分液漏斗上下气压,促使分液漏斗中液体顺利流下 ③水银球插入反应物液面下 测反应混合物温度 ④与蒸馏烧瓶与支管口平行 蒸馏出气体温度 2. ⑴长颈漏斗(或者相当于长颈漏斗的装置) 插入液面下形成液封 随时开始,也能随时停止 ⑵闭导管处活塞 水于长颈漏斗中至浸没下端口 继续加水时,长颈漏斗与启普发生器中有一段稳定的液面差 ⑶闭导气管处活塞 有一段稳定的液面差 ⑷防止部分气体从长颈漏斗逸出 3.⑴ 试管口略下倾 ⑵将导管末端口浸没水中(关闭出气口) 加热试管,导管口有气泡产生 待停止加热后,导管末端有一段 稳定的水柱 ⑶取出集气瓶 撤出导气管 熄灭酒精灯 ⑷减缓气体对流速度,使收集的气体更纯净 ⑸防止KMnO4粉末进入导管而使导管发生堵塞 防止实验中产生的泡沫涌入导管发生堵塞 4.⑴通入××排净体系中空气 ⑵把装置中产生的××气体全部排出 ⑶除去空气中的某种成分(如CO2、H2O),防止它进入装置 ⑷实验中欲测产生气体的质量 实验中欲测生成气体的体积 5. 干燥 充分混合 比例关系 【对点训练】 1.体积 一个计时设备 关闭分液漏斗活塞 将注射器活塞向外拉出一段距离 待一段时间后松手,活塞能回复到原位置 2.闭分液漏斗活塞 , 关闭导管处活塞 水于长颈漏斗中至浸没下端口 继续加水,长颈漏斗与锥形瓶中有一段稳定的液面差 3.关闭分液漏斗活塞,向B、D中加水浸没导管口,打开活塞K 加热A中的圆底烧瓶,D中导管有气泡冒出 待停止加热,关闭活塞K后,D中导管有一段稳定的水柱,B中长颈漏斗口会产生稳定的气泡 关闭K,关闭分液漏斗活塞,把D导管口放入水中 向B中长颈漏斗中加水,若长颈漏斗与B中产生稳定的液面差,表明K前面的装置气密性良好 加热C,若D处出现气泡,停止微热,D处导管产生一段稳定的水柱,表明这部分气密性良好 【基础落实】 二.安全装置 1.⑴进气管口和出气管口位置都较高 防止倒吸 保证气流平稳 ⑵制气装置 净化装置 2. ⑴防倒吸 右侧导管堵塞产生危险 临时贮存气体 瓶中液面下降,漏斗中液面上升 ⑵导管堵塞产生危险 临时贮存气体 不能 三、净化装置 1. ⑴液态 HCl或NH3 饱和NaCl 饱和NaHSO3 饱和NaHCO3 饱和NaHS 酸性气体 吸收H2O(干燥气体) NH3 、H2S 、HI 、HBr ⑵长 短 不能充得太满 ⑶酸性强 酸性弱 水蒸气 2. ⑴固态 除去水蒸气 NH3 除去酸性气体和水蒸气 酸性气体 检验水蒸气 除去水蒸气(干燥气体) ⑵大 小 3. ⑴灼热Cu 灼热CuO ⑵后 四、气体收集装置 1. ⑴很小 ⑵饱和NaCl 饱和NaHSO3 饱和NaHCO3 饱和NaHS ⑶测量气体体积 在水面上加一层植物油 ①体系至常温 ②量筒和水槽 /(试剂瓶和量筒)/(干燥管和滴定管)中液面水平 ③平视液面,使凹液面最低处与刻度线相切 2. 下 上 比空气重且不与空气反应 3.⑴上 下 ⑵比空气轻且不与空气反应 ⑶减缓气体扩散速度 使收集的气体更纯净 ⑷用玻璃棒沾小块红色石蕊试纸靠近导管口,试纸变蓝 五、 尾气处理装置 1. ⑴溶解性不大的气体 不能 能 ⑵很大 刚刚接触液面,不能插入液面太深 溶解度大或反应 温度变化 ⑶很大的 下层液体中 溶解度大或反应 温度变化 2. ⑴酸性气体 ⑵吸收反应产生的气体 ,防止污染空气 空气中CO2或H2O进入装置 ⑶用于吸收并测出生成气体质量 防止空气中CO2或H2O进入装置 3. 可燃的有毒 有毒 【对点训练】 1.(1) MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O , 浓硫酸 。 (2)HCl 。HCl和H2 。发生倒吸 、可燃性气体H2不能被吸收 。 (3) KSCN溶液 。点燃A处的酒精灯 ,点燃C处的酒精灯 。查看更多