【化学】福建省莆田第一中学2020届高三10月月考
福建省莆田第一中学2020届高三10月月考
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27 S-32 Mg-24 Fe-56 Cu-64 Ba-137
第I卷(选择题)
一、 选择题(每小题2分,共46分;每小题只有一个选项符合题意)
1.下面的“诗”情“化”意,分析正确的是( )
A.“粉身碎骨浑不怕,要留清白在人间”只发生了物理变化
B.“日照澄州江雾开”中伴有丁达尔效应
C.“试玉要烧三日满,辨才须待七年期”中“玉”成分是硅酸盐,该句诗表明玉的硬度很大
D.“绿蚁新醅酒,红泥小火炉”,“新醅酒”即新酿的酒,在酿酒过程中,葡萄糖发生了水解反应
2.化学与生产、生活、社会、环境密切相关,下列说法中正确的是( )
①铝制容器不能盛放酸性或碱性食品,但可长期盛放腌制食品
②共享单车利用太阳能发电完成卫星定位,有利于节能环保
③向氢氧化铁胶体中滴加稀硫酸,开始有沉淀生成,而后会溶解
④明矾净水的原理和“84”消毒液消毒的原理相同
⑤“天宫二号”空间实验室的太阳能电池板的主要材料是二氧化硅
⑥补铁剂与维生素C共同服用可提高补铁效果
A.①③⑤ B.②③⑤ C.②③⑥ D.④⑤⑥
3.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.标准状况下,2.24 L己烷中共价键数目为1.9NA
B.2 L 0.5 mol/L亚硫酸溶液中含有的H+数为2NA
C.高温下,16.8 g Fe与足量的水蒸气完全反应转移的电子数为0.8NA
D.在密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA
4.从物质分类的角度进行下列判断,正确的是( )
A.根据是否具有丁达尔效应,可将分散系分为溶液、浊液和胶体
B.SiO2既能与NaOH溶液反应,又能与氢氟酸反应,所以SiO2属于两性氧化物
C.AgCl的水溶液不易导电,但AgCl是强电解质
D.烧碱、纯碱、熟石灰均属于碱
5.下列指定反应的离子方程式正确的是( )
A.硫化亚铁与稀硝酸混合反应:2H+ +FeS=H2S↑+ Fe2+
B.酸化NaIO3和NaI的混合溶液,滴入几滴淀粉溶液变蓝色:5I− +IO3− +6H + =3I2+3H2O
C.Ba(OH)2与等物质的量 NaHSO4混合:Ba2+ +2OH−+2H+ +SO42-= BaSO4↓+2H2O
D.电解饱和食盐水:2Cl− +2H + = Cl2↑+ H2↑
6.2019年8月1日我国自主设计研制、具有国际主流水准的104架国产大型客机C919在上海浦东机场完成首次飞行实验。新材料的应用是C919的一大亮点,C919客机首次大范围采用的合金是( )
A.铝锂合金 B.铜锌合金 C.不锈钢 D.铝镁合金
7.同温同体积同质量的CO2、CO、H2、O2的压强,按从大到小的顺序排列正确的是( )
A.H2>O2>CO>CO2 B.CO2>O2>CO>H2
C.H2>CO>O2>CO2 D.CO2>H2>O2>CO
8.下图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
A.a通入NH3,然后b通入CO2,c中放碱石灰
B.b通入NH3,然后a通入CO2,c中放蘸稀硫酸的脱脂棉
C.a通入CO2,然后b通入NH3,c中放碱石灰
D.a通入NH3,然后b入CO2,c中放蘸稀硫酸的脱脂棉
9.在标准状况下,容积为1 L的密闭容器中刚好可以盛放a个N 2 分子和b个O 2 分子组成的混合气体,则阿伏加德罗常数的近似值可以表示为( )
A.22.4(a + b) B.22.4(a + b)/(6.02×1023)
C.a + b D.22.4(a + b)×6.02×1023
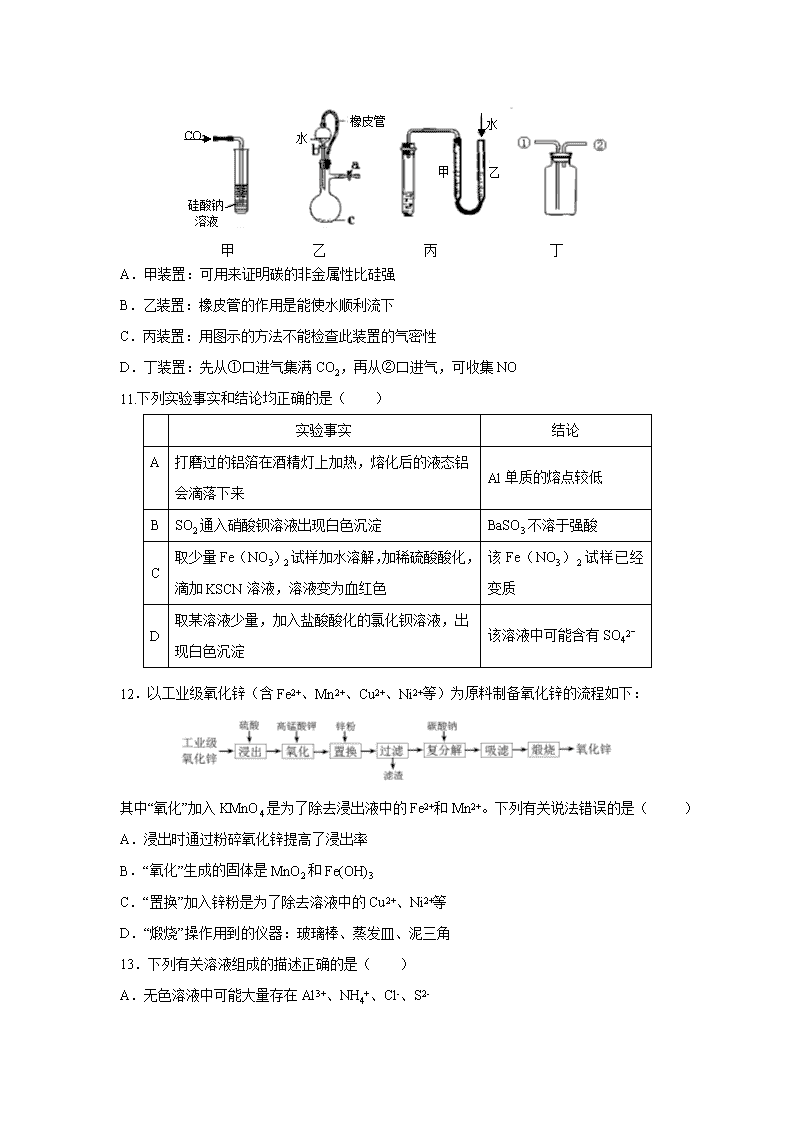
10.某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中说法不正确的是( )
CO2
硅酸钠
溶液
水
橡皮管
水
甲
乙
甲 乙 丙 丁
A.甲装置:可用来证明碳的非金属性比硅强
B.乙装置:橡皮管的作用是能使水顺利流下
C.丙装置:用图示的方法不能检查此装置的气密性
D.丁装置:先从①口进气集满CO2,再从②口进气,可收集NO
11.下列实验事实和结论均正确的是( )
实验事实
结论
A
打磨过的铝箔在酒精灯上加热,熔化后的液态铝会滴落下来
Al单质的熔点较低
B
SO2通入硝酸钡溶液出现白色沉淀
BaSO3不溶于强酸
C
取少量Fe(NO3)2试样加水溶解,加稀硫酸酸化,滴加KSCN溶液,溶液变为血红色
该Fe(NO3)2试样已经变质
D
取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀
该溶液中可能含有SO42﹣
12.以工业级氧化锌(含Fe2+、Mn2+、Cu2+、Ni2+等)为原料制备氧化锌的流程如下:
其中“氧化”加入KMnO4是为了除去浸出液中的Fe2+和Mn2+。下列有关说法错误的是( )
A.浸出时通过粉碎氧化锌提高了浸出率
B.“氧化”生成的固体是MnO2和Fe(OH)3
C.“置换”加入锌粉是为了除去溶液中的Cu2+、Ni2+等
D.“煅烧”操作用到的仪器:玻璃棒、蒸发皿、泥三角
13.下列有关溶液组成的描述正确的是( )
A.无色溶液中可能大量存在Al3+、NH4+、Cl-、S2-
B.酸性溶液中可能大量存在Na+、ClO-、SO42-、I-
C.弱碱性溶液中可能大量存在 Na+、K+、Cl-、HCO3-
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO42-
14.某含铬(Cr2O72-)废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀经干燥后得到n mol FeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是( )
A.消耗硫酸亚铁铵的物质的量为n(2-x) mol
B.处理废水中Cr2O72-的物质的量为 (nx)/2 mol
C.反应中发生转移的电子数为3nx mol
D.在FeO·FeyCrxO3中,3x=y
15.甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后生成的气体的体积比为甲∶乙=1∶2,则加入铝粉的质量为( )
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
16.将打磨后的镁条放入盛有50ml蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图。下列有关描述正确的( )
A.该实验是在常温下进行的
B.实线表示溶液浊度随时间的变化
C.50s时向溶液中滴入酚酞试液,溶液变红
D.该反应温度下饱和Mg(OH)2溶液的pH约为10
17.将15.2 g铜和镁组成的混合物加入250mL 4.0mol • L-1 的稀硝酸中,固体完全溶解。若生成的气体只有NO,向所得溶液中加入1.0LNaOH溶液,此时金属离子恰好沉淀完全,沉淀质量为25.4g,下列说法不正确的是( )
A.原固体混合物中,Cu和Mg的物质的量之比为2:1
B.氢氧化钠溶液的浓度为0.8mol·L-1
C.固体溶解后的溶液中硝酸的物质的量为0.1 mol
D.生成的NO气体在标况下的体积为4.48 L
18.A、B是短周期元素m、n组成的常见二元化合物(原子序数m
T>L
23.常温下,用0.1 mol·L-1MgSO4和0.05 mol·L-1Al2(SO4)3溶液进行实验:①各取25 mL,分别滴加0.5 mol·L-1NaOH溶液,测得溶液的pH与V(NaOH)的关系如图1所示;②将两种溶液等体积混合后,取出25 mL,逐滴加入上述NaOH溶液,观察现象。下列判断正确的是( )
A.图1中的曲线II表示MgSO4与NaOH反应的关系
B.根据图1可得Ksp[Al(OH)3]的值大于1.0×10-32
C.实验②中,Al(OH)3完全溶解前溶液中c(Mg2+)/c(Al3+)逐渐变大
D.图2可以表示实验②中n(沉淀)与V(NaOH)的关系
第Ⅱ卷 非选择题(共54分)
24.(12分)磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:________________。AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为________。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
CuSO4+PH3+H2O=Cu3P↓+H3PO4+H2SO4
(3)工业制备PH3的流程如图所示。
①次磷酸属于________元酸。
②白磷和烧碱溶液反应的化学方程式为:__________________________________________。
③若起始时有1 mol P4参加反应,则整个工业流程中共生成________mol PH3。(不考虑产物的损失)
25.(11分)人体血液里Ca2+的浓度一般采用mg·cm-3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用酸性KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
I.配制酸性KMnO4标准溶液:下图是配制50 mL酸性KMnO4标准溶液的过程示意图。
(1)请你观察图示并判断其中不正确的操作有 (填序号)。
(2)其中确定50 mL溶液体积的容器是 (填名称)。
(3)如果按照图示的操作配制溶液,在其他操作均正确的情况下,配制溶液的浓度将
(填“偏大”或“偏小”)。
II.测定血液样品中Ca2+的浓度:取血液样品20.00 mL,经过上述处理后得到草酸,再用0.020 mol·L-1酸性 KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL酸性KMnO4溶液。
(4)请写出草酸与酸性KMnO4溶液反应的离子方程式 。
(5)滴定时,根据现象 ,即可确定反应达到终点。
(6) 经过计算,血液样品中Ca2+的浓度为 mg·cm-3。
26.
(16分)硒(Se)和铜(Cu)在生产生活中有广泛的应用。硒可以用作光敏材料、电解锰行业的催化剂,也是动物体必需的营养元素和对植物有益的营养元素等。氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下所示:
请回答下列问题:
(1)若步骤①中得到的氧化产物只有一种,则它的化学式是____________。
(2)写出步骤③中主要反应的离子方程式:____________________________________。
(3)步骤⑤包括用pH=2的溶液酸洗、水洗两步操作,酸洗采用的酸是__________(写酸的名称)。
(4)上述工艺中,步骤⑥和⑦的作用是 。
(5)Se为ⅥA族元素,用乙二胺四乙酸铜阴离子水溶液和硒代硫酸钠(Na2SeSO3)溶液反应可获得纳米硒化铜,硒代硫酸钠还可用于Se的精制,写出硒代硫酸钠(Na2SeSO3)与H2SO4溶液反应得到精硒的化学方程式:____________________________________。
(6)氯化亚铜产率与温度、溶液pH关系如下图所示。据图分析,流程化生产氯化亚铜的过程中,温度过低影响CuCl产率的原因是____________________________________;温度过高、pH过大也会影响CuCl产率的原因是_______________________________。
(7)用NaHS作污水处理的沉淀剂,可以处理工业废水中的Cu2+。已知:25℃时,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15,CuS的溶度积为Ksp(CuS)=6.3×10-36。
反应Cu2+(aq)+HS-(aq) CuS(s)+H+(aq)的平衡常数K=__________(结果保留1位小数)。
27.(15分)草酸(乙二酸)存在于自然界的植物中,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,175℃时分解。
Ⅰ.用硝酸氧化法制备草酸晶体并测定其纯度,制备装置如图所示(加热、固定等装置略去)。
实验步骤如下
①糖化:先将淀粉水解为葡萄糖;
②氧化:在淀粉水解液中加入混酸(质量之比为3:2的65%HNO3与98%H2SO4的混合物),在55~60℃下水浴加热发生反应;
③结晶、蒸发、干燥:反应后溶液经冷却、减压过滤,即得草酸晶体粗产品。
(1)装混酸的仪器名称为________;步骤②中,水浴加热的优点为 。
(2)“②氧化”时发生的主要反应如下,完成下列化学方程式:
___C6H12O6 + ___HNO3 ___H2C2O4 + 9NO2↑ + 3NO↑+ ______
(3)称取m g草酸晶体粗产品,配成100 mL溶液。取20.00 mL于锥形瓶中,用a moL·L-1KMnO4标准液标定,只发生5H2C2O4 + 2MnO4- + 6H+ = 2Mn2+ + 10CO2↑ + 8H2O反应,消耗KMnO4标准液体积为VmL,则所得草酸晶体(H2C2O4·2H2O)的纯度为___________。
Ⅱ.证明草酸晶体分解得到的产物
(4) 甲同学选择上述装置验证产物CO2,装置B的主要作用是__________。
(5)乙同学认为草酸晶体分解的产物中除了CO2、H2O应该还有CO,为进行验证,选用甲同学实验中的装置A、B和如图所示的部分装置(可以重复选用)进行实验。
①乙同学的实验装置中,依次连接的合理顺序为A、B、_____________。其中装置H反应管中盛有的物质是________________________。
②能证明草酸晶体分解产物中有CO的现象是_____________________。
【参考答案】
1~23(共46分,每小题2分)
1
2
3
4
5
6
7
8
9
10
11
12
B
C
C
C
B
A
C
D
A
C
D
D
13
14
15
16
17
18
19
20
21
22
23
C
A
A
D
C
B
A
B
C
B
C
24.(共12分,每空2分)
(1)第3周期第VA族 Al(OH)3
(2)24 ,11,12 ,8, 3,24
(3)①一 ② P4 + 3NaOH + 3H2O = PH3↑+ 3NaH2PO2 ③2.5
25.(共11分,第(1)小题1分,其余每空2分)
(1)②⑤ (2)50 mL容量瓶 (3)偏小
(4)5H2C2O4 + 2MnO4- + 6H+ = 2Mn2+ + 10CO2↑ + 8H2O
(5)当滴入最后一滴酸性高锰酸钾溶液时,溶液恰好由无色变为紫红色,且半分钟内不褪色
(6)1.2
26.(16分,每空2分)
(1)CuSO4 (2)2Cu2++SO+2Cl-+H2O===2CuCl↓+SO+2H+
(3)硫酸 (4)使CuCl干燥,防止其水解氧化
(5)Na2SeSO3+H2SO4===Na2SO4+Se↓+SO2↑+H2O
(6)温度过低反应速率慢
温度过高、pH过大,容易向CuO和Cu2O转化,且温度过高,铵盐(氯化铵,亚硫酸铵)易受热分解(任答一点即可)
(7)1.1×1021
27.(15分,第(1)小题1分,其余每空2分)
(1) 分液漏斗 使受热均匀,便于控制温度。
(2) 1, 12, 3, 9 H2 O
(3)12.6aV/8m×100%或1.575aV/m×100%
(4)使升华的草酸冷凝,避免对CO2检验的干扰。
(5)①FDGHDI CuO
②H中黑色固体变红色,第一个D装置无现象,第 二个D装置出现白色浑浊,即可证明。