高中化学 2_3化学平衡 第3课时练习 新人教版选修4
2.3化学平衡 第3课时练习
1.下列关于某一化学反应的平衡常数的说法中,正确的是( )
A.与该反应的压强有关
B.与反应的温度有关,还与反应本身有关
C.与化学反应本身和温度有关,并且会受到起始浓度的影响
D.只与化学反应本身有关,与其他任何条件无关的一个不变的常数
【解析】 K与反应温度有关,表达式与方程式的书写有关,但与起始浓度、压强无关。
【答案】 B
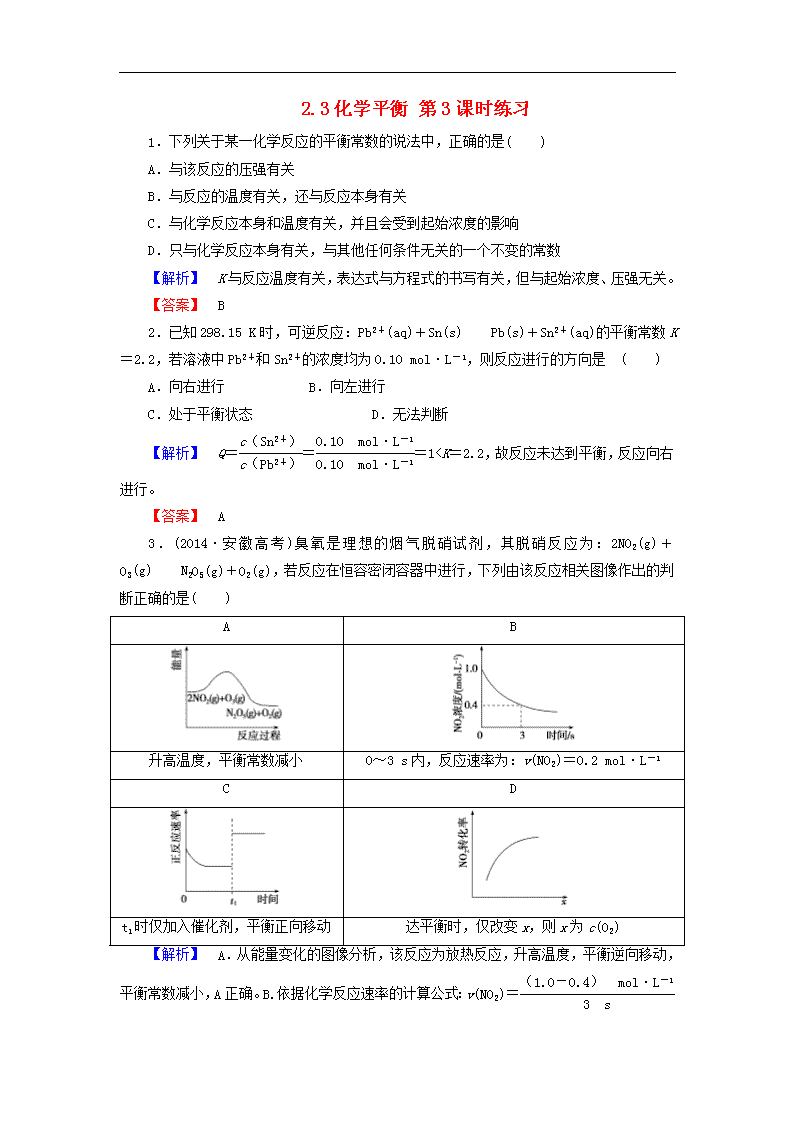
2.已知298.15 K时,可逆反应:Pb2+(aq)+Sn(s)Pb(s)+Sn2+(aq)的平衡常数K=2.2,若溶液中Pb2+和Sn2+的浓度均为0.10 mol·L-1,则反应进行的方向是 ( )
A.向右进行 B.向左进行
C.处于平衡状态 D.无法判断
【解析】 Q===1
”、“<”或“=”)。
若在T1时某状态c(I-)/c(I)=,________平衡状态(填“是”、“不是”或“不一定是”)。
(3)写出该平衡常数的表达式K=________。若升高温度,K值将________(填“增大”、“减小”或“不变”,下同);若向溶液中加入少量的溴水,K值将________。
【解析】 (1)由题意及图象知,I2(aq)+I-I,升高温度,c(I)减小,
平衡向逆反应方向移动,故正反应为放热反应。
(2)在T1、D点时,要达到平衡状态A点,T1不变,c(I)增大,反应向右进行,故v(正)>v(逆)。
K=,而=,但不知c(I2)的大小,故无法确定是否达平衡状态。
(3)K=,升高温度,平衡逆移,故K值减小;若加入少量的溴水,改变了物质的浓度,但K值不变。
【答案】 (1)放热
(2)> 不一定是
(3) 减小 不变
6.(2014·四川高考)在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)M(g)+N(g),所得实验数据如下表:
实验编号
温度/℃
起始时物质的量/mol
平衡时物质的量/mol
n(X)
n(Y)
n(M)
①
700
0.40
0.10
0.090
②
800
0.10
0.40
0.080
③
800
0.20
0.30
a
④
900
0.10
0.15
b
下列说法正确的是( )
A.实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol/(L·min)
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
【解析】 A.根据方程式可知在5 min内反应生成的n(N)等于生成的n(M),则v(N)==1×10-3 mol/(L·min),该项错误;B.根据表格中数据可知平衡时c(X)=0.002 mol/L、c(Y)=0.032 mol/L、c(N)=c(M)=0.008 mol/L,则平衡常数K===1.0,该项错误;C.因该反应在800 ℃时平衡常数为1,
设反应中转化的X的物质的量为x,则有(0.20-x)×(0.30-x)=x·x,故x=0.12 mol,X的转化率为×100%=60%,该项正确;假设在900 ℃时,该反应的平衡常数也为1.0,根据实验④中的数据可知b=0.060 mol,由①中数据可知在700 ℃时平衡常数约为2.6,结合800 ℃时平衡常数为1.0可知,温度越高,该平衡常数越小,平衡逆向移动,故b<0.060,该项错误。
【答案】 C
7.(2014·新课标全国卷Ⅱ)在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1;反应的平衡常数K1为________。
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
a:T________100 ℃(填“大于”或“小于”),判断理由是
__。
b:列式计算温度T时反应的平衡常数K2________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半。平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是__。
【解析】 (1)由题意及图示知,在1.00 L的容器中,通入0.100 mol的N2O4,发生反应:N2O4(g)2NO2(g),随温度升高混合气体的颜色变深,说明反应向生成NO2的方向移动,即向正反应方向移动,所以正反应为吸热反应,即ΔH>0;由图示知60 s时该反应达到平衡,消耗N2O4为0.100 mol·L-1-0.040 mol·L-1=0.060 mol·L-1,根据v=可知:v(N2O4)==0.001 0 mol·L-1·s-1;求平衡常数可利用三段式:
N2O4(g)2NO2(g)
起始量/(mol·L-1) 0.100 0
转化量/(mol·L-1) 0.060 0.120
平衡量/(mol·L-1) 0.040 0.120
K1===0.36 mol·L-1
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)降低,说明平衡N2O4(g)2NO2(g)向正反应方向移动,根据勒夏特列原理,温度升高,向吸热反应方向移动,即向正反应方向移动,故T>100 ℃,由c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡,可知此时消耗N2O4 0.002 0 mol·L-1·s-1×10 s=0.020 mol·L-1,由三段式:
N2O4(g)2NO2(g)
起始量/(mol·L-1) 0.040 0.120
转化量/(mol·L-1) 0.020 0.040
平衡量/(mol·L-1) 0.020 0.160
K2==≈1.3 mol·L-1
(3)温度T时反应达到平衡后,将反应容器的容积减少一半,压强增大,平衡会向气体体积减小的方向移动,该反应逆反应为气体体积减小的反应,故平衡向逆反应方向移动。
【答案】 (1)大于 0.001 0 0.36 mol·L-1
(2)大于 反应正方向吸热,反应向吸热方向进行,故温度升高
平衡时,c(NO2)=0.120 mol·L-1+0.002 0 mol·L-1·s-1×10 s×2=0.160 mol·L-1
c(N2O4)=0.040 mol·L-1-0.002 0 mol·L-1·s-1×10 s=0.020 mol·L-1
K2=≈1.3 mol·L-1
(3)逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动