- 2021-07-07 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2021届高考化学一轮复习化学实验方案的设计、评价及探究实验作业
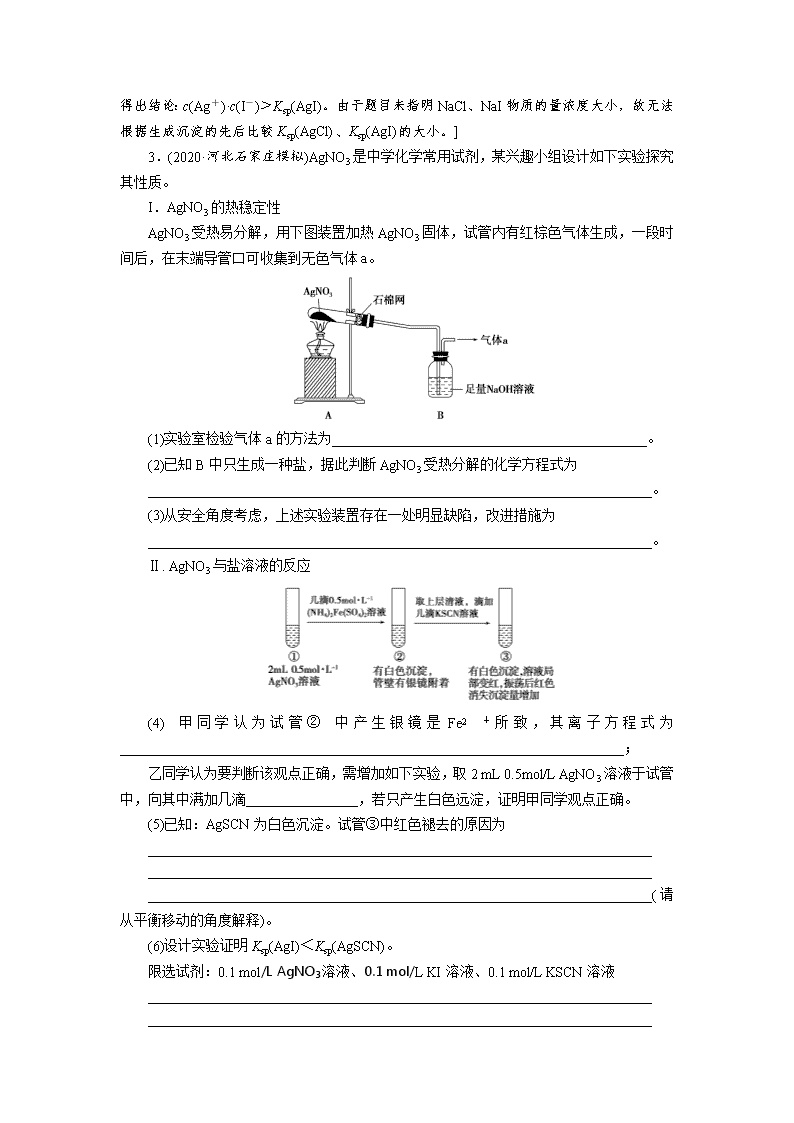
课时作业(四十一) 化学实验方案的设计、评价及探究实验 1.由下列实验及现象推出的相应结论正确的是( ) 实验 现象 结论 A 某溶液中滴加 K3[Fe(CN)6]溶液 产生蓝色沉淀 原溶液中有 Fe2+,无 Fe3 + B 向 C6H5ONa 溶液中通入 CO2 溶液变浑浊 酸性:H2CO3>C6H5OH C 向含有 ZnS 和 Na2S 的悬 浊液中滴加 CuSO4 溶液 生成黑色沉淀 Ksp(CuS)<Ksp(ZnS) D ①某溶液中加入 Ba(NO3)2 溶液 ②再加足量盐酸 ①产生白色沉淀 ②仍有白色沉淀 原溶液中有 SO2- 4 B [B 对:符合较强酸制较弱酸的原理。A 错:可以证明含有 Fe2+,但不能确定是否含 有 Fe3+。C 错:由于 ZnS 难溶而 Na2S 易溶,且浓度未知,向悬浊液中滴加 CuSO4 溶液产生 黑色沉淀,不能比较 ZnS 和 CuS 的 Ksp 大小。D 错:若原溶液中存在 SO2- 3 ,也会产生同样 的现象。] 2.根据下列实验操作和现象所得出的结论正确的是( ) 选项 实验操作和现象 结论 A 向苯酚浊液中滴加 Na2CO3 溶液,浊液变 清 苯酚的酸性强于 H2CO3 的酸性 B 向碘水中加入等体积 CCl4,振荡后静置, 上层接近无色,下层显紫红色 I2 在 CCl4 中的溶解度大于在水中的溶解 度 C 向 CuSO4 溶液中加入铁粉,有红色固体 析出 Fe2+的氧化性强于 Cu2+的氧化性 D 向 NaCl、NaI 的混合稀溶液中滴入少量 稀 AgNO3 溶液,有黄色沉淀生成 Ksp(AgCl)>Ksp(AgI) B [B 对:向碘水中加入等体积 CCl4,振荡后静置,上层接近无色,下层显紫红色, 由于 CCl4 的密度大于水,则下层是有机层,从而得出结论:I2 在 CCl4 中的溶解度大于在水 中的溶解度。A 错:苯酚与 Na2CO3 溶液反应生成苯酚钠和 NaHCO3,故实验的结论应是苯 酚的酸性强于 HCO- 3 。C 错:向 CuSO4 溶液中加入铁粉,有红色固体析出,发生反应:Cu2 ++Fe===Fe2++Cu,Cu2+是氧化剂,Fe2+是氧化产物,则氧化性:Cu2+>Fe2+。D 错:向 NaCl、NaI 的混合稀溶液中滴入少量稀 AgNO3 溶液,有黄色沉淀生成,说明生成 AgI 沉淀, 得出结论:c(Ag+)·c(I-)>Ksp(AgI)。由于题目未指明 NaCl、NaI 物质的量浓度大小,故无法 根据生成沉淀的先后比较 Ksp(AgCl)、Ksp(AgI)的大小。] 3.(2020·河北石家庄模拟)AgNO3 是中学化学常用试剂,某兴趣小组设计如下实验探究 其性质。 I.AgNO3 的热稳定性 AgNO3 受热易分解,用下图装置加热 AgNO3 固体,试管内有红棕色气体生成,一段时 间后,在末端导管口可收集到无色气体 a。 (1)实验室检验气体 a 的方法为_____________________________________________。 (2)已知 B 中只生成一种盐,据此判断 AgNO3 受热分解的化学方程式为 ________________________________________________________________________。 (3)从安全角度考虑,上述实验装置存在一处明显缺陷,改进措施为 ________________________________________________________________________。 Ⅱ. AgNO3 与盐溶液的反应 (4) 甲 同 学 认 为 试 管 ② 中 产 生 银 镜 是 Fe2 + 所 致 , 其 离 子 方 程 式 为 ________________________________________________________________________; 乙同学认为要判断该观点正确,需增加如下实验,取 2 mL 0.5mol/L AgNO3 溶液于试管 中,向其中满加几滴________________,若只产生白色远淀,证明甲同学观点正确。 (5)已知:AgSCN 为白色沉淀。试管③中红色褪去的原因为 ________________________________________________________________________ ________________________________________________________________________ ________________________________________________________________________( 请 从平衡移动的角度解释)。 (6)设计实验证明 Ksp(AgI)<Ksp(AgSCN)。 限选试剂:0.1 mol/L AgNO3 溶液、0.1 mol/L KI 溶液、0.1 mol/L KSCN 溶液 ________________________________________________________________________ ________________________________________________________________________ ________________________________________________________________________。 解析 (1)根据实验,加热硝酸银,有红棕色气体产生,说明产生 NO2,通过装置 B 后, 在末端导管口可收集到无色气体,无色气体可能为氧气,检验氧气的方法是将带火星的木条 放至导管口,木条复燃;(2)NO2 与 NaOH 反应:2NO2+2NaOH===NaNO2+NaNO3+H2O, 氧气能把 NaNO2 氧化成 NaNO3,根据信息,B 中只生成一种盐,说明氧气过量,根据得失 电子数目守恒,Ag 的化合价降低,推断出硝酸银受热分解的方程式为:2AgNO3===== △ 2Ag +2NO2↑+O2↑;(3)NO2 能与 NaOH 发生反应,容易造成导管内的气体压强减小,容易引 起倒吸,因此 A、B 装置之间连接一个防倒吸的安全瓶;(4)Ag+的氧化性比 Fe3+强,因此发 生 Ag++Fe2+===Fe3++Ag;根据②的实验现象以及若只产生白色沉淀,证明甲同学观点正 确,推出所加溶液为 0.5mol·L-1(NH4)2SO4;(5)溶液中发生 Fe3++3SCN- Fe(SCN)3 使局 部变红;振荡试管时,过量的 Ag+与 SCN-反应生成 AgSCN 沉淀,降低了 c(SCN-),平衡 逆向移动,溶液褪色;(6)方案一:向盛有 0.1 mol·L-1 AgNO3 溶液的试管中滴加 0.1 mol·L-1 KSCN 溶液至不再有白色沉淀生成,向其中滴加 0.1 mol·L-1 KI 溶液,白色沉淀转化为黄色 沉淀,则证明 Ksp(AgI)<Ksp(AgSCN)。方案二:将等体积的 0.1 mol·L-1 KSCN 溶液和 0.1 mol·L -1 KI 溶液混合,向混合液中滴加 0.1 mol·L-1 AgNO3 溶液,若生成黄色沉淀,则证明 Ksp(AgI) <Ksp(AgSCN)。 答案 (1)将带火星的木条放至导管口,木条复燃 (2)2AgNO3===== △ 2Ag+2NO2↑+O2↑ (3)A、B 装置之间连接一个防倒吸的安全瓶 (4)Ag++Fe2+===Ag+Fe3+ 0.5 mol/L (NH4)2SO4 溶液 (5)溶液中发生 Fe3++3SCN- Fe(SCN)3 使局部变红;振荡 试管时,过量的 Ag+与 SCN-反应生成 AgSCN 沉淀,降低了 c(SCN- ),平衡逆向移动,溶液 褪色 (6)方案一:向盛有 0.1 mol/L AgNO3 溶液的试管中滴加 0.1 mol/L KSCN 溶液至不再 有白色沉淀生成,向其中滴加 0.1 mol/L KI 溶液,白色沉淀转化为黄色沉淀,则证明 Ksp(AgI) <Ksp(AgSCN)。方案二:将等体积的 0.1 mol/L KSCN 溶液和 0.1 mol/L KI 溶液混合,向混 合液中滴加 0.1 mol/L AgNO3 溶液,若生成黄色沉淀,则证明 Ksp(AgI)<Ksp(AgSCN)。 4.(2020·辽宁丹东一模)某化学实验小组的同学将打磨过的镁条投入到滴有酚酞的饱和 NaHCO3 溶液中,发现反应迅速,产生大量气泡和白色不溶物,溶液的浅红色加深。该小组 同学对白色不溶物的成分进行了探究和确定。 I.提出假设: (1)甲同学:可能只是 MgCO3; 乙同学:可能只是________; 丙同学:可能是 xMgCO3·yMg(OH)2。 (2)在探究沉淀成分前,需将沉淀从溶液中过滤、洗涤、低温干燥,洗涤沉淀的操作方 法是________________________________________________________________________ ________________________________________________________________________。 Ⅱ.定量实验探究:取一定量已干燥过的沉淀样品,利用下列装置测定其组成(部分固定 夹持装置未画出),经实验前后对比各装置的质量变化来分析沉淀样品的组成,得出丙同学 的假设是正确的。请回答下列问题: (3)写出 xMgCO3·yMg(OH)2 受热分解的化学方程式 ___________________________________________________。(用 x、y 表示) (4)①实验中合理的实验装置连接顺序为; e→____→____→____→____→____→____→____。(各装置只使用一次) ②实验一段时间后,当装置 B 中__________(填实验现象)时,停止加热,说明沉淀样品 已完全分解,然后打开 f 处的活塞,缓缓通入空气数分钟的目的是____________________。 ③指导老师认为在上述实验装置末端还需再连接一个装置 D,若无此装置,则会使测出 的 x∶y 的值__________(填“偏大”“偏小”或“无影响”)。 (5)若改进实验后,最终装置 B 质量增加 m 克,装置 D 质量增加 n 克,则 x∶y=________(用 含 m、n 的代数式表示)。 解析 I.(1)综合甲和丙的假设,乙的假设只能是 Mg(OH)2;(2)洗涤沉淀的操作方法是 向过滤器中沿玻璃棒注入蒸馏水至浸没沉淀,待水自然流下后重复操作 2~3 次; Ⅱ.(3) 根 据 原 子 守 恒 可 知 xMgCO3·yMg(OH)2 受 热 分 解 的 化 学 方 程 式 为 xMgCO3·yMg(OH)2===== △ (x+y)MgO+xCO2↑+yH2O;(4)①根据各装置的特点可以发现该定 量实验是这样设计的,先用除去二氧化碳和水的空气把整套装置内的空气排尽,再把一定质 量的沉淀样品加热让其完全分解,分解产生的气体先通过浓硫酸吸收水,再通过碱石灰吸收 二氧化碳,分别称量浓硫酸和碱石灰的增重,即可计算出样品的组成。所以合理的实验装置 连接顺序为 efabcdgh;②实验一段时间后,当装置 B 中无气泡冒出时,停止加热,说明沉 淀样品完全分解;然后打开 f 处的活塞,缓缓通入空气数分钟的目的是将装置中生成的 CO2 和水蒸气排入后续装置被碱石灰和浓硫酸充分吸收;③指导老师认为在上述实验装置末端还 需再连接一个装置 D,其目的是防止空气中的水蒸气和二氧化碳被原来的 D 装置吸收,以 致因测得二氧化碳的质量偏大导致碳酸镁的含量偏多,所以若无此装置,会使测出的 x∶y 的值偏大; (5)若改进实验后,最终装置 B 质量增加 m 克,水的物质的量是 m 18mol。装置 D 质量增 加 n 克,即 CO2 的物质的量是 n 44mol,则根据原子守恒可知 x∶y= n 44mol∶m 18 =9n∶22m。 答案 (1)Mg(OH)2 (2)向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复操 作 2~3 次 (3)xMgCO3· yMg(OH)2===== △ (x+y)MgO+xCO2↑+yH2O (4)①fabcdgh ②无气泡冒出 排出装置中的 CO2 和水蒸气 ③偏大 (5)9n∶22m 5.为了探究 AgNO3 的氧化性和热稳定性,某化学兴趣小组设计了如下实验。 Ⅰ.AgNO3 的氧化性 将光亮的铁丝伸入 AgNO3 溶液中,一段时间后将铁丝取出。为检验溶液中 Fe 的氧化产 物,将溶液中的 Ag+除尽后,进行了如下实验。可选用的试剂:KSCN 溶液、K3[Fe(CN)6] 溶液、氯水。 (1)请完成下表: 操作 现象 结论 取少量除尽 Ag+后的溶液于试管中,加入 KSCN 溶液,振荡 ①________ 存在 Fe3+ 取少量除尽 Ag+后的溶液于试管中,加入②__________,振荡 ③________ 存在 Fe2+ [实验结论] Fe 的氧化产物为 Fe2+和 Fe3+ Ⅱ.AgNO3 的热稳定性 用如图所示的实验装置 A 加热 AgNO3 固体,产生红棕色气体,在装置 D 中收集到无色 气体。当反应结束后,试管中残留固体为黑色。 (2)装置 B 的作用是__________。 (3)经小组讨论并验证该无色气体为 O2,其验证方法是 ________________________________________________________________________。 (4) [查阅资料] Ag2O 和粉末状的 Ag 均为黑色;Ag2O 可溶于氨水。 [提出设想] 试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag2O;ⅲ.Ag 和 Ag2O。 [实验验证] 该小组为验证上述设想,分别取少量黑色固体放入试管中,进行了如下实 验。 实验编号 操作 现象 a 加入足量氨水,振荡 黑色固体不溶解 b 加入足量稀硝酸,振荡 黑色固体溶解,并有气体产生 [实验评价] 根据上述实验,不能确定固体产物成分的实验是______(填实验编号)。 [实验结论] 根据上述实验结果,该小组得出 AgNO3 固体热分解的产物有________。 解析 (1)检验 Fe3+可用 KSCN 溶液,现象为溶液呈红色。检验 Fe2+可用 K3[Fe(CN)6] 溶液,Fe2+与 K3[Fe(CN)6]反应可产生蓝色沉淀。(2)装置 B 的作用为防止溶液倒吸进入试管 中。(3)O2 的检验方法为用带火星的木条伸入集气瓶内,木条复燃。(4)由题干信息可知,Ag2O 可溶于氨水,实验 a 加入足量氨水,固体不溶解,所以固体成分为 Ag;而 Ag 和 Ag2O 都溶 于稀 HNO3,所以实验 b 不能确定固体成分。 答案 (1)①溶液呈红色 ②K3[Fe(CN)6]溶液 ③产生蓝色沉淀 (2)防倒吸 (3)用带火 星的木条伸入集气瓶内,木条复燃,证明无色气体为 O2 (4)b Ag、NO2、O2 6.(2019·广东六校联考)某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱 和食盐水,并用电解产生的 H2 还原 CuO 粉末来测定 Cu 的相对原子质量,同时检验氯气的 氧化性。 (1)写出装置甲的电解总反应方程式 ____________________________________________________________________。 (2)为完成上述实验,正确的连接顺序为 E→__________(填写连接的字母)。 (3)对硬质玻璃管里的氧化铜粉末进行加热前,需要先通一段时间某气体并检验该气体 的纯度,检验该气体已经纯的具体的操作和现象为 ________________________________________________________________________ ____________________________________________________________________。 (4)乙装置的 a 瓶溶液可选用________。 A.淀粉碘化钾溶液 B.酸性高锰酸钾溶液 C.硫化钠溶液 D.Fe(NO3)2 溶液 (5) 若 a 瓶 中 盛 放 过 量 的 NaHSO3 溶 液 , 写 出 发 生 的 离 子 反 应 方 程 式 ________________________________________________________________________。 (6)为测定 Cu 的相对原子质量,设计了如下甲、乙两个实验方案。精确测量硬质玻璃管 的质量为 a g,加入 CuO 后,精确测量硬质玻璃管和 CuO 的总质量为 b g , 实验完毕后: 甲方案:通过精确测量硬质玻璃管和 Cu 粉的总质量为 c g, 进而确定 Cu 的相对原子质 量。 乙方案:通过精确测定生成水的质量 d g,进而确定 Cu 的相对原子质量。 乙方案不足之处是_________________________________________________。 按甲方案进行计算,Cu 的相对原子质量为__________。(用含 a、b、c 的式子来表示) 解析 (1)电解饱和食盐水生成氢氧化钠、氯气、氢气,反应的总反应方程式为 2NaCl +2H2O===== 电解 2NaOH+H2↑+Cl2↑。 (2)A 是阴极,阴极上产生的是氢气,B 是阳极,阳极上产生的是氯气,要用氢气来还 原氧化铜,所以 A 连接 E,干燥氢气后用氢气来还原氧化铜,所以 B 连接 C。 (3)氢气属于易燃气体,对硬质玻璃管里的氧化铜粉末进行加热前,需要先通一段时间 某氢气,以排除装置中的空气,检验氢气的纯度的方法为用排水法收集一小试管该气体,用 拇指堵住试管口,移近酒精灯火焰,松开拇指,如果听到轻微的爆鸣声,说明该气体已纯。 (4)检验氯气的氧化性可以利用还原性的物质发生反应,且有明显的现象,可以把氯气 通入淀粉碘化钾溶液发生氧化还原反应,生成碘单质遇淀粉变蓝;也可以将氯气通入硫化钠 溶液中,反应生成淡黄色的沉淀,氯气与酸性高锰酸钾溶液不反应,氯气与硝酸亚铁反应不 能证明是氯气的氧化性,可能是硝酸的氧化性,故选 AC; (5)若 a 瓶中盛放过量的 NaHSO3 溶液,氯气将亚硫酸氢钠氧化为硫酸钠,反应的离子反 应方程式为 4HSO- 3 +Cl2===SO2- 4 +2Cl-+3SO2+2H2O。 (6)在乙方案中,装置中 U 型管会吸收空气中的 CO2 和水,会导致测定 Cu 的相对原子 质量有误差,所以乙方案不合理,甲合理;根据甲方案,设金属铜的原子量为 M,则 CuO ~ Cu M+16 M b-a c-a 则:M+16 b-a = M c-a ,解得:M=16c-a b-c 。 答案 (1)2NaCl+2H2O===== 遇电 2NaOH+H2↑+Cl2↑ (2)A→B→C (3)用排水法收集一 小试管该气体,用拇指堵住试管口,移近酒精灯火焰,松开拇指,如果听到轻微的爆鸣声, 说明该气体已纯 (4)AC (5)4HSO- 3 +Cl2===SO2- 4 +2Cl-+3SO2+2H2O (6)空气中的 CO2 和 H2O 可以通过 D 口进入 U 形管造成所测水质量偏大 16(c-a)/(b-c)查看更多