安徽省蚌埠市教师2020届高三化学“我为高考命题”仿真模拟试题蚌埠一中5
安徽省蚌埠市教师2020届高三化学“我为高考命题”仿真模拟试题(蚌埠一中5)
7.下列说法中不正确的是 A.用电化学氧化的方法,可以在铝制品表面生成坚硬的氧化膜 B.煤的间接液化是指先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇 C.聚甲基丙烯酸甲酯(又称有机玻璃)是由缩聚反应制得的高分子化合物 D.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染
8.环之间共用一个碳原子的化合物称为螺环化合物,螺[3,3]庚烷()是其中的一 种。下列关于该化合物的说法正确的是
A.与甲苯(C7H8)互为同分异构体
B.1mol 该化合物完全燃烧时消耗 10 mol O2
C.所有碳原子均处同一平面
D.一氯代物共有 3 种(不含立体异构)
9.通常检测 SO2 含量是否达到排放标准的反应原理是 SO2 +H2O2 + BaCl2 ===BaSO4↓+ 2HCl。
NA 表示阿伏加德罗常数,下列说法正确的是( )
A.0.1 mol BaCl2 晶体中所含微粒总数为 0.1NA
B.25 ℃时,pH =1 的 HCl 溶液中含有 H+的数目为 0.1NA
C.17 g H2O2 中含有非极性键数目为 0.5NA
D.生成 2.33 g BaSO4 沉淀时,转移电子数目为 0.01NA
10.下列实验方案能达到相应实验目的的是
选项
实验目的
实验方案
A
分离 Fe2O3、Al2O3
将混合物投入足量 NaOH 溶液中然后依次进行过 滤、洗涤、蒸发、灼烧四项操作
B
验证淀粉溶液水解生成葡萄糖
向淀粉溶液中加入稀硫酸共热,冷却后再加入新 制 Cu(OH)2 悬浊液,加热
C
制备无水 AlCl3
蒸发铝与稀盐酸反应后的溶液
D
检验 FeSO4 晶体是否完全变质
取少量久置的 FeSO4 晶体于试管中,逐滴加入酸 性高锰酸钾溶液
8
A.A B.B C.C D.D
11.W、X、Y、Z 是四种短周期主族元素,原于序数依次增大,W 的一种原子核内无中子, X、Y 原子核外 L 电子层的电子数之比为 3:4,Y, Z 位于同一周期,Z 的一种单质常温下 是淡黄色晶体,四种元素的原子最 外层电子数之和为 14。下列说法错误的是()
A.X 与其它三种元素均能形成二种二元化合物
B.X、Z 阴离子的还原性强弱:Z>X C.X、Y 的简单离子半径大小:X>Y D.X 和 Z 的简单氢化物沸点;X
c(HA-)>c(H+)>c(A2-)>c(OH-)
8
26.三氯氧磷(POCl3)是一种重要的化工原料,工业上可以直接氧化 PCl3 制备 POCl3,反应原
理为:P4(白磷)+6Cl2=4PCl3 2PCl3+O2=2POCl3
PCl3、POCl3 的部分性质如下:
熔点/℃
沸点/℃
其他
PCl3
-112
75.5
遇水生成 H3PO3 和 HCl
POCl3
2
105.3
遇水生成 H3PO4 和 HCl
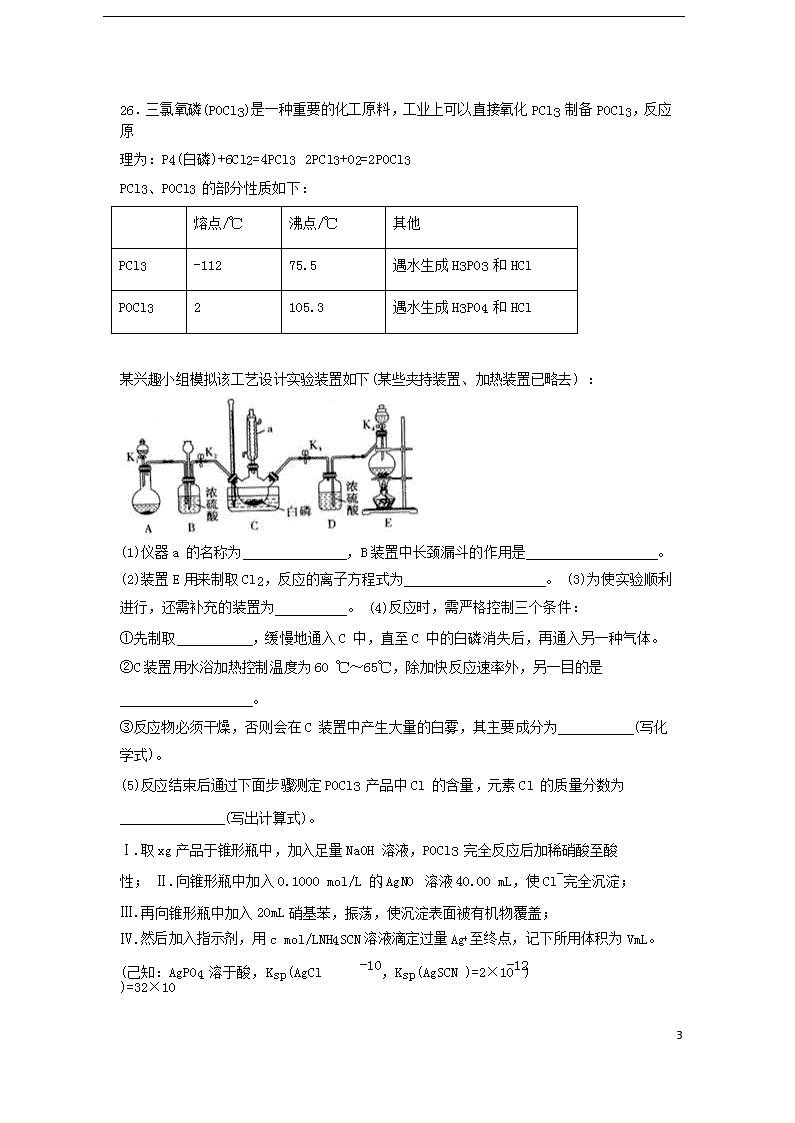
某兴趣小组模拟该工艺设计实验装置如下(某些夹持装置、加热装置已略去) :
(1)仪器 a 的名称为 ,B 装置中长颈漏斗的作用是 。 (2)装置 E 用来制取 Cl2,反应的离子方程式为 。 (3)为使实验顺利进行,还需补充的装置为 。 (4)反应时,需严格控制三个条件:
①先制取 ,缓慢地通入 C 中,直至 C 中的白磷消失后,再通入另一种气体。
②C 装置用水浴加热控制温度为 60 ℃~65℃,除加快反应速率外,另一目的是
。
③反应物必须干燥,否则会在 C 装置中产生大量的白雾,其主要成分为 (写化 学式)。
(5)反应结束后通过下面步骤测定 POCl3 产品中 Cl 的含量,元素 Cl 的质量分数为
(写出计算式)。
3
Ⅰ.取 xg 产品于锥形瓶中,加入足量 NaOH 溶液,POCl3 完全反应后加稀硝酸至酸性; Ⅱ.向锥形瓶中加入 0.1000 mol/L 的 AgNO 溶液 40.00 mL,使 Cl-完全沉淀; Ⅲ.再向锥形瓶中加入 20mL 硝基苯,振荡,使沉淀表面被有机物覆盖;
8
+
Ⅳ.然后加入指示剂,用 c mol/LNH4SCN 溶液滴定过量 Ag
�至终点,记下所用体积为 VmL。
8
8
-10
�-12
8
(己知:AgPO4 溶于酸,Ksp(AgCl )=32×10
�,Ksp(AgSCN )=2×10 )
8
27.工业上用含锰废料(主要成分 MnO2,含有少量 Fe2O3、Al2O3、CuO、CaO 等)与烟气脱硫进
行联合处理并制备 MnSO4 的流程如下:
已知:25℃时,部分氢氧化物的溶度积常数(Ksp)如下表所示。
氢氧化物
Al(OH)3
Fe(OH)3
Cu(OH)2
Mn(OH)2
Ksp
1.0×10-33
4.0×10-38
2.0×10-20
4.0×10-14
请回答:
(1)沉淀 1 的化学式为 。
(2)(NH4)2S 的电子式为 ;“净化”时,加入(NH4)2S 的作用为
。
(3)“酸化、还原”中,发生的所有氧化还原反应的离子方程式为 。 (4)已知:滤液 3 中除 MnSO4 外,还含有少量(NH4)2SO4。(NH4)2SO4、MnSO4 的溶解度曲线如 下图所示。
据此判断,操作“I”应为蒸发浓缩、 、洗涤、干燥。
(5)工业上可用电解酸性 MnSO4 溶液的方法制备 MnO2,其阳极反应式为 。 (6)25.35 g MnSO4·H2O 样品受热分解过程的热重曲线(样品质量随温度变化的曲线)如 下图所示。
8
①300℃时,所得固体的化学式为 。
②1150℃时,反应的化学方程式为 。
28.火山爆发时会喷出 SO2,SO2 是大气主要污染物之一,在工业中可用于制备硫酸。 回答下列问题:
(1)SO2 是 (填“电解质”或“非电解质”)。
(2)Cu2S 与 O2 反应可生成 SO2,已知:
8
1
Cu(s)+
2
�
O2(g)=CuO(s) △H=x kJ∙mol-1
8
8
1
Cu(s)+
2
�1
S(s)=
2
�
Cu2S(s) △H=y kJ∙mol-1
8
S(s)+O2(g)=SO2(g) △H=z kJ∙mol-1
写出 Cu2S 与 O2 反应生成 CuO 和 SO2 的热化学方程式 。
(3)硫酸工业中涉及反应:2SO2(g)+O2(g)⇌2SO3(g)△H=Q kJ·mol-1。一定条件下,在 2L 恒容密闭容器中,通入 2molSO2 和 1molO2 发生上述反应,SO2 的平衡转化率与压强、温度 的关系如图所示。a 点时此反应的平衡常数的数值为 。
关于该反应,下列说法正确的是 。
A.容器内混合气体的密度不再变化时,反应达到平衡
8
B.相同时间内生成 2molSO2 同时消耗 1molO2,反应达到平衡
C.Q 大于 0
D.相同温度下,压强越大,SO2 的平衡转化率就越大,该反应的平衡常数就越大 E.反应达到平衡后保持温度不变,再充入 2molSO2 和 1molO2,SO2 的平衡转化率增大 F.反应达到平衡后保持温度不变,再充入 He(g),SO2 的平衡转化率增大
(4)将 SO2 通入酸化的硝酸钡溶液可生成硫酸钡沉淀,25℃时,KSP(BaSO4)=1×10-10。
4
c (SO2- )
8
3
KSP(BaCO3)=2.6×10-9。该温度下,BaSO4 和 BaCO3 沉淀共存的悬浊液中,
�c (CO2- ) = 。
8
(5)用如图装置回收 SO2 可制得硫酸,电极为惰性电极,a、b 膜分别为阳离子交换膜、阴
离子交换膜。阳极的电极反应为 。
35.铬和铜都是人体所必需的微量元素。回答下列问题:
(1)铬原子的最高能层符号是 ,其价层电子的轨道表达式(电子排布图)为 。
(2) 比较第二电离能 Cu Zn(填“>”、“=”、“<”),理由是
(3)铬的一种氧化物常温下呈蓝色,化学式为 CrO5,已知该氧化物中铬为+6 价,请写出 CrO5
的结构式
(4)氧化亚铜溶于浓氨水中形成无色配离子[Cu(NH3)2]+,则该配离子中铜的化合价为
,杂化类型为 。[Cu(NH3)2]2SO4 中阴离子的立体构型是 。
(5)已知图 1 为铬的晶胞结构图,则铬晶胞属于 堆积,晶胞中实际拥有的铬原子数 为 ;图 2 是铜的晶胞结构图,若其立方晶胞参数为 a nm,该晶胞中原子的体积占 晶胞体积的百分率为 。
8
36.(15 分)(化学——选修 5:有机化学基础)
高血脂是一种常见的心血管疾病,治疗高血脂的新药 I 的合成路线如下:
回答下列问题:
(1)反应①所需试剂、条件分别是 ;F 的化学名称为 。
(2)②的反应类型是 ;A→B 的化学方程式为 。
(3)G 的结构简式为 ;H 中所含官能团的名称是 。
(4)化合物 W 的相对分子质量比化合物 C 大 14,且满足下列条件,W 的可能结构有
种。
①遇 FeCl3 溶液显紫色 ②属于芳香族化合物 ③能发生银镜反应其中核磁共振氢谱显示 有 5 种不同化学环境的氢,峰面积比为 2:2:2:1:1,写出符合要求的 W 的结构简式
。
(5)设计用甲苯和乙醛为原料制备的合成路线,其他无机试剂任选
(合成路线常用的表示方式为: ) 。
8
8
参考答案
7C 8B 9 C 10 D 11 D 12 D 13 D
26.球形冷凝管 平衡气压 4H++2Cl-+MnO
�Mn2++Cl ↑+2H O 在 a 仪器后连
2 2 2
接装有碱石灰的干燥管 Cl2 防止 PCl3 气化 HCl
2+ 2+
27.CaSO4 使 Cu
�转化为 CuS 沉淀(或除去 Cu )
2+ 2-
�+ 2+ 2-
MnO2+SO2=Mn
�+SO4
�、 Fe2O3+SO2+2H =2Fe
�+SO4
�+H2O 趁热过滤
Mn2++2H O-2e-=MnO +4H+ MnSO
�3MnO
�Mn O +O ↑
2 2 4
�2 3 4 2
5
28.非电解质 Cu2S(s)+2O2(g)=2CuO(s)+SO2(g) △H=(2x+z―2y)kJ·mol-1
32
1
2- -
�2- +
或 0.15625 BE
26
�SO3
�-2e +H2O=SO4
�+2H
35.N > 测试第二电离能时铜原子失去
的是处于全充满稳定状态的 3d10 电子;而锌原子失去的是 4s1 电子,之后价电子层形成 稳定状态的 3d10 +1 sp 正四面体 体心立方 2
74%
36.(1)Cl2、光照(1 分) 辛醛 (1 分)
(1)取代反应 (1 分) (2 分)
(3) (2 分) 羟基 (1 分)
(4) 13 (2 分) (2 分)
(5)
(3 分)