- 2021-07-06 发布 |
- 37.5 KB |
- 8页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2017-2018学年陕西省黄陵中学高新部高二上学期开学考化学试题
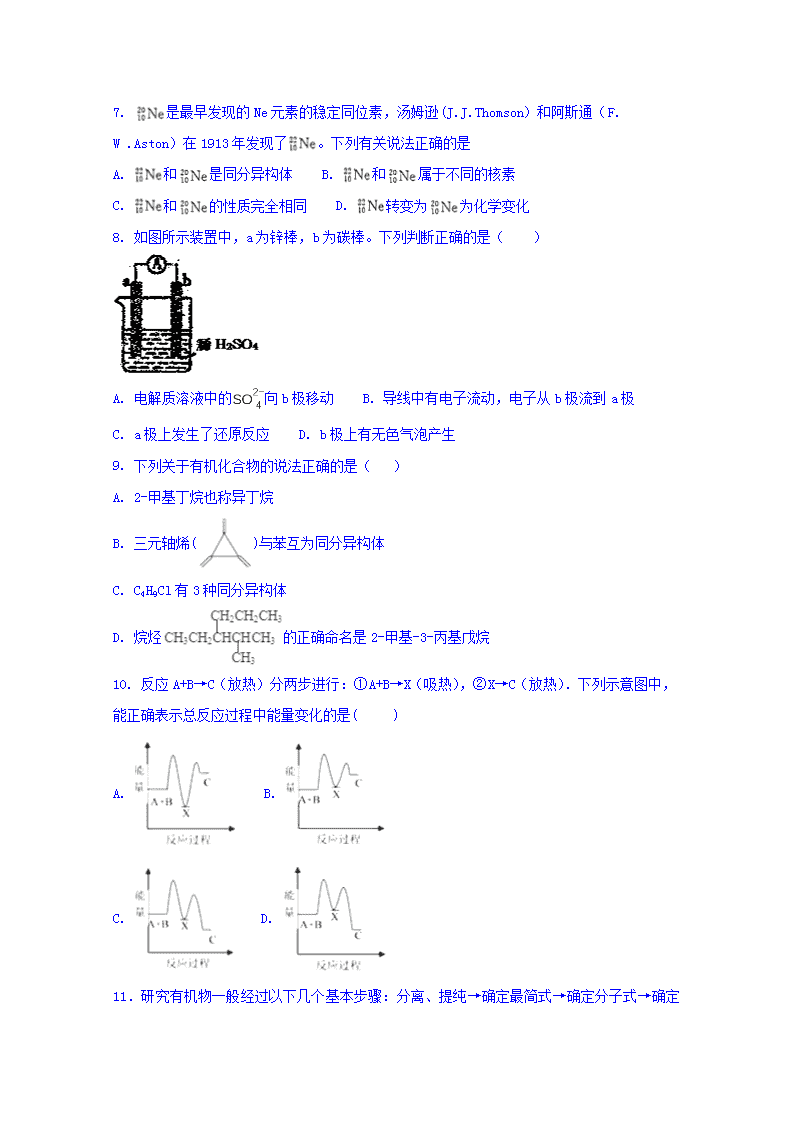
2017-2018学年高新部高二开学考试化学试题 第I卷(选择题) 一.选择题(20×3分=60分) 一、选择题(60分) 1.丙烯酸(CH2=CH—C00H)的性质可能有①加聚反应②酯化反应③中和反应④氧化反应⑤水解反应 A.只有①③ B.只有②③④ C.只有①④ D.全部 2.能通过化学反应使溴水褪色,又能使酸性髙锰酸钾褪色的是 A.苯 B.乙烯 C.乙醇 D.乙酸 3.设NA表示阿伏加德罗常数,下列叙述不正确的是 A. 1mol羟基所含电子数为9NA B.常温下有的共价键数为NA C.标准状况下,22.4L CH3Cl所含原子数为5NA D. 23gNA与足量乙醉反应完全后可生成H2数为NA 4. 用60K乙酸雨92g乙醇的反应,实际得到乙酸乙酯的质量为52.8g,本实验的产率是 A.30% B.40% C.60% D.90% 5.下图为元素周期表中短周期的一部分,下列说法正确的是() A. 非金属性:Y>Z>M B. 离子半径:M->Z2->Y- C. ZM2分子中各原子的最外层均满足8电子稳定结构 D. 三种元素中,Y的最高价氧化物对应的水化物酸性最强 6. 某有机物的结构简式为,它在一定条件下可能发生的反应是( ) ①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦还原. A. ①③④⑤⑥⑦ B. ①③④⑤⑦ C. ①③⑤⑥⑦ D. ②③④⑤⑥ 7. 是最早发现的Ne元素的稳定同位素,汤姆逊(J.J.Thomson)和阿斯通(F. W .Aston)在1913年发现了。下列有关说法正确的是 A. 和是同分异构体 B. 和属于不同的核素 C. 和的性质完全相同 D. 转变为为化学变化 8. 如图所示装置中,a为锌棒,b为碳棒。下列判断正确的是( ) A. 电解质溶液中的向b极移动 B. 导线中有电子流动,电子从b极流到a极 C. a极上发生了还原反应 D. b极上有无色气泡产生 9. 下列关于有机化合物的说法正确的是( ) A. 2-甲基丁烷也称异丁烷 B. 三元轴烯()与苯互为同分异构体 C. C4H9Cl有3种同分异构体 D. 烷烃的正确命名是2-甲基-3-丙基戊烷 10. 反应A+B→C(放热)分两步进行:①A+B→X(吸热),②X→C(放热).下列示意图中,能正确表示总反应过程中能量变化的是( ) A. B. C. D. 11.研究有机物一般经过以下几个基本步骤:分离、提纯→确定最简式→确定分子式→ 确定结构式,以下用于研究有机物的方法错误的是( ) A. 蒸馏常用于分离提纯液态有机混合物 B. 燃烧法是研究确定有机物成分的有效方法 C. 1H核磁共振谱通常用于分析有机物的相对分子质量 D. 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 12.柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是( ) A.柠檬烯的一氯代物有7种 B.柠檬烯和丁基苯互为同分异构体 C.柠檬烯的分子中所有的碳原子可能在同一个平面上 D.在一定条件下,柠檬烯可以发生加成、取代、氧化、还原等反应 13.关于化学反应与能量的说法正确的是( ) A.中和反应是吸热反应 B.燃烧属于放热反应 C.化学键断裂放出能量 D.反应物总能量与生成物总能量一定相等 14.进行一氯取代反应后,只能生成两种沸点不同的有机物的烷烃是( ) A. (CH3)2CHCH(CH3)2 B. 新戊烷 C. 异戊烷 D. (CH3)3CCH2CH3 15.银锌纽扣电池放电时的反应为:Zn+Ag2O=ZnO+2Ag,下列有关说法中不正确的是 A.该反应属于置换反应 B.做负极 C.Ag2O在正极上发生还原反应 D.可用稀硝酸做电解质溶液 16.向等质量的两份锌粉a、b中分别加入过量的稀硫酸,同时向a中加入少量的CuSO4溶液,下列各图表示的是产生H2的体积V与时间t的关系,其中正确的是 17.反应:2NO2 2NO + O2,在恒温恒容的容器中反应,说明反应达平衡状态的标志是: ① 单位时间内生成n mol O2的同时生成2n mol NO2; ② 单位时间内生成n mol O2 的同时, 生成2n mol NO; ③ NO2、NO、O2 的反应速率的比为2 : 2 : 1的状态; ④ 混合气体的 颜色不再改变的状态; ⑤ 混合气体的密度不再改变的状态; ⑥ 混合气体的总压强不再改变的状态。 A.①④⑥ B.①③④ C.②③⑤ D.①②③④⑤⑥ 18.在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如右图所示。下列说法不正确的是 A.该反应的化学方程式为5A+4B4C B.2min前,正反应速率逐渐减小,逆反应速率逐渐增大 C.用B的浓度变化表示2min内的速率为2mol/(L·min) D.2min时,该反应达到平衡,此时A、B、C的浓度比为5:4:4 19. 分子式为C4H10O属于醇的同分异构体的数目为 A.2种 B.3种 C.4种 D.5种 20.冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或H2、CO)法;③活泼金属置换法;④电解法。这四种方法在工业上均有应用。古代有:(Ⅰ)火烧孔雀石[主要成分是Cu2(OH) 2CO3]炼铜;(Ⅱ)湿法炼铜。现代有:(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石(主要成分是MgCl2)中炼镁。下列分析不正确的是 A.①用于(Ⅰ) B.②用于(Ⅱ) C.③用于(Ⅲ) D.④用于(Ⅳ) 第II卷(非选择题共40分) 21.(12分) 元素及其化合物的知识是高中化学重要的组成部分,是考查化学基本概念和理论、化学计算、化学实验知识的载体。 (1)元素周期表1-20号元素中,某两种元素的原子序数相差3,周期数相差1。 ①这样的两种元素的组合有________种。 ②若这样的两种元素形成的化合物中原子数之比为1∶1。 写出其中一种化合物的名称:_______________________; (2)A是自然界存在最广泛的ⅡA族元素,常以化合物F存在.从单质A起始发生的一系列化学反应可由下图表示: 请回答下列问题: ①F的化学式为________,D的电子式为________________。 ②E与水反应的化学方程式为___________________________________________; ③实际生产中,可由F为原料制备单质A,写出制备过程的化学方程式(不需考虑综合经济效益)_______________________________________________________。 22.(8分)已知X是一种具有果香味的合成香料,下图为合成X的某种流程: 提示:①不能最终被氧化为-COOH; ②D的产量可以用来衡量一个国家的石油化工水平。 请根据以上信息,回答下列问题: (1)D与C分子中官能团的名称分别是____________,E的结构简式是____________。 (2)D→E的化学反应类型为____________反应。 (3)上述A、B、C、D、E、X六种物质中,互为同系物的是____________。 (4)反应C+E→X的化学方程式为___________________________________________。 (5)反应B→C的化学方程式为_______________________________________________。 23.海带中含有丰富的碘。某研究性学习小组按下图所示实验流程提取海带中的碘。(12分) 回答下列问题: (1)步骤①灼烧海带时,除三脚架外,还需要用到下列仪器中的________(填字母标号)。 A.烧杯 B.坩埚 C.蒸发皿 D.泥三角 E.酒精灯 F.干燥器 (2)步骤③的实验操作名称是________。 (3)步骤④反应的离子方程式为____________________________。 (4)步骤⑤中,可以用苯来提取碘的理由是___________________,碘水溶液加入苯后,振荡、静止可观察到的实验现象为________。 (5)请设计实验检验提取碘后的水溶液中是否还有单质碘______________________________________________________。 24.(8分) I.现用右图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。请回答下列问题: (1)b电极材料为 ,其电极反应式为_________________________。 (2)当量筒中收集到672 mL(标准状况下)气体时,通过导线的电子的物质的量为__________,此时a电极质量减少__________g。 II.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题: (1)上述实验中发生反应的离子方程式有: ; (2)硫酸铜溶液可以加快氢气生成速率的原因是 ; (3)要加快上述实验中气体产生的速率,还可采取的措施有 (答两种); 答案 1. C 2.B 3.D 4.C 5.C 6.A 7.B 8.D 9. B 10. D 11.C 12.D 13. B 14.A 15.D 16.A 17.A 18.D 19.C 20.B 21.(1) ①7 ;③过氧化钠或过硫化钾 (2)①CaCO3 ② NaH+H2O===NaOH+H2↑ ③CaCO3CaO+CO2↑ 2CaO2Ca+O2↑ 或CaCO3+2HCl=CaCl2+CO2↑+H2O CaCl2 Ca+Cl2↑ 22. 碳碳双键、羧基 CH3CH2OH 加成 A、E CH3CH2COOH+C2H5OHCH3CH2COOC2H5+H2O 2CH3CH2CHO+O22CH3CH2COOH 23.(1)BDE (2)过滤 (3)2I-+MnO2+4H+=Mn2++I2+2H2O (4)苯与水互不相溶;碘在苯中的溶解度比在水中的大 分层,上层为紫色,下层接近无色 (5)取少量提取碘后的水溶液于试管中,加入几滴淀粉试液。如果溶液变蓝,说明还有单质碘;如果溶液不变蓝,说明没有单质碘 24.(8分) I (1)纯铜片(1分);2H++2e-===H2↑(1分) (2) 0.06 mol(1分);1.95(1分) II(1)Zn + 2H+ ==Zn2+ + H2↑ Zn + Cu2+ == Zn2+ + Cu (1分) (2)CuSO4与Zn反应产生的Cu与Zn以及硫酸溶液形成Cu/Zn原电池,加快了氢气产生的速率。(1分) (3)升高反应温度、适当增加硫酸的浓度、增大锌粒的比表面积等(答两种即可)(2分)查看更多