- 2021-07-06 发布 |
- 37.5 KB |
- 5页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
高中化学 3_3_2乙酸课时提升卷 新人教版必修2
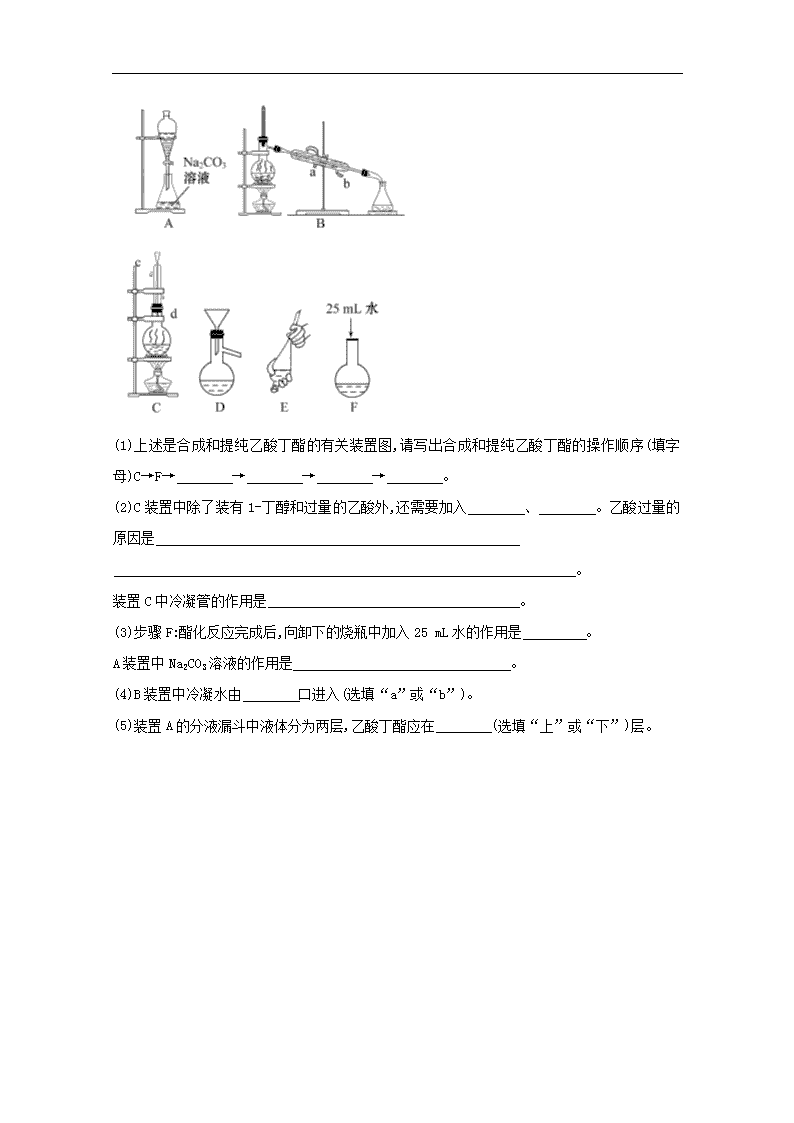
课时提升卷(十五) 乙 酸 一、选择题(本题包括6小题,每小题5分,共30分) 1.如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。该物质不可能具有的性质是( ) A.与氢氧化钠反应 B.与稀硫酸反应 C.发生酯化反应 D.使紫色石蕊溶液变红 2.(2013·嘉兴高一检测)下列物质中最难电离出H+的是 ( ) A.CH3COOH B.CH3CH2OH C.H2O D.H2CO3 3.实验室制乙酸乙酯1 mL后,沿试管壁慢慢加入紫色石蕊溶液0.5 mL,这时石蕊溶液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间(整个过程不振荡)。对可能出现的现象,叙述正确的是 ( ) A.石蕊层仍为紫色,有机层无色 B.石蕊层为三层环,由上而下呈红、紫、蓝三种颜色 C.石蕊层有两层,上层为紫色、下层为蓝色 D.石蕊层为三层环,由上而下呈蓝、紫、红三种颜色 4.(2013·长春高一检测)下列关于乙酸性质的叙述中,错误的是 ( ) A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体 B.乙酸具有氧化性,能跟钠反应放出H2 C.乙酸分子中含有碳氧双键,所以它能使溴水褪色 D.乙酸在温度低于16.6℃时,就凝结成冰状晶体 5.(双选)下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的 是 ( ) A.金属钠 B.溴水 C.碳酸钠溶液 D.紫色石蕊溶液 6.关于有机物HOOC—CHCH—CH2OH,下列说法不正确的是 ( ) A.分子式为C4H6O3,每摩尔该物质充分燃烧需消耗4 mol O2 B.能发生取代反应、加成反应、氧化反应、中和反应 C.分别与足量Na、NaOH、Na2CO3反应,生成物均为NaOOC—CH=CH—CH2OH D.该物质分子内和分子间都能发生酯化反应 二、非选择题(本题包括2小题,共20分) 7.(8分)(2013·锦州高一检测)巴豆酸的结构简式为CH3—CH=CH—COOH。 试回答: (1)巴豆酸的分子中含有 和 两种官能团(写名称)。 (2)巴豆酸与金属钠反应的化学方程式为 。 (3)巴豆酸 (选填“能”或“不能”)使溴水褪色。 (4)巴豆酸跟乙醇在浓硫酸催化下发生酯化反应的化学方程式为 。 8.(12分)(能力挑战题)乙酸丁酯(CH3COOCH2CH2CH2CH3)是具有果香味的香精,经酯化反应可进行乙酸丁酯的合成。有关物质的物理性质见下表。 乙酸 1-丁醇 乙酸丁酯 熔点/℃ 16.6 -89.5 -73.5 沸点/℃ 117.9 117 126.3 密度/g·cm-3 1.05 0.81 0.88 水溶性 互溶 互溶 难溶 合成过程如下:第一步:将1-丁醇和过量的乙酸混合加热发生酯化反应;第二步:洗涤提纯;第三步:蒸馏提纯。 (1)上述是合成和提纯乙酸丁酯的有关装置图,请写出合成和提纯乙酸丁酯的操作顺序(填字母)C→F→ → → → 。 (2)C装置中除了装有1-丁醇和过量的乙酸外,还需要加入 、 。乙酸过量的原因是 。 装置C中冷凝管的作用是 。 (3)步骤F:酯化反应完成后,向卸下的烧瓶中加入25 mL水的作用是 。 A装置中Na2CO3溶液的作用是 。 (4)B装置中冷凝水由 口进入(选填“a”或“b”)。 (5)装置A的分液漏斗中液体分为两层,乙酸丁酯应在 (选填“上”或“下”)层。 答案解析 1.【解析】选B。由比例模型可知该物质为乙酸(CH3COOH),显酸性,能使紫色石蕊变成红色,能与NaOH反应,能发生酯化反应,但与稀硫酸不反应。 2.【解析】选B。电离出H+的难易或酸性的强弱,主要取决于羟基氢的活泼性。上述四种物质羟基氢的活泼性由强到弱的顺序为CH3COOH>H2CO3> H2O>CH3CH2OH。 3.【解析】选B。上层为乙酸乙酯层,溶有乙酸,遇石蕊显红色,中间为石蕊层,显紫色,下层为碳酸钠层,显碱性,遇石蕊显蓝色。 4.【解析】选C。碳氧双键不能与Br2加成,故不能使溴水褪色。 5.【解析】选C、D。Na2CO3与乙酸反应产生气泡,与乙醇互溶,与苯分层,与Ba(OH)2反应产生沉淀;紫色石蕊溶液遇乙酸变红,与乙醇互溶,与苯分层,遇Ba(OH)2溶液变蓝。 6.【解析】选C。该物质分子式为C4H6O3,1 mol该物质完全燃烧消耗O2为(4+-)mol,即4 mol,A正确;因含碳碳双键,能发生加成反应、氧化反应,含有羧基能发生取代反应和中和反应,故B正确;该物质与Na反应的产物应为NaOOC—CH=CH—CH2ONa,C错误;因同时含有羧基和羟基,则该物质分子内与分子间均能发生酯化反应。 【答题技巧】利用官能团判断物质的性质 (1)碳碳双键:能发生加成反应、氧化反应,如与溴发生加成反应,能使酸性高锰酸钾溶液褪色。 (2)羟基:能发生氧化反应、取代反应,如能催化氧化,发生酯化反应。 (3)羧基:具有酸的通性,能发生酯化反应,如与钠、氢氧化钠、碳酸氢钠溶液反应,与乙醇发生酯化反应。 7.【解析】由巴豆酸的结构简式可知,巴豆酸分子中含有碳碳双键和羧基两种官能团,能使溴水褪色,能与金属钠反应产生氢气,和乙醇发生酯化反应。 答案:(1)碳碳双键 羧基 (2)2CH3—CH=CH—COOH+2Na2CH3—CH=CH—COONa+H2↑ (3)能 (4)CH3—CH=CH—COOH+CH3CH2OHCH3—CH=CH—COOCH2CH3+H2O 8.【解析】(1)根据合成步骤:发生酯化反应→洗涤(加水、振荡、分液)→蒸馏,所以仪器的连接顺序是C→F→E→A→D→B。 (2)酯化反应需要加入浓硫酸作催化剂和吸水剂,加热液体和液体的混合物时需要加入沸石或碎瓷片,防止暴沸。加入过量的反应物,可以使平衡正向移动,增大酯化反应的产率。竖直向上的冷凝管一般起两个作用:①导气,平衡内外压强;②使挥发出的原料和产品冷凝回流,增加原料的利用率。(3)因为乙酸丁酯难溶于水而1-丁醇和乙酸与水互溶,所以加入水的作用是溶解1-丁醇和乙酸,然后分液即可分离出乙酸丁酯。加入Na2CO3溶液可以中和残留在乙酸丁酯中的酸。为了保证冷凝管中始终充满冷水,应该是下端进水,上端出水。乙酸丁酯的密度比水的小,应该在液体的上层。 答案:(1)E A D B (2)浓硫酸 沸石或碎瓷片 提高乙酸浓度以促使酯化反应平衡正向移动 冷凝回流挥发的原料和产品 (3)溶解吸收未反应的酸和醇 中和(或吸收)残留在乙酸丁酯中的酸 (4)b (5)上查看更多