- 2021-07-06 发布 |
- 37.5 KB |
- 22页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
新疆乌鲁木齐市第八中学2020届高三第一次月考化学试题
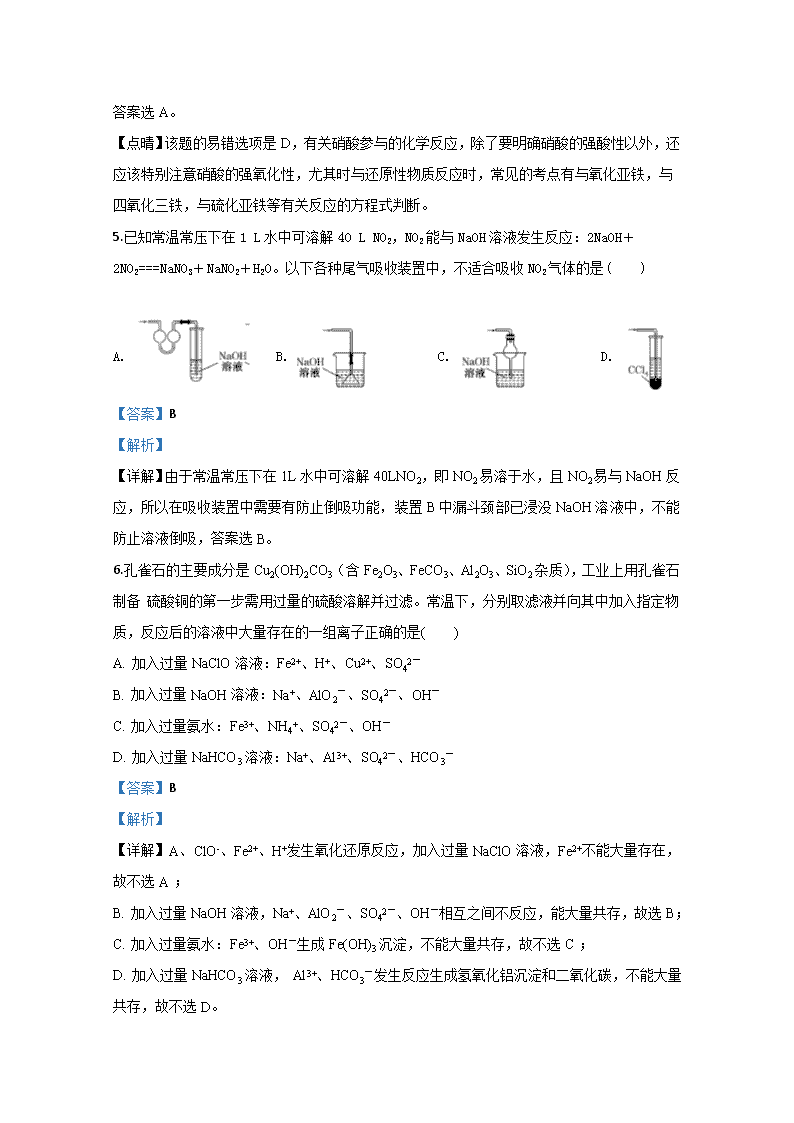
乌鲁木齐市第八中学2020届高三第一次月考化学试卷 1.化学与生活、社会发展息息相关。下列说法不正确的是 A. “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 B. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 C. “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 D. 氢氧化铝具有弱碱性,可用作胃酸中和剂 【答案】C 【解析】 A.雾霾所形成的气溶胶属于胶体,胶体都有丁达尔效应,A正确;B. “熬胆矾铁釜,久之亦化为铜”,意思是用铁锅加热硫酸铜晶体,时间长了,铁锅表面就变成了铜,该过程发生了铁与硫酸铜反应生成铜和硫酸亚铁,属于置换反应,B正确;C. “青蒿一握,以水二升渍,绞取汁”,文中对青蒿素的提取方法是浸取溶解,属于物理变化,没有涉及化学变化,C不正确;D. 氢氧化铝是两性氢氧化物,与强碱反应时表现酸性,与酸反应时表现碱性。由于氢氧化铝是难溶的弱电解质,所以不论其表现酸性还是表现碱性,都是非常弱的,所以它可以用作抗酸药。氢氧化铝可以与胃酸的主要成分盐酸反应生成氯化铝和水,在这个反应中氢氧化铝表现了碱性,D正确。本题选C。 2.用NA表示阿伏加德罗常数,下列说法正确的是( ) A. 含0.1 mol Na2O2的晶体中阳离子与阴离子总数为0.4NA B. 46 g NO2和N2O4的混合气体中含有的氧原子数为2NA C. 1 mol Fe与一定量硝酸恰好完全反应时,转移电子数一定为3NA D. 1 mol CH4与过量氯气发生取代反应,生成CH3Cl气体的体积约为22.4 L 【答案】B 【解析】 A.0.1mol Na2O2晶体中阳离子Na+为0.2mol,阴离子O22-物质的量为0.1mol,阳离子与阴离子总数为0.3NA,故D错误;B.NO2和N2O4的最简式相同,只需要计算46g NO2中氧原子数=×2×NA=2NA,故B正确;C.1mol Fe与硝酸反应可能生成硝酸铁也可能生成硝酸亚铁,故C错误;D.氯气与甲烷反应发生取代反应,同时有多个反应发生,所以标准状况下,1mol CH4与过量的氯气发生取代反应,生成CH3Cl气体的体积小于22.4L,故D错误;故选B。 点睛:本题考查阿伏加德罗常数的相关计算,熟悉公式是关键,注意物质的组成、结构。本题的易错点为D,要注意甲烷的取代反应得不到纯净的一氯甲烷。 3.下列离子方程式书写正确的是( ) A. 澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-===CaCO3↓+H2O B. 酸性高锰酸钾溶液与稀草酸反应:5C2O42-+2MnO4-+16H+===2Mn2++10CO2+8H2O C. AgCl的悬浊液中滴加Na2S溶液:2AgCl+S2-===Ag2S+2Cl- D. NH4HCO3溶液加入过量NaOH溶液加热:NH4++OH-===NH3•H2O 【答案】C 【解析】 【详解】A、酸式盐和碱反应量少的全部反应,离子方程式中符合化学式的组成比,澄清石灰水与过量的小苏打溶液反应的离子方程式为Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-,选项A错误;B.草酸是弱酸必须写化学式,酸性高锰酸钾可使草酸溶液褪色的离子反应为2MnO4-+5 H2C2O4+6H+=2Mn2++10CO2↑+8H2O,选项B错误;C、向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2―=Ag2S↓+2C1―,选项C正确;D.NH4HCO3溶液中加入过量NaOH溶液加热,离子方程式为:HCO3-+NH4++2OH-NH3↑+H2O+CO32-,选项D错误;答案选C。 4.下列说法正确的是( ) A. SiO2、CO2都是酸性氧化物,都能与NaOH溶液反应 B. Na2O、Na2O2组成元素相同,与CO2反应的产物相同 C. SO2、NO、CO2都是大气污染物,在空气中都能稳定存在 D. HCl、HNO3都是强酸,和FeO的反应都属于复分解反应 【答案】A 【解析】 【详解】A.SiO2、CO2都是酸性氧化物,都能与NaOH溶液反应生成相应的钠盐和水,A正确; B.Na2O、Na2O2组成元素相同,与CO2反应的产物不相同,后者还有氧气生成,B错误; C.SO2、NO都是大气污染物,CO2不是大气污染物,其中NO在空气中不能稳定存在,易被氧化为NO2,C错误; D.HCl、HNO3都是强酸,盐酸和FeO的反应属于复分解反应,硝酸具有强氧化性,与氧化亚铁发生氧化还原反应,D错误。 答案选A。 【点晴】该题的易错选项是D,有关硝酸参与的化学反应,除了要明确硝酸的强酸性以外,还应该特别注意硝酸的强氧化性,尤其时与还原性物质反应时,常见的考点有与氧化亚铁,与四氧化三铁,与硫化亚铁等有关反应的方程式判断。 5.已知常温常压下在1 L水中可溶解40 L NO2,NO2能与NaOH溶液发生反应:2NaOH+2NO2===NaNO3+NaNO2+H2O。以下各种尾气吸收装置中,不适合吸收NO2气体的是( ) A. B. C. D. 【答案】B 【解析】 【详解】由于常温常压下在1L水中可溶解40LNO2,即NO2易溶于水,且NO2易与NaOH反应,所以在吸收装置中需要有防止倒吸功能,装置B中漏斗颈部已浸没NaOH溶液中,不能防止溶液倒吸,答案选B。 6.孔雀石的主要成分是Cu2(OH)2CO3(含Fe2O3、FeCO3、Al2O3、SiO2杂质),工业上用孔雀石制备 硫酸铜的第一步需用过量的硫酸溶解并过滤。常温下,分别取滤液并向其中加入指定物质,反应后的溶液中大量存在的一组离子正确的是( ) A. 加入过量NaClO溶液:Fe2+、H+、Cu2+、SO42- B. 加入过量NaOH溶液:Na+、AlO2-、SO42-、OH- C. 加入过量氨水:Fe3+、NH4+、SO42-、OH- D. 加入过量NaHCO3溶液:Na+、Al3+、SO42-、HCO3- 【答案】B 【解析】 【详解】A、ClO-、Fe2+、H+发生氧化还原反应,加入过量NaClO溶液,Fe2+不能大量存在,故不选A ; B. 加入过量NaOH溶液,Na+、AlO2-、SO42-、OH-相互之间不反应,能大量共存,故选B; C. 加入过量氨水:Fe3+、OH-生成Fe(OH)3沉淀,不能大量共存,故不选C ; D. 加入过量NaHCO3溶液, Al3+、HCO3-发生反应生成氢氧化铝沉淀和二氧化碳,不能大量共存,故不选D。 7.X、Y、Z、W为原子序数依次增大的短周期元素。其形成的小分子化合物Y2X2、Z2X4、X2W2中,分子内各原子最外层电子都满足稳定结构。下列说法正确的是( ) A. X、Y、Z、W的原子半径的大小关系为W>Y>Z>X B. 在Y2X2、Z2X4、X2W2的一个分子中,所含的共用电子对数相等 C. 与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键 D. X、Y、Z、W四种元素可形成化学式为X7Y2ZW2化合物 【答案】D 【解析】 【分析】 X、Y、Z、W为原子序数依次增大的短周期元素。其形成的小分子化合物Y2X2、Z2X4、X2W2中,分子内各原子最外层电子都满足稳定结构,X、Y、Z、W分别是H、C、N、O;Y2X2是C2H2、Z2X4是N2H4 、X2W2是H2O2。 【详解】A.同周期元素从左到右半径减小, H、C、N、O的原子半径的大小关系为C>N>O>H,故A错误; B. C2H2一个分子中有5对共用电子对、N2H4一个分子中有5对共用电子对、 H2O2一个分子中有3对共用电子对,故B错误; C. C、N、O形成的简单氢化物中H2O最稳定,是因为氧元素的非金属性最强,与 氢键无关,故C错误; D. H、C、N、O四种元素可形成醋酸铵(CH3COONH4),故D正确; 选D。 8.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是 A. 氯水的颜色呈浅绿色,说明氯水中含有Cl2 B. 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- C. 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ D. 向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO 【答案】D 【解析】 【详解】A、氯气是黄绿色气体,因此氯水的颜色呈浅绿色,说明氯水中含有Cl2,A正确; B、向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,白色沉淀是氯化银,这说明氯水中含有Cl-,B正确; C、向氯水中加入NaHCO3粉末,有气泡产生,气体是CO2,这说明氯水中含有H+,C正确; D、向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明反应中有氯化铁生成。由于氯气也能把氯化亚铁氧化生成氯化铁,因此不能说明氯水中含有HClO,D不正确。 答案选D。 9.为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是( ) A. 氢氧化钠溶液的作用是吸收多余的SO2气体 B. 反应管内产生的红色粉末可能是Fe2O3 C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3 D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1 【答案】C 【解析】 【详解】A、氢氧化钠溶液的作用是吸收多余的酸性气体,避免污染空气,A正确; B、硫酸亚铁受热分解,产生的红色固体一定含有Fe元素,所以可能是Fe2O3, B正确; C、如果二氧化硫气体,通入硝酸钡溶液中,因为二氧化硫溶于水溶液显酸性,酸性条件下,硝酸根离子将二氧化硫氧化为硫酸,再与钡离子生成硫酸钡沉淀,所以用硝酸钡溶液的问题是:无法判断使硝酸钡溶液出现白色沉淀的是二氧化硫还是三氧化硫, C错误; D、实验后反应管中残留固体为红色粉末(Fe2O3),BaCl2溶液中有白色沉淀产生(说明有SO3),品红溶液中红色褪去(说明有SO2),检查氢氧化钠溶液出口处无氧气产生,所以分解的方程式为:,所以氧化产物(Fe2O3)和还原产物(SO2)物质的量之比为1:1,D正确; 故选C。 10.甲、乙两烧杯中各盛有1L0.6mol· L-1的盐酸和 NaOH 溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体的体积比为V(甲) : V(乙)= 3: 4,则加入铝粉的质量为 A. 7.2 g B. 5.4 g C. 3.6 g D. 2.7 g 【答案】A 【解析】 【详解】甲、乙两烧杯中各盛有1L0.6mol· L-1的盐酸和 NaOH溶液,向两烧杯中分别加入等质量的铝粉,分别发生反应2Al+6HCl=AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑;反应结束后测得生成的气体的体积比为V(甲) : V(乙)= 3: 4,甲烧杯放出的氢气少,说明甲中铝有剩余,盐酸完全反应,n(HCl)=0.6mol,根据方程式2Al+6HCl=AlCl3+3H2↑,生成氢气的物质的量是0.3mol,则乙中生成氢气的物质的量是0.4mol,根据方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑,消耗铝的物质的量是,铝的质量是×27g/mol=7.2g,故选A。 11.下列除杂方案错误的是 选项 被提纯的物质 杂质 除杂试剂 除杂方法 A CO(g) CO2(g) NaOH 溶液、浓 H2SO4 洗气 B NH4Cl(aq) Fe3+(aq) NaOH溶液 过滤 C Cl2(g) HCl(g) 饱和食盐水、浓H2SO4 洗气 D Na2CO3(s) NaHCO3(s) — 灼烧 A. A B. B C. C D. D 【答案】B 【解析】 【详解】A.二氧化碳与NaOH反应,而CO不能,则洗气后利用浓硫酸干燥即可除杂,A正确; B.NaOH与NH4Cl、Fe3+均反应,将原物质反应掉,不符合除杂的原则,B错误; C.HCl极易溶于水,而食盐水抑制氯气的溶解,则洗气后利用浓硫酸干燥即可除杂,C正确; D.NaHCO3加热分解生成碳酸钠,则直接加热即可实现除杂,D正确; 答案选B。 12.能正确表示下列反应的离子方程式是( ) A. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O B. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3- C. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O D. 0.1 mol/L NH4Al(SO4)2溶液与0.2 mol/L Ba(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4+AlO2-+2H2O 【答案】C 【解析】 【详解】A.浓盐酸与KMnO4溶液发生氧化还原反应放出氯气,不能用盐酸酸化的KMnO4溶液,故A错误; B. 向次氯酸钠溶液中通入足量SO2气体,次氯酸根离子完全被还原为氯离子,二氧化硫被氧化为硫酸,故B错误; C. Fe3+能把I-氧化为I2,Fe2O3溶于过量氢碘酸溶液中,发生反应的离子方程式是Fe2O3+6H++2I-=2Fe2++I2+3H2O,故C正确; D. 0.1 mol/L NH4Al(SO4)2溶液与0.2 mol/L Ba(OH)2溶液等体积混合,完全反应生成硫酸钡、氢氧化铝沉淀、一水合氨,反应的离子方程式是:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4+Al(OH)3↓+NH3·H2O,故D错误; 选C。 13.下列实验中,对应现象以及结论都正确且两者具有因果关系的是 ( ) 选项 实验 现象 结论 A 将CO2通入BaCl2稀溶液中 产生白色沉淀 沉淀是BaCO3 B 向淀粉KI溶液中滴加FeCl3溶液 溶液变蓝色 氧化性:Fe3+>I2 C 向包裹Na2O2粉末的脱脂棉中吹入CO2气体 脱脂棉发生燃烧 Na2O2与CO2反应有O2生成 D 向CuSO4溶液中通入H2S 产生黑色沉淀 H2S属于强酸 A. A B. B C. C D. D 【答案】B 【解析】 【详解】A. 碳酸的酸性小于盐酸,二氧化碳与氯化钡溶液不反应,故不选A; B. 向淀粉KI溶液中滴加FeCl3溶液,溶液变蓝色,说明Fe3+把I-氧化为I2,故选B; C. 向包裹Na2O2粉末的脱脂棉中吹入CO2气体,脱脂棉发生燃烧,说明Na2O2与CO2反应放热且有O2生成,故不选C; D. 向CuSO4溶液中通入H2S ,产生黑色沉淀CuS,说明CuS难溶于硫酸,但H2S是弱酸,故不选D。 答案选B。 14.氯化铝(AlN)是一种新型无机非金属原料,常温下AlN+Na0H+H20=NaAl02+NH3↑。某课题小组利用甲图所示装置测定样品AlN的含量 (杂质不反应)。下列说法中正确的是 A. 量气管中的液体应为水 B. 用长颈漏斗代替分液漏斗,有利子控制反应速率 C. 反应结束时a、b两管液面的差值即为产生气体的体枳 D. 若其它操作均正确,实验结束时按乙图读数,测得AlN含量偏高 【答案】D 【解析】 【详解】A.反应产生的气体为氨气,氨气极易溶于水,所以量气管中的液体不应为水,可以为四氯化碳,A错误; B.长颈漏斗没有玻璃旋塞,不能控制液体的滴加,也就不能控制反应速率,B错误; C.反应结束时,待气体冷却到室温,调节右侧的量气管,使左右两端的液面相平,才能读数,根据起始和结束时右侧量气管的液面的差值,计算产生气体的体积,C错误; D.俯视量气管的读数,使所量气体的体积增大,氨气的量增大,氮化铝的量增大,测得AlN 含量偏高,D正确; 答案选D。 【点睛】用量气法测量气体的体积时要注意,一定要等到反应结束后冷却到室温;通过上下调节量气管的位置,保持量气装置两端的液面要保持水平;读数时一定要平视。 15.向KOH溶液中通入11.2L(标准状况)氯气恰好完全反应生成三种含氯盐:0.7molKCl、0.2molKClO和X,则X是( ) A. 0.1molKClO4 B. 0.1molKClO3 C. 0.2molKClO2 D. 0.1molKClO2 【答案】B 【解析】 【详解】11.2L(标准状况)氯气的物质的量为:=0.5mol,生成物中含0.7molKCl、0.2molKClO,根据氯守恒,所以X的物质的量为:0.5mol×2-0.7mol-0.2mol=0.1mol,设X中Cl的化合价为x价,由电子得失守恒分析可知:0.7mol×1=0.2mol×1+0.1mol×(x-0),解得x=5,所以X中氯的化合价为+5价,则X为KClO3,物质的量为0.1mol,故选B。 【点睛】明确得失电子守恒和氯守恒为解答关键。 16.在一密闭容器中有HCHO、H2和O2混合气体共20g,放入足量Na2O2用电火花引燃,使其完全反应,Na2O2增重8g,则原混合气体中O2的质量分数是 A. 40% B. 33.3% C. 60% D. 36% 【答案】C 【解析】 【详解】由于HCHO可以看作是CO·H2,所以气体燃烧后再通过过氧化钠吸收后,过氧化钠增加质量就是原混合气中氢气和甲醛的质量,则氧气的质量是12g,质量分数是12÷20=0.6,即60%,答案选C。 17.已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是 A. 若A是铁,则E可能为稀硝酸 B. 若A是CuO,E是碳,则B为CO C. 若A是NaOH溶液,E是CO2,则B为NaHCO3 D. 若A是AlCl3溶液,E可能是氨水 【答案】D 【解析】 【详解】A、如果A是Fe,E为稀硝酸,B为Fe(NO3)3,D为Fe(NO3)2,Fe(NO)3和Fe反应生成Fe(NO3)2,Fe(NO3)2和硝酸反应生成Fe(NO3)3,符合转化关系,故说法正确; B、C+CuO=Cu+CO2,过量的C和CO2发生反应:C+CO2=2CO,因此B为CO,D为CO2,符合转化关系,故说法正确; C、2NaOH+CO2(少量))=Na2CO3+H2O,NaOH+CO2(过量)=NaHCO3、2NaHCO3Na2CO3+CO2↑+H2O,Na2CO3+CO2+H2O=2NaHCO3,符合转化关系,故说法正确; D、氢氧化铝溶于强碱,不溶于弱碱,无论氨水是否过量,生成都是氢氧化铝沉淀,不符合转化关系,故说法错误。 答案选D。 18.下列说法不正确的是 ( ) A. 向Na2CO3溶液中逐滴加入HCl,直到不再生成CO2气体为止,在此过程中,溶液中的HCO3-浓度变化是先变大后变小(溶液体积变化均忽略不计) B. 向NaHCO3溶液中加入Ba(OH)2固体,CO32-的浓度变化是先变大后变小(溶液体积变化均忽略不计) C. 将等质量的Na2O和Na2O2样品分别放入等量的水中,所得溶液的质量分数分别为a%和b%,则a、b的关系是:a=b D. 有含0.2 mol Na2CO3和含0.3 mol HCl的两种溶液:①将Na2CO3溶液逐滴滴入HCl溶液中;②将HCl溶液逐滴滴入Na2CO3溶液中;①②两种操作生成的CO2体积之比为3∶2 【答案】C 【解析】 【详解】A. 向Na2CO3溶液中逐滴加入HCl,依次发生反应的离子方程式:CO32-+H+=HCO3-、HCO3-+H+=CO2+H2O,溶液中的HCO3-浓度变化是先变大后变小,故A正确; B.向NaHCO3溶液中加入Ba(OH)2固体,首先生成碳酸钡和碳酸钠,继续加Ba(OH)2固体,碳酸钠转化为碳酸钡沉淀,所以CO32-的浓度变化是先变大后变小,故B正确; C. 设Na2O和Na2O2质量都是1g,水的质量都是mg,n(Na2O)= 、n(Na2O2)=;氧化钠和水反应生成氢氧化钠,生成氢氧化钠的质量是,所得溶液的质量是(1+m)g,氢氧化钠的质量分数是 ;Na2O2溶于水生成氢氧化钠和氧气,生成氢氧化钠的质量是,生成氧气的质量是,所得溶液的质量是(1+m-)g,氢氧化钠的质量分数是,所以a>b,故C错误; D.将Na2CO3溶液逐滴滴入HCl溶液中,立即生成二氧化碳气体,二氧化碳的物质的量是0.15mol;将HCl溶液逐滴滴入Na2CO3溶液中,先生成碳酸氢钠,然后碳酸氢钠再和剩余盐酸反应生成二氧化碳,生成二氧化碳0.1mol,①②两种操作生成的CO2体积之比为3∶2,故D正确; 选C。 19.下列设计的实验方案能达到实验目的的是() A. 制备Al(OH)3悬浊液:向1mol·L-1的AlCl3溶液中加过量的6mol·L-1NaOH溶液 B. 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入氢氧化钠溶液,振荡后静置分液,并除去有机相的水 C. 检验溶液中是否含有Fe3+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象 D. 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 【答案】D 【解析】 【详解】A.Al(OH)3是两性氢氧化物,可以和过量氢氧化钠反应生偏铝酸钠,故不能制备氢氧化铝悬浊液,A错误; B.氢氧化钠也和乙酸乙酯反应,应该用饱和碳酸钠除去乙酸,然后分液即可,B错误; C.氯水具有强氧化性,可能把Fe2+氧化成Fe3+,也会出现上述现象,C错误; D.两试管做对比实验,如果第二支试管冒出气泡多与第一支,说明FeCl3是催化剂,加快反应速率,D正确。 答案选D。 【点睛】实验方案设计要求最简,对环境危害小,实验能否成功需要看细节,氢氧化铝呈两性,氢氧化钠过量,会使氢氧化铝溶解;实验室常用氨水,离子检验要防止其他离子的干扰,特别注意氯离子干扰,因此平时学习时多注意细节问题,注意相关基础知识的积累和灵活应用。 20.将9.0 g铜和铁的混合物投入100 mL稀硝酸中并加热,充分反应后得到标准状况下1.12 L NO,剩余4.8 g金属;继续加入100 mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下1.12 L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法正确的是 ( ) A. 原混合物中铜和铁的物质的量均为0.075 mol B. 反应前稀硝酸的物质的量浓度无法计算 C. 若向上述最后所得溶液中再加入足量稀硝酸,还可得到标准状况下1.12 L NO D. 第一次与100 mL稀硝酸反应后剩余的4.8 g金属为铜和铁 【答案】A 【解析】 【分析】 第一次加硝酸时金属有剩余,无论参加反应的是铁还是铁和铜,溶解的4.2克金属均被氧化到+2价:3Fe(或3Cu)+8HNO3=3Fe(NO3)2[或3Cu(NO3)2]+2NO↑+4H2O,金属的物质的量为×=0.075mol ,则第一次溶解的金属摩尔质量为56g·mol-1,所以第一次溶解的是铁。第二次加硝酸后的溶液不能使KSCN溶液变红,溶解的4.8克金属也一定被氧化到+2价,同理可得其物质的量为0.075mol,金属摩尔质量为64g·mol-1,是铜。 【详解】A. 根据分析,第一次溶解的是0.075mol铁,第二次溶解的是0.075mol铜,原混合物中铜和铁的物质的量均为0.075 mol,故A正确; B. 根据氮元素守恒,反应前稀硝酸的物质的量浓度为 =2mol/L,故B错误; C. 若向上述最后所得溶液中再加入足量稀硝酸,亚铁离子被氧化为铁离子,反应为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,生成NO的物质的量是,标准状况下的体积为0.56 L NO,故C错误; D. 根据以上分析,第一次与100 mL稀硝酸反应后剩余的4.8 g金属为铜,不含铁,故D错误; 选A。 【点睛】本题考查混合物的有关计算,利用整体法解答及判断最终的产物是关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的化学计算能力。 21.将一定质量的镁铜合金加入到100 mL某浓度HNO3中,两者恰好反应,假设反应的还原产物只有NO气体。反应后向所得溶液中加入物质的量浓度为3 mol/L的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g;则下列有关叙述中不正确的是( ) A. 开始加入合金的总物质的量为0.15 mol B. 生成NO气体体积在标准状况下为2.24 L C. 生成沉淀完全时消耗NaOH溶液体积为100 mL D. 参加反应的硝酸的物质的量浓度为1 mol/L 【答案】D 【解析】 【分析】 将一定量的镁和铜合金加入到HNO3中,二者恰好反应,发生反应:3Mg+8HNO3(稀)═3 Mg(NO3)2+2NO↑+4H2O、3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O;向反应后的溶液中加入3mol/L NaOH溶液至沉淀完全,发生反应:Mg(NO3)2+2NaOH═Mg(OH)2↓+2NaNO3、Cu(NO3)2+2NaOH═Cu(OH)2↓+2NaNO3,沉淀为氢氧化镁和氢氧化铜,生成沉淀的质量比原合金的质量增加5.1g,则氢氧化镁和氢氧化铜含有氢氧根的质量为5.1g,氢氧根离子的物质的量是,根据电荷守恒可知,Mg2+、Cu2+所带正电荷总数是0.3mol,根据得失电子守恒,生成NO的物质的量是0.1mol,溶液呈电中性,则和硝酸反应后的溶液中含NO3-的物质的量是0.3mol。 【详解】A,Mg2+、Cu2+所带正电荷总数是0.3mol,则开始加入合金的总物质的量为0.3mol ÷2=0.15 mol,故A正确; B、Mg2+、Cu2+所带正电荷总数是0.3mol,根据得失电子守恒,生成NO的物质的量是0.1mol,在标准状况下为0.1mol×22.4L/mol= 2.24 L,故B正确; C、反应消耗氢氧根离子的物质的量是,则氢氧化钠溶液的体积是=0.1L,故C正确; D. 根据氮元素守恒,参加反应的硝酸的物质的量是反应后的溶液中含NO3-的物质的量加NO 的物质的量,硝酸的浓度是4mol/L,故D错误; 选D。 【点睛】本题结合镁、铜与硝酸的反应考查混合物有关计算,重点考查得失电子守恒、电荷守恒、元素守恒等,注意掌握守恒思想在化学计算中的应用方法。 22.A、B、D、E、F为短周期元素,非金属元素 A 最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的 2 倍。 B在 D中充分燃烧能生成其最高价化合物 BD2。E+与D2-具有相同的电子数。 A 在 F中燃烧,产物溶于水得到一种强酸。回答下列问题: (1)A在周期表中位置是____________,写出单质 F和NaOH的离子方程式____________。 (2)B、D、E 组成的一种盐中, E的质量分数为43%,其俗名为________ ,其水溶液与等物质的量的 F单质反应的化学方程式为___________________; (3)由这些元素组成的物质,其组成和结构信息如下表: a的化学式为_______;b与水反应的化学方程式为_______; 【答案】 (1). 第一周期IA主族 (2). Cl2 + 2OH-=Cl— + ClO— + H2O (3). 纯碱 (4). Na2CO3+ Cl2 +H2O= NaHCO3 +NaCl+ HClO (5). NaH (6). 2Na2O2 +2H2O=4NaOH+O2↑ 【解析】 【分析】 非金属元素A最外层电子数与其周期数相同,A为H元素;A 在 F中燃烧,产物溶于水得到一种强酸,F是Cl元素;D形成D2-,说明D最外层有6个电子,E+与D2-具有相同的电子数,E是Na元素、D是O元素;B在 D中充分燃烧能生成其最高价化合物 BD2,B为+4价,B的最外层电子数是其所在周期数的 2 倍,则B是C元素。据此解答。 【详解】(1)A是H元素,在周期表中的位置是第一周期IA主族,单质 F是氯气,氯气和NaOH反应生成氯化钠、次氯酸钠和水,反应的离子方程式是Cl2 + 2OH-=Cl- + ClO- + H2O; (2)C、O、Na 组成的一种盐中, Na的质量分数为43%,该盐是Na2CO3 ,其俗名为纯碱,氯气和水反应生成盐酸和次氯酸,酸性HCl>H2CO3>HClO>HCO3-,根据强酸制弱酸,碳酸钠与等物质的量的氯气反应生成碳酸氢钠、氯化钠、次氯酸,反应方程式是Na2CO3+ Cl2 +H2O= NaHCO3 +NaCl+ HClO; (3)金属元素与非金元素易形成离子化合物,含有H的二元离子化合物是NaH;b是含有非极性共价键的二元离子化合物,原子个数比是1:1,b是Na2O2,Na2O2与水反应生成氢氧化钠和氧气,反应的化学方程式为2Na2O2 +2H2O=4NaOH+O2↑。 23.联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题: (1)联氨分子的电子式为__________,其中氮的化合价为______。 (2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的离子方程式____________。 (3)联氨和N2O4可作为火箭推进剂,其反应的产物均无污染。其氧化产物和还原产物之比为 _______。 (4)联氨为二元弱碱,在水中的电离方程式与氨相似。联氨与硫酸形成的酸式盐的化学式为______________。 【答案】 (1). (2). -2 (3). 2NH3+NaClO=N2H4+ NaCl+ H2O (4). 2:1 (5). N2H6(HSO4)2 【解析】 【详解】(1)联氨分子式为N2H4,氮原子形成3个单键,电子式为,根据化合价代数和等于0,其中氢元素化合价为+1价,则氮元素化合价为-2价。 (2)次氯酸钠把氨气氧化为联氨,次氯酸钠被还原为氯化钠,根据得失电子守恒,反应的方程式是2NH3+NaClO=N2H4+ NaCl+ H2O。 (3)联氨和N2O4可作为火箭推进剂,反应的产物为无污染的氮气和水,N2O4中N元素化合价由+4降低为0、N2H4中N元素化合价由-2升高为0;根据得失电子守恒,其氧化产物和还原产物之比为2:1; (4)联氨为二元弱碱,在水中的电离方程式与氨相似,形成阳离子为N2H62+,与硫酸形成的酸式盐的化学式为N2H6(HSO4)2。 24.某校学生化学实验小组,为验证非金属元素氯的氧化性强于硫和氮,设计了一套实验装置:(部分夹持装置已略去) (1)写出A中反应的离子方程式___________________________。 (2)写出F中反应的化学方程式_________________________。 (3)B中浸有NaOH溶液的棉花作用___________________,B中溶液出现现象_______________,写出B中发生的离子反应_________________。 (4)E中干燥管装的干燥剂是________,检验F中气体的方法______________。 (5)D中干燥管中出现的现象______________,D中干燥管中化学方程式_________________。 【答案】 (1). MnO2 +4H++2Cl-Mn2++Cl2↑+2H2O (2). Ca(OH)2+2NH4ClCaCl2+2NH3↑+2H2O (3). 吸收过量的氯气,防止污染环境 (4). 有淡黄色沉淀生成 (5). S2- +Cl2 =S +2Cl- (6). 碱石灰 (7). 湿润的红色石蕊试纸变蓝 (8). 有白烟生成 (9). 8NH3+3Cl2=N2+6NH4Cl 【解析】 【详解】(1)反应装置A为浓盐酸和二氧化锰共热制备氯气,其离子方程式为:MnO2+4H++2Cl-Mn2++Cl2↑+2H2O; (2)装置F中氯化铵和氢氧化钙加热制取氨气,反应的化学方程式是Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O; (3)氢氧化钠溶液能与氯气反应生成氯化钠、次氯酸钠,B中浸有NaOH溶液的棉花作用是吸收过量的氯气,防止污染环境;B中Na2S和氯气反应生成氯化钠和硫单质,B中的现象是有淡黄色沉淀生成,反应的离子方程式是S2- +Cl2 =S +2Cl-; (4)氨气是碱性气体,一般用碱石灰干燥氨气,E中干燥管装的干燥剂是碱石灰;氨气的水溶液呈碱性,氨气能使湿润的红色石蕊试纸变蓝,用湿润的红色石蕊试纸检验氨气; (5)氨气、氯气反应生成氯化铵和氮气,D 中干燥管中出现的现象是有白烟生成,反应方程式是8NH3+3Cl2=N2+6NH4Cl。 【点睛】本题考查实验方案的设计与评价,考查了氯气、氨气的实验室制法及性质的检验,明确制备原理及物质的性质是解题关键,会根据氧化性强弱判断非金属性。 25.高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题: 相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下: 金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+ 开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9 沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9 (1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______________________________________。 (2)“氧化”中添加适量的MnO2的作用是将________________________,检验生成离子试剂___________。 (3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间,除铝的离子反应方程式是__________。 (4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。 (5)氧化中除了添加适量MnO2还可以用H2O2来氧化,写出该离子反应_______________。 (6)写出“沉锰”的离子方程式_______________________________________。 (7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=时,z=___________。 (8)写出Fe2+和HNO3的离子反应__________。 【答案】 (1). SiO2(不溶性硅酸盐) (2). MnO2+MnS+2H2SO4=2MnSO4+S+2H2O (3). 将Fe2+氧化为Fe3+ (4). KSCN溶液 (5). 4.7 (6). Al3++3NH3·H2O=Al(OH)3↓+3NH4+ (7). NiS和ZnS (8). 2Fe2++H2O2+2H+=2Fe3+ +2H2O (9). Mn2++2=MnCO3↓+CO2↑+H2O (10). (11). 3Fe2+ +4H++NO3-=3Fe3++NO↑+2H2O 【解析】 【分析】 (1)SiO2难溶于硫酸;“溶浸”中二氧化锰能氧化硫化锰生成硫酸锰、硫和水; (2)MnO2具有氧化性,可以将Fe2+氧化为Fe3+;KSCN溶液遇Fe3+变红; (3)Fe3+完全沉淀的pH是2.8,Al3+完全沉淀的pH是4.7;氨水与硫酸铝反应生成氢氧化铝沉淀和硫酸铵; (4)加入Na2S除去Zn2+和Ni2+,生成沉淀NiS和ZnS; (5)H2O2和Fe2+反应,氧化产物是Fe3+、还原产物是H2O; (6)“沉锰”过程中硫酸锰和碳酸氢铵反应生成碳酸锰沉淀、硫酸铵、二氧化碳; (7)根据元素化合价代数和等于0计算z值; (8)Fe2+和HNO3发生氧化还原反应,氧化产物是Fe3+、还原产物是NO。 【详解】(1)SiO2难溶于硫酸,所以“滤渣1”含有SiO2;“溶浸”中二氧化锰能氧化硫化锰生成硫酸锰、硫和水,根据得失电子守恒,反应方程式是MnO2+MnS+2H2SO4=2MnSO4+S+2H2O; (2)MnO2具有氧化性,“氧化”中添加适量的MnO2的作用是将Fe2+氧化为Fe3+;KSCN溶液遇Fe3+变红,检验Fe3+的试剂是KSCN溶液; (3)Fe3+完全沉淀的pH是2.8,Al3+完全沉淀的pH是4.7,“调pH”除铁和铝,溶液的pH范围应调节为4.7~6之间,氨水与硫酸铝反应生成氢氧化铝沉淀和硫酸铵,反应的离子方程式是Al3++3NH3∙H2O=Al(OH)3↓+3NH4+; (4)加入Na2S除去Zn2+和Ni2+,生成沉淀NiS和ZnS,所以“滤渣3”的主要成分是NiS和ZnS; (5)H2O2和Fe2+反应,氧化产物是Fe3+、还原产物是H2O,反应的离子方程式是2Fe2++H2O2+2H+=2Fe3+ +2H2O; (6)“沉锰”过程中硫酸锰与碳酸氢铵反应生成碳酸锰沉淀、硫酸铵、二氧化碳,反应的离子方程式是Mn2++2=MnCO3↓+CO2↑+H2O; (7)LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=时,根据元素化合价代数和等于0,1+2+3+4z-2×2=0,z=; (8)Fe2+和HNO3发生氧化还原反应,氧化产物是Fe3+、还原产物是NO,根据得失电子守恒,反应的离子方程式是3Fe2+ +4H++NO3-=3Fe3++NO↑+2H2O。 26.磷化铝、磷化锌、磷化钙与水反应产生高毒的PH3气体(熔点为-132℃,还原性强、易自燃),可用于粮食熏蒸杀虫。卫生安全标准规定:当粮食中磷化物(以PH3计)的含量低于0.05mg·kg-1时算合格。可用以下方法测定粮食中残留的磷化物含量: 【操作流程】安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸钠标准溶液滴定。 【实验装置】C中盛100 g原粮,D中盛有 20.00 mL 1.12×10-4 mol • L-1KMnO4溶(H2SO4酸化)。 (1)仪器C的名称是_________;原粮最好先打成粉末,其原因是_____________。 (2)磷化钙与水反应化学方程式为_____________________________________;检查整套装置气密性良好的方法是_______________________________________。 (3)A中盛装KMnO4溶液的作用是除去空气中的还原性气体;B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的O2,防止___________;通入空气的作用是____________。 (4)D中PH3被氧化成磷酸,所发生反应的离子方程式为_________________________。 (5)把D中吸收液转移至容量瓶中,加水稀释至250mL,取25.00mL于锥形瓶中,用5.0×10-5mol • L-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,写出该反应的离子方程式________________,消耗标Na2SO3准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为______mg • kg-1。 (6)滴定结束的现象_____________________。 【答案】 (1). 三颈烧瓶 (2). 使原粮中磷化物与水充分反应 (3). Ca3P2 + 6H2O=3Ca(OH)2 +2PH3 (4). 关闭K1,打开K2用抽气泵缓慢抽气,若观察到A,B,D的装置中有气泡产生则气密性良好 (5). 氧化装置C中生成的PH3 (6). 吹出PH3使其全部被酸性高锰酸钾溶液吸收 (7). 5PH3 + 8MnO4— +24H+ =5H3PO4 +8Mn2+ + 12H2O (8). 2MnO4—+ 5SO32-+6H+=2Mn2++5SO42- +3H2O (9). 0.0085 (10). 滴入最后一滴标准液紫色褪去且30s 不恢复 【解析】 【分析】 (1)根据装置图分析仪器C的名称;原粮打成粉末可以增大与水的接触面积; (2)磷化钙与水反应生成氢氧化钙和磷化氢;用抽气泵缓慢抽气,依据连续装置中的压强变化判断装置气密性; (3)PH3具有较强还原性,用高锰酸钾溶液吸收原粮放出的PH3,根据消耗高锰酸钾的物质的量计算磷化物含量; (4)D中PH3被高锰酸钾氧化成磷酸,高锰酸钾被还原为锰离子; (5)高锰酸钾被Na2SO3溶液还原为锰离子,Na2SO3被氧化为Na2SO4;根据方程式计算PH3的含量; (6)高锰酸钾溶液呈紫色,滴定结束紫色褪去。 【详解】(1)根据装置图可知,仪器C的名称是三颈烧瓶;原粮打成粉末可以增大与水的接触面积,使原粮中磷化物与水充分反应; (2)磷化钙与水反应生成氢氧化钙和磷化氢,化学方程式为Ca3P2 + 6H2O=3Ca(OH)2 +2PH3;检查整套装置气密性良好的方法是:关闭K1,打开K2用抽气泵缓慢抽气,若观察到A、B、D的装置中有气泡产生则气密性良好; (3)实验原理是:用高锰酸钾溶液吸收原粮放出的PH3,根据消耗高锰酸钾的物质的量计算磷化物含量, B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的O2,防止氧气氧化装置C中生成的PH3;通入空气的作用是吹出PH3使其全部被酸性高锰酸钾溶液吸收。 (4)D中PH3被高锰酸钾氧化成磷酸,高锰酸钾被还原为锰离子,根据得失电子守恒,发生反应的离子方程式为5PH3 + 8MnO4- +24H+ =5H3PO4 +8Mn2+ + 12H2O; (5)高锰酸钾被Na2SO3溶液还原为锰离子,Na2SO3被氧化为Na2SO4,反应的离子方程式是2MnO4-+ 5SO32-+6H+=2Mn2++5SO42- +3H2O;加水稀释至25mL,用浓度为5×10-5mol/L Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL;依据滴定反应2MnO4-+ 5SO32-+6H+=2Mn2++5SO42- +3H2O 可知2KMnO4~5Na2SO3;未反应的高锰酸钾物质的量=0.011L×5×10-5mol/L×=2.2×10-7mol;与PH3反应的高锰酸钾物质的量= 0.02L×1.12×10-4 mol•L-1-2.2×10-7mol=0.04×10-6mol,根据反应5PH3 + 8MnO4- +24H+ =5H3PO4 +8Mn2+ + 12H2O得到定量关系为:5PH3~8KMnO4,PH3的物质的量为 0.04×10-6mol×=2.5×10-8 mol,PH3的质量为2.5×10-8 mol×34g/mol=8.5×10-7g,则该原粮中磷化物(以PH3计)的含量为8.5×10-4mg/0.1 kg =0.0085mg•kg-1; (6)高锰酸钾溶液呈紫色,滴定结束的现象是滴入最后一滴标准液紫色褪去且30s不恢复。 【点睛】本题以粮食中残留磷化氢的定量测定为命题背景,考查氧化还原反应滴定及相关计算,明确非常规装置气密性的检验方法,重点是滴定实验原理的理解和定量测定的计算。 27.有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对电子,F原子核外电子数是B 与C核外电子数之和,D是主族元素且与E同周期,E能形成红色或砖红色E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示。请回答下列问题: (1)C原子基态时的电子排布式为_______________,元素A、B、C、F的原子半径由大到小的顺序_________。 (2)A2F的分子空间构型为_______________,FO3分子中F原子的杂化方式______________。 (3)从图中可以看出,D 与B形成的离子化合物的化学式为__________(用元素符号表示),该离子晶体的密度为ag·cm-3,则晶胞的体积是_________(写出表达式即可,不用化简)。 (4)已知E单质的晶体为面心立方最密堆积 (在晶胞的顶点和面心均含有一个E原子),则E的晶体中E原子的配位数为________。 (5)氮化硼(BN)是一种重要的功能陶瓷材料,其晶胞结构如图所示。请回答下列问题: B和N相比,电负性较大的是_________,氮化硼的晶体类型______,氮化硼的晶胞中有几个氮原子_________。 【答案】 (1). 1s22s22p3 或[He]2s22p3 (2). S>N>F>H (3). V形 (4). sp2 (5). CaF2 (6). (7). 12 (8). N (9). 原子晶体 (10). 4 【解析】 【分析】 A是周期表中原子半径最小的元素,A为H元素;B是电负性最大的元素,B为F元素;C的2p轨道中有三个未成对电子,C的电子排布式是1s22s2sp3,C为N元素;F原子核外电子数是B 与C核外电子数之和,F是S元素;E能形成红色或砖红色E2O和黑色的EO两种氧化物,E是Cu元素;根据 D与F元素可形成离子化合物的晶胞结构图,可知D与F元素形成离子化合物化学式是DF2,D为+2价,D是主族元素且与E同周期,D是Ca元素。据此解答。 【详解】(1)C是N元素,核外有7个电子,基态时的电子排布式为1s22s22p3;电子层数越多半径越大,电子层数相同,质子数越多半径越小,元素H、F、N、S的原子半径由大到小的顺序S>N>F>H; (2)H2S中S原子的价电子对数是4,有2对孤电子对,分子空间构型为V形,SO3分子中S原子的价电子对数是,S的杂化方式是sp2; (3)根据均摊原则,Ca原子数是,F原子数是8,所以该离子化合物的化学式为CaF2,设晶胞的体积为V, ag·cm-3=,晶胞的体积是; (4)根据晶胞结构可知为面心立方最密堆积,原子的配位数为12; (5)同周期元素从左到右,电负性增大,B和N相比,电负性较大的是N,氮化硼是功能陶瓷材料,晶体类型是原子晶体,根据均摊原则,1个晶胞中氮原子有4个。查看更多