- 2021-07-05 发布 |
- 37.5 KB |
- 17页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
河北省衡水中学2020届高三上学期期中考试 化学
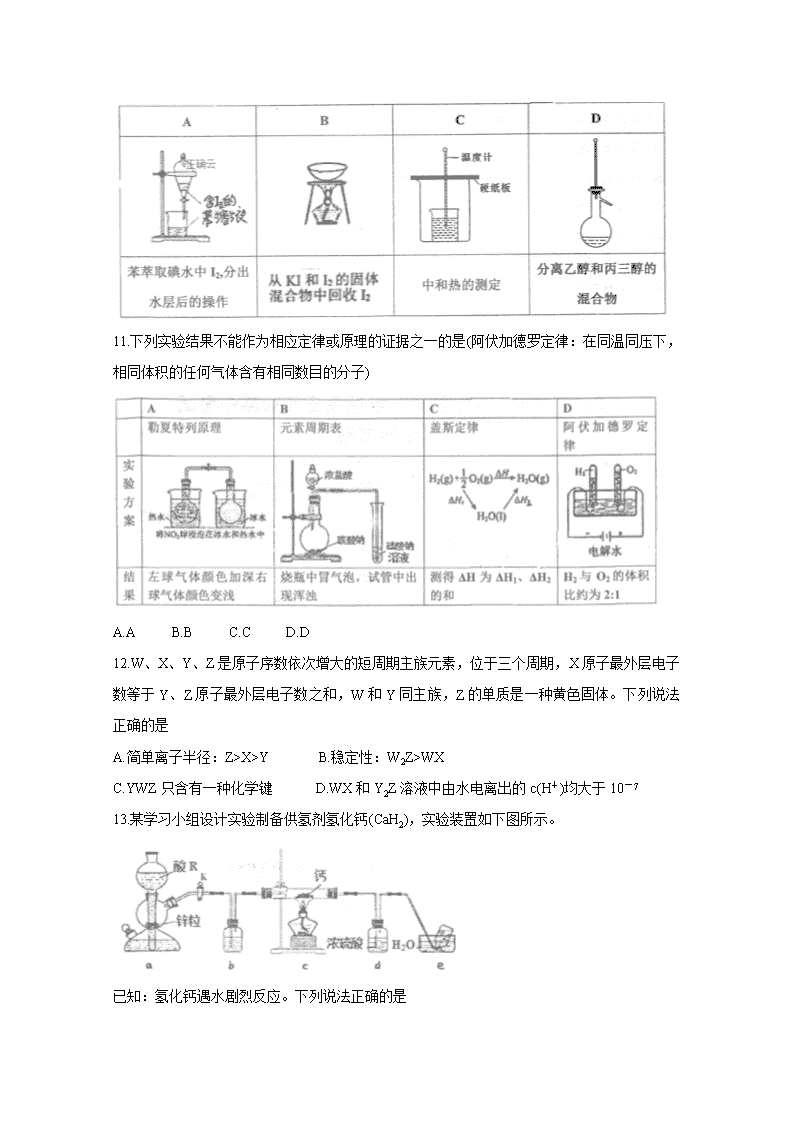
2019~2020学年度第一学期高三年级期中考试 化学试卷 本试卷分第I卷共30题,第II卷共5题。共100分。考试时间110分钟。 可能用到的原子量:C12 O16 S32 Cl35.5 Li7 Na23 Fe56 第I卷(选择题 共40分) 一、选择题(每小题只有一个选项符合题意。1×20=20分) 1.党的十九大强调树立“社会主义生态文明观”。下列做法不应该提倡的是 A.推广碳捕集和封存技术缓解温室效应 B.研发可降解高分子材料解决白色污染问题 C.用硅制作太阳能电池减少对化石燃料的依赖 D.工业污水向远海洋排放防止污染生活水源 2.中国是瓷器的故乡,钧瓷是宋代五大名窑瓷器之一,以“入窑一色出窑万彩”的神奇窑变著称。下列关于陶瓷的说法正确的是 A.高品质的白瓷晶莹剔透,属于纯净物 B.瓷器中含有大量的金属元素,因此陶瓷属于金属材料 C.氮化硅陶瓷属于传统无机非金属材料 D.“窑变”是高温下釉料中的金属化合物发生氧化还原反应导致颜色的变化 3.NA代表阿伏加德罗常数的值,下列说法正确的是 A.12g石墨和C60的混合固体中,含NA个碳原子 B.标准状况下,2.24L水中含有0.1NA个水分子 C.7.8g过氧化钠含有的共用电子对数为0.2NA D.5.6g铁在足量氯气中燃烧,电子转移数目为0.2NA 4.高温时,焦炭和水蒸气反应,所得气体含CO、CO2、H2和H2O,现用浓硫酸、无水硫酸铜、氧化铜、澄清石灰水、氢氧化钠溶液五种试剂,一次性检测气体中的CO、CO2和H2,下列说法不正确的是 A.气体检验的顺序应该是CO2、H2、CO B.检验CO和H2之前,需用浓硫酸将气体干燥后再完成后续实验 C.干燥气体通过灼热氧化铜后,可根据无水硫酸铜是否变蓝色来确定是否含H2 D.该实验中,澄清石灰水只需使用一次 5.实验室将NaClO3和Na2SO3按物质的量比2:1倒入烧瓶中,用水浴加热,同时滴入H2SO4 溶液,产生棕黄色的气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X为 A.ClO2 B.Cl2O C.Cl2 D.Cl2O3 6.化学与社会密切相关。下列叙述Ⅰ和Ⅱ都正确且二者有因果关系的是 选项 叙述I 叙述II A N2常作食品防腐剂 N2的密度与空气接近 B FeCl3常作净水剂 FeCl3具有氧化性 C MgO和Al2O3常作耐高温材料 MgO和Al2O3的熔点高、难分解 D 醋酸常用于清洗水壶中水垢 醋酸是强酸且醋酸钙、醋酸镁易溶于水 7.下列有关水处理方法不正确的是 A.用含碳铁粉处理水体中的NO3- B.用可溶性的铝盐和铁盐处理水中的悬浮物 C.用氯气处理水中的Cu2+、Hg2+等重金属离子 D.用烧碱处理含高浓度NH4+的废水并回收利用氨 8.对下列过程的化学用语表述正确的是 A.用硫酸铜溶液除去乙炔中的硫化氢气体:H2S+Cu2+=CuS↓+2H+ B.向氯化铝溶液中滴入过量氨水:Al3++4OH-=AlO2-+2H2O C.用电子式表示Na和Cl形成NaCl的过程: D.钢铁发生电化学腐蚀的正极反应:Fe-3e-=Fe3+ 9.研究海水中金属桥墩的腐蚀及防护是桥梁建设的重要课题。下列有关说法错误的是 A.桥墩的腐蚀主要是析氢腐蚀 B.钢铁桥墩在海水中比在河水中腐蚀更快 C.图1辅助电极的材料可以为石墨 D.图2钢铁桥墩上发生的反应是O2+2H2O+4e-=4OH- 10.下列有关实验的选项正确的是 11.下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子) A.A B.B C.C D.D 12.W、X、Y、Z是原子序数依次增大的短周期主族元素,位于三个周期,X原子最外层电子数等于Y、Z原子最外层电子数之和,W和Y同主族,Z的单质是一种黄色固体。下列说法正确的是 A.简单离子半径:Z>X>Y B.稳定性:W2Z>WX C.YWZ只含有一种化学键 D.WX和Y2Z溶液中由水电离出的c(H+)均大于10-7 13.某学习小组设计实验制备供氢剂氢化钙(CaH2),实验装置如下图所示。 已知:氢化钙遇水剧烈反应。下列说法正确的是 A.相同条件下,粗锌(含少量铜)比纯锌反应速率慢 B.酸R为浓盐酸,装置b中盛装浓硫酸 C.实验时先点燃酒精灯,后打开活塞K D.装置d的作用是防止水蒸气进入硬质玻璃管 14.由NO2、O2和熔融NaNO3组成的燃料电池如图所示在该电池工作过程中石墨I电极产生一种气态氧化物Y。下列说法正确的是 A.Y可能为NO B.电流由石墨I流向负载 C.石墨I上发生还原反应 D.石墨II上的电极反应:O2+2N2O5+4e-=4NO3- 15.短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可与其最高价氧化物的水化物反应生成盐,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。下列说法正确的是 A.W、X、Y、Z的简单离子的半径依次增大 B.X的简单氢化物的热稳定性比W的强 C.析出的黄色沉淀易溶于乙醇 D.X与Z属于同一主族,X与Y属于同一周期 16.下列实验过程可以达到实验目的的是 编号 实验目的 实验过程 A 配制0.1 mol/L的FeCl3溶液 称取16.25gFeCl3固体加入少量蒸馏水溶解,转移至1000mL容量瓶中定容 B 探究H2O2的氧化性 向盛有2mL酸性KMnO4溶液的试管中滴入H2O2的溶液,观察溶液颜色变化 C 制备纯净的SO2 向Na2SO3中加入浓硝酸,产生的气体通过浓硫酸 D 制备Fe(OH)3胶体 将饱和的FeCl3溶液滴入沸水中,继续加热至液体变为红褐色 A.A B.B C.C D.D 17.SO2与我们的生活息息相关,低浓度SO2 废气的处理是工业难题,目前常用的一种处理方法如下 已知:反应器中发生反应3H2+SO2=H2S+2H2O。 下列有关说法不正确的是 A.SO2是有毒气体,能形成酸雨破坏环境,不能用作食品的防腐剂 B.二乙醇胺的作用是吸收H2S,且可以循环使用 C.再生塔中加热分解重新获得H2S,主要目的是富集H2S D.理论上燃烧室中的O2可以用SO2代替 18.一种新型的合成氨的方法如图所示,下列说法错误的是 A.反应①属于“氮的固定” B.反应②属于非氧化还原反应 C.反应③可通过电解LiOH水溶液实现 D.上述三步循环的总结果为2N2+6H2O=4NH3+3O2 19.雌黄(As2S3)在我国古代常用作书写涂改修正液。浓硝酸氧化雌黄可制得硫磺,并生成砷酸和一种红棕色气体,利用此反应原理设计为某原电池。下列有关叙述正确的是 A.砷酸的分子式为H2AsO4 B.红棕色气体在该原电池的负极区生成并逸出 C.该反应的氧化剂和还原剂物质的量之比为12:1 D.该反应中每析出4.8g硫磺,则转移0.5 mol电子 20.海水提镁的主要流程如下,下列说法正确的是 ①试剂M是盐酸 ②流程中的反应全部都是非氧化还原反应 ③操作b只是过滤 ④用海水晒盐后的饱和溶液加石灰乳制Mg(OH2) ⑤采用电解法冶炼镁是因为镁很活泼 A.①②③④⑤ B.②③ C.④⑤ D.①④⑤ 二、选择题(每小题只有1个选项符合题意。10×2=20分) 21.常温下,下列各组离子在指定溶液中一定能大量共存的是 A.在NaClO和NaCl的混合溶液中:Ag+、K+、NO3-、I- B.=1×10-13 mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3- C.K+、Na+、Br-、SiO32-在溶液中能大量共存通入过量CO2后仍能大量共存 D.由水电离的c(H+)=1×10-13 mol·L-1的溶液中K+、Na+、AlO2-、CO32- 22.铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如下图。若上端开口关闭,可得到强还原性的H·(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的·OH(羟基自由基)。下列说法错误的是 A.无论是否鼓入空气,负极的电极反应式均为Fe-2e-=Fe2+ B.不鼓入空气时,正极的电极反应式为H++e-=H· C.鼓入空气时,每生成1 mol·OH有2 mol电子发生转移 D.处理含有草酸(H2C2O4)的污水时,上端开口应打开并鼓入空气 23.我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H原子将CO2高效还原为重要工业原料之一的甲醇,反应机理如图所示。下列有关说法不正确的是 A.CO2生成甲醇是通过多步还原反应实现的 B.催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒 C.该催化过程中只涉及化学键的形成,未涉及化学键的断裂 D.有可能通过调控反应条件获得甲醛等有机物 24.下表是某同学探究Na2SO3溶液和铬(VI)盐溶液反应规律的实验记录,已知:Cr2O72-(橙色)+H2O2CrO42-(黄色)+2H+ 序号 a b 现象 1 2mL0.05 mol·L-1K2Cr2O7溶液(pH=2) 3滴饱和Na2SO3溶液(pH=9) 溶液变绿色(含Cr3+) 2 2mL0.1 mol·L-1K2CrO4溶液(pH=8) 3滴饱和Na2SO3溶液 溶液没有明显变化 3 2mL饱和Na2SO3溶液 3滴0.05 mol·L-1K2Cr2O7溶液 溶液变黄色 4 2mL蒸馏水 3滴0.05 mol·L-1K2Cr2O7溶液 溶液变成浅橙色 下列说法不正确的是 A.实验1中的绿色溶液中含有SO42- B.实验1、2的a溶液中所含的离子种类相同 C.向实验3溶液中继续滴加过量硫酸可使溶液变为浅橙色 D.实验4的目的是排除稀释对溶液颜色变化造成的影响 25.热激活电池可用作火箭、导弹的工作电源。某种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能,此时硫酸铅电池处生成Pb,下列有关说法正确的是 A.输出电能时,外电路中的电子由硫酸铅电极流向钙电极 B.放电时电解质LiCl-KCl中的Li+向钙电极区迁移 C.每转移0.2 mol电子,理论上消耗42.5gLiCl D.电池总反应为Ca+PbSO4+2LiCl=Pb+Li2SO4+CaCl2 26.硫酸铵在一定条件下发生反应:4(NH4)2SO4=6NH3↑+3SO2↑+SO3↑+N2↑+7H2O ,将反应后的气体通入一定量的氯化钡溶液中恰好完全反应,有白色沉淀生成。下列有关说法正确的是 A.白色沉淀为BaSO4 B.白色沉淀为BaSO3和BaSO4的混合物,且n(BaSO3):n(BaSO4)约为1:1 C.白色沉淀为BaSO3和BaSO4的混合物,且n(BaSO3):n(BaSO4)约为3:1 D.从溶液中逸出的气体为N2,最后溶液中的溶质只有NH4Cl 27.在酸性条件下,黄铁矿(FeS2)催化氧化的反应方程式为2FeS2+7O2+2H2O=2Fe2++4SO42-+4H+,实现该反应的物质间转化如图所示。下列分析错误的是 A.反应I的离子方程式为4Fe(NO)2++O2+4H+=4Fe3++4NO+2H2O B.反应II的氧化剂是Fe3+ C.反应III是氧化还原反应 D.黄铁矿催化氧化中NO作催化剂 28.中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是 A.C3N4中C的化合价为-4 B.反应的两个阶段转移电子数相等 C.阶段II中,H2O2既是氧化剂,又是还原剂 D.通过该反应,实现了化学能向太阳能的转化 29.探究Na2O2与水的反应,实验如下: (已知:H2O2H++HO2-、HO2-H++O22-) 下列分析不正确的是 A.①、⑤中产生的气体能使带火星的木条复燃 B.①、④中均发生了氧化还原反应和复分解反应 C.②、⑤中KMnO4与MnO2的作用不同产生气体的量也不同 D.通过③能比较酸性:HCl>H2O2 30.空气中的硫酸盐会加剧雾霾的形成,我国科学家用下列实验研究其成因:反应室底部盛有不同吸收液,将SO2和NO2按一定比例混合,以N2或空气为载气通入反应室,相同时间后,检测吸收液中SO42-的含量,数据如下: 反应室 载气 吸收液 SO42-含量 数据分析 ① N2 蒸馏水 a ⅰ.b≈d>a≈c ⅱ.若起始不通过NO2,则最终检测不到SO42- ② 3%氨水 b ③ 空气 蒸馏水 c ④ 3%氨水 d 下列说法不正确的是 A.控制SO2和氮氧化物的排放是治理雾霾的有效措施 B.反应室①中可能发生反应:SO2+2NO2+2H2O=H2SO4+2HNO2 C.本研究表明:硫酸盐的形成主要与空气中O2有关 D.农业生产中大量使用铵态氮肥可能会加重雾霾的形成 第II卷(非选择题 共60分) 31.(12分)一定条件下,CH4和CO2都能与H2O形成笼状结构的水合物晶体,CH4与H2O形成的水合物俗称“可燃冰”。 (1)“可燃冰”晶体中平均每46个H2O分子构建8个笼,其中6个笼分别容纳1个CH4分子,另外2个笼分别容纳1个H2O分子,则“可燃冰”平均组成可表示为 (填化学式)。 (2)已知: CO2(g)+nH2O(l)=CO2·nH2O(s)△H=-57.98kJ· mol-1 CH4(g)+nH2O(l)=CH4·nH2O(s)△H=-54.49kJ· mol-1 反应CO2(g)+CH4·nH2O(s)=CH4(g)+CO2·nH2O(s)的△H= kJ· mol-1 (3)科学家提出用CO2“置换”CH4开采海底“可燃冰”的设想,提出该设想的理论依据是 。 (4)图中显示,CO2·nH2O的生产速率明显大于CH4·nH2O释放出的速率,其原因是 。 (5)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图。 ①反应(i)的化学方程式为 。 ②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是 。 32.(10分)高氯酸铵(NH4ClO4)常作火箭发射的推进剂,实验室用NaClO4、NH4Cl等原料制取(部分物质的溶解度如图1、图2),其实验流程如图3: (1)反应器中发生反应的基本反应类型是 。 (2)上述流程中由粗产品获得纯净高氯酸铵的方法为 。 (3)洗涤粗产品时,宜用 (填“0℃冷水”或“80°C热水”)洗涤。 (4)已知NH4ClO4在400℃时开始分解为N2、Cl2、O2、H2O。某课题组设计实验探究NH4ClO4的分解产物(假设装置内药品均足量,部分夹持装置已省略) 实验开始前,已用CO2气体将整套实验装置中空气排尽;焦性没食子酸溶液用于吸收氧气。 ①写出高氯酸铵分解的化学方程式 。 ②为了验证上述产物,按气流从左至右,装置的连接顺序为A→ (填装置对应的字母),证明氧气存在的实验现象为 。 ③若装置E硬质玻璃管中的Cu粉换成Mg粉,向得到的产物中滴加蒸馏水,产生使湿润的红色石蕊试纸变蓝的气体。滴加蒸馏水发生反应的化学方程式为 。 33.(16分) Ⅰ.太阳能、风能发电逐渐得到广泛应用,在发电系统中安装储能装置有助于持续稳定供电,其构造的简化图如下: (1)下列说法中,不正确的是 (填字母序号) a.太阳能、风能都是清洁能源 b.太阳能电池组实现了太阳能到电能的转化 c.控制系统能够控制储能系统是充电还是放电 d.阳光或风力充足时,储能系统实现由化学能到电能的转化 (2)全钒液流电池是具有发展前景的、用作储能系统的蓄电池。已知放电时V2+发生氧化反应,则放电时电极A的电极反应式为 。 (3)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+,Fe3+等进行综合处理可实现钒资源的回收利用,流程如下: 已知溶液pH范围不同时,钒的存在形式如下表所示: 钒的化合价 pH<2 pH>11 +4价 VO2+,VO(OH)+ VO(OH)3- +5价 VO2+ VO43- ①加入NaOH调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH后涉及到氧化物还原反应的化学反应方程式为 。 ②向碱性的滤液1(V的化合价为+4)中加入H2O2的作用是。 Ⅱ.氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在某工厂处理氨氮废水的流程如下: (4)Ⅰ中加入NaOH溶液,调pH=11并鼓入大量空气用离子方程式表示加NaOH溶液的作用式是 ;鼓入大量空气的目的是 。 (5)Ⅱ中加入适量NaClO溶液,控制pH在6~7,将氨氮转化为无毒物质。 过程Ⅱ发生3个反应: i.ClO-+H+=HClO ii.NH4++HClO=NH2Cl+H++H2O (NH2Cl中Cl元素为+1价) iii.…… 已知:水体中以+1价形式存在的氯元素有消毒杀菌的作用,被称为“余氯”。右图为NaClO加入量与“余氯”含量的关系示意图。其中氨氮含量最低的点是c点。 b点表示的溶液中氮元素的主要存在形式是(用化学式表示) ; 反应ⅲ的化学方程式是 。 (6)Ⅲ中用Na2SO3溶液处理含余氯废水,要求达标废水中剩余Na2SO3的含量小于5mg·L-1。若含余氯废水中NaClO的含量是7.45mg·L-1,则处理10m3含余氯废水,至多添加10%Na2SO3溶液 kg(溶液体积变化忽略不计)。 34.(12分) 某化学小组研究盐酸被氧化的条件,进行如下实验。 (1)研究盐酸被MnO2氧化。 实验 操作 现象 I 常温下将MmO2和12 mol·L-1浓盐酸混合 溶液呈浅棕色,有刺激泩气味 II 将Ⅰ中混合物过滤,加热滤液 生成大量黄绿色气体 III 加热MnO2和4 mol·L-1稀盐酸混合物 无明显现象 ①已知MnO2呈弱碱性。I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程是 。 ②II中发生了分解反应,反应的化学方程式是 。 ③III中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验Ⅳ进行探究: 将实验III、Ⅳ作对比,得出的结论是 。 ④用右图装置(a、b均为石墨电极)进行实验V: i.K闭合时,指针向左偏转 ii.向右管中滴加浓H2SO4至c(H+)≥7 mol·L-1,指针偏转幅度变化不大 iii.再向左管中滴加浓H2SO4至c(H+)≥7 mol·L-1,指针向左偏转幅度增大 将i和ii、iii作对比,得出的结论是 。 (2)研究盐酸能否被氧化性酸氧化。 ①烧瓶中放入浓H2SO4,通过分液漏斗向烧瓶中滴加浓盐酸,烧瓶上方立即产生白雾,用湿润的淀粉KI试纸检验,无明显现象。由此得出浓硫酸 (填“能”或“不能”)氧化盐酸。 ②向试管中加入3mL浓盐酸,再加入1mL浓HNO3,试管内液体逐渐变为橙色,加热,产生棕黄色气体,经检验含有NO2。 实验 操作 现象 I 将湿润的淀粉KI试纸伸入棕黄色气体中 试纸先变蓝,后褪色 II 将湿润的淀粉KI试纸伸入纯净Cl2中 试纸先变蓝,后褪色 III …… …… 通过实验I、II、III证明混合气体中含有Cl2,III的操作是 。 (3)由上述实验得出:盐酸能否被氧化与氧化剂的种类、 有关。 35.(10分)铵明矾[NH4Al(SO4)2·12H2O]是分析化学常用的基准试剂,工业上常用铝土矿(主要成分为Al2O3)来生产铵明矾,其中Z的水溶液可用于伤口消毒,其工艺流程图如下: (1)写出反应Ⅱ的离子方程式 。 (2)从反应IV的铵明矾溶液中获得铵明矾晶体的实验操作依次为 、 、过滤、洗涤(填操作名称)。 (3)反应Ⅵ的化学方程式为 。 (4)废水中含有Fe2+、Mn2+等金属离子对自然环境有严重的破坏作用,可用(NH4)2S2O8氧化除去。写出Mn2+被氧化生成MnO2的离子方程式为 。Z也有较强氧化性,在实际生产中不用Z氧化Mn2+的原因是 。查看更多